Introducción
La regulación del apetito constituye uno de los procesos fisiológicos más finamente ajustados del organismo, orientado a mantener la homeostasis energética mediante la integración dinámica entre señales internas y estímulos externos. Este sistema no solo determina cuándo iniciar o detener la ingesta de alimentos, sino que también modula la selección de nutrientes, la motivación por comer y la respuesta conductual asociada al alimento. (Morton et al., 2006; Berthoud, 2011)
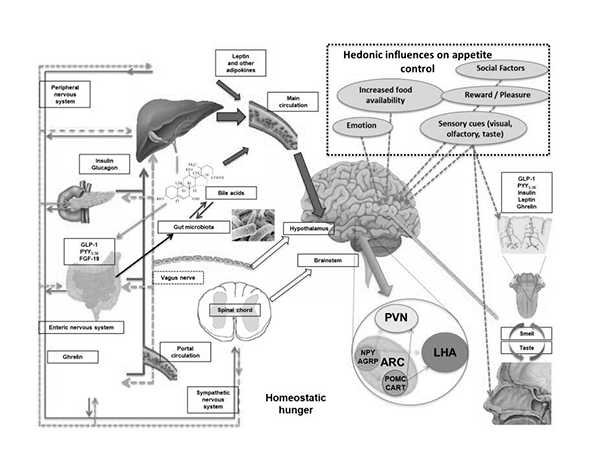
Lejos de ser un mecanismo lineal, el control del apetito emerge de la interacción entre múltiples sistemas: señales metabólicas periféricas (como leptina, grelina e insulina), circuitos neuronales centrales (principalmente en el hipotálamo y el tronco encefálico) y redes de recompensa que conectan con el sistema límbico. Esta integración permite al organismo ajustar la ingesta en función tanto de las necesidades energéticas como del contexto ambiental y emocional. (Schwartz et al., 2000; Grill & Hayes, 2012)
En este marco, el sistema endocannabinoide (SEC) actúa como un modulador transversal capaz de influir simultáneamente en los componentes homeostáticos y hedónicos de la alimentación. Su actividad se asocia a la facilitación de la ingesta, especialmente en condiciones de déficit energético o en presencia de estímulos altamente palatables, lo que lo sitúa como un nodo clave en la regulación del apetito. (Di Marzo & Matias, 2005; Kirkham, 2009)
La relevancia del SEC en este contexto radica en su capacidad para integrar señales periféricas y centrales, ajustando la excitabilidad neuronal en circuitos específicos y modulando la liberación de neurotransmisores implicados en la conducta alimentaria. Este papel no se limita al aumento del apetito, sino que participa en un sistema más amplio de regulación energética, donde intervienen procesos como el almacenamiento, el gasto energético y la señalización metabólica. (Pagotto et al., 2006)
Historia del descubrimiento
El estudio de la regulación del apetito tiene sus raíces en los trabajos clásicos de neurofisiología del siglo XX, donde se identificó por primera vez el papel central del hipotálamo en el control de la ingesta. Experimentos de lesión en modelos animales mostraron que daños en el hipotálamo lateral producían hipofagia, mientras que lesiones en el núcleo ventromedial generaban hiperfagia y aumento de peso, estableciendo así la idea de “centros del hambre y la saciedad”. (Anand & Brobeck, 1951)
A lo largo de las décadas siguientes, este modelo simplificado fue evolucionando hacia una visión más compleja, donde el hipotálamo se entiende como un integrador de múltiples señales periféricas. El descubrimiento de hormonas como la leptina, secretada por el tejido adiposo, supuso un punto de inflexión al demostrar que el estado energético del organismo se comunica activamente al cerebro mediante señales endocrinas. (Zhang et al., 1994)
En paralelo, la identificación de la grelina como hormona orexigénica producida principalmente en el estómago reforzó la idea de que el sistema digestivo participa activamente en la regulación del apetito, enviando señales que anticipan la ingesta y modulan la conducta alimentaria. (Kojima et al., 1999)
La implicación del sistema endocannabinoide en la regulación del apetito comenzó a esclarecerse a finales del siglo XX, a partir de observaciones farmacológicas que mostraban que los agonistas cannabinoides aumentaban la ingesta alimentaria. Este fenómeno, descrito inicialmente en estudios con Δ9-THC, apuntaba a la existencia de un sistema endógeno capaz de modular el comportamiento alimentario. (Williams et al., 1998)
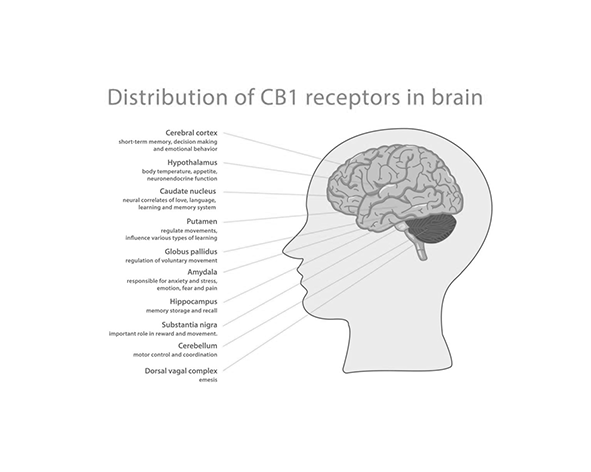
Con la identificación de los receptores CB1 en regiones clave del cerebro, especialmente en el hipotálamo y el sistema mesolímbico, se consolidó la hipótesis de que el SEC desempeña un papel central en la regulación del apetito. Estudios posteriores demostraron que la activación de CB1 estimula la ingesta, mientras que su bloqueo reduce significativamente el consumo de alimentos, tanto en modelos animales como en humanos. (Di Marzo et al., 2001; Cota et al., 2003)
Este conocimiento dio lugar al desarrollo de antagonistas del receptor CB1 como estrategia para modular el peso corporal, aunque su uso clínico se vio limitado por efectos adversos a nivel central, lo que puso de manifiesto la complejidad del sistema y su implicación en múltiples funciones neuropsicológicas. (Christensen et al., 2007)
En conjunto, la evolución del conocimiento sobre la regulación del apetito refleja un cambio desde modelos localizados hacia una comprensión sistémica, donde el sistema endocannabinoide se integra como un modulador clave dentro de una red neuroendocrina altamente distribuida. (Pagotto et al., 2006)
Organización y distribución del sistema endocannabinoide
El sistema endocannabinoide (SEC) se distribuye de forma amplia y estratégica en estructuras cerebrales y periféricas implicadas en la regulación del apetito, actuando como un modulador fino de la integración entre señales energéticas y conductuales. Su organización permite influir tanto en los circuitos homeostáticos del hambre como en los componentes hedónicos asociados a la ingesta. (Pagotto et al., 2006; Di Marzo & Matias, 2005)
A nivel central, el hipotálamo constituye el principal nodo de integración del apetito, donde el SEC interactúa con poblaciones neuronales clave localizadas en el núcleo arcuato. En esta región coexisten neuronas orexigénicas (NPY/AgRP), que promueven la ingesta, y neuronas anorexigénicas (POMC/CART), que inducen saciedad. La señalización endocannabinoide modula la actividad de ambos sistemas, ajustando el equilibrio entre hambre y saciedad en función del estado energético. (Cone, 2005; Horvath, 2005)
Además del núcleo arcuato, los receptores CB1 se expresan en otras regiones hipotalámicas como el núcleo paraventricular y el hipotálamo lateral, que participan en la regulación neuroendocrina y en la coordinación de respuestas conductuales relacionadas con la alimentación. Esta distribución sugiere que el SEC no actúa sobre un único punto de control, sino sobre una red integrada de núcleos funcionales. (Kirkham, 2009)
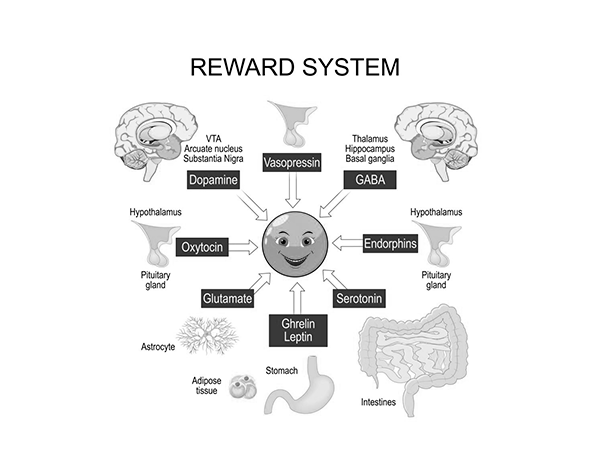
Más allá del hipotálamo, el SEC está presente en circuitos de recompensa como el sistema mesolímbico, incluyendo el área tegmental ventral y el núcleo accumbens. En estas regiones, la activación de CB1 modula la liberación de dopamina, influyendo en la motivación por consumir alimentos, especialmente aquellos con alta palatabilidad. Este componente hedónico resulta clave para entender conductas alimentarias no estrictamente ligadas a necesidades energéticas. (Solinas et al., 2008)
A nivel periférico, el SEC se expresa en órganos metabólicamente activos como el tejido adiposo, el hígado, el páncreas y el tracto gastrointestinal. En el intestino, por ejemplo, participa en la regulación de la motilidad y en la señalización entre el sistema digestivo y el cerebro, mientras que en el tejido adiposo influye en el almacenamiento de energía y en la secreción de adipocinas. (Osei-Hyiaman et al., 2005)
La síntesis y degradación de endocannabinoides como la anandamida (AEA) y el 2-araquidonoilglicerol (2-AG) se produce de forma local y dinámica, lo que permite una regulación espacial y temporal altamente precisa. Este carácter “a demanda” del SEC es clave para su papel como modulador fisiológico, evitando una activación sostenida que podría alterar el equilibrio energético. (Piomelli, 2003)
En conjunto, la organización del SEC en la regulación del apetito refleja una arquitectura distribuida y jerárquica, donde señales metabólicas, neuronales y conductuales convergen en un sistema capaz de ajustar de forma continua la conducta alimentaria. (Pagotto et al., 2006)
Mecanismos de interacción con el sistema endocannabinoide
El sistema endocannabinoide (SEC) modula la regulación del apetito mediante una combinación de mecanismos sinápticos, neuroendocrinos y metabólicos que afectan tanto a los circuitos homeostáticos como a los hedónicos de la alimentación. Su acción no es directa sobre “el hambre” como concepto aislado, sino sobre la excitabilidad neuronal y la liberación de neurotransmisores en redes específicas implicadas en la conducta alimentaria. (Di Marzo & Matias, 2005; Pagotto et al., 2006)
A nivel sináptico, los endocannabinoides como la anandamida (AEA) y el 2-AG actúan como mensajeros retrógrados, liberándose desde la neurona postsináptica para unirse a receptores CB1 en terminales presinápticos. Esta activación reduce la liberación de neurotransmisores excitatorios o inhibitorios, modulando así la actividad de circuitos neuronales implicados en el control del apetito. (Piomelli, 2003)
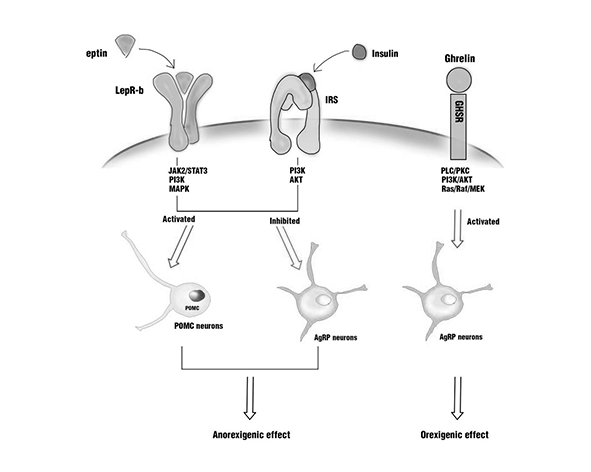
En el hipotálamo, este mecanismo permite al SEC ajustar el equilibrio entre señales orexigénicas y anorexigénicas. La activación de CB1 favorece la actividad de neuronas NPY/AgRP (que estimulan la ingesta) y reduce la señalización de neuronas POMC/CART (asociadas a la saciedad), inclinando el sistema hacia un estado de mayor apetito. (Cota et al., 2003; Horvath, 2005)
El SEC también interactúa de forma estrecha con señales hormonales periféricas. La leptina, por ejemplo, reduce los niveles de endocannabinoides en el hipotálamo, mientras que en estados de déficit energético o resistencia a la leptina se observa un aumento de la señalización endocannabinoide, lo que puede contribuir a un incremento del apetito. (Di Marzo et al., 2001)
Por su parte, la grelina, considerada una de las principales hormonas orexigénicas, potencia la actividad del SEC, facilitando la activación de circuitos que promueven la ingesta. Esta interacción sugiere que el SEC actúa como un amplificador de señales que indican necesidad energética. (Kola et al., 2008)
En paralelo, en el sistema mesolímbico, la activación de CB1 modula la liberación de dopamina, reforzando la motivación por consumir alimentos, especialmente aquellos ricos en grasa y azúcar. Este componente hedónico explica por qué el SEC no solo influye en la cantidad de alimento ingerido, sino también en su valor percibido y en la conducta de búsqueda. (Solinas et al., 2008; Kirkham, 2009)
A nivel periférico, el SEC participa en la regulación del metabolismo energético mediante efectos sobre el hígado, el tejido adiposo y el sistema gastrointestinal. La activación de CB1 en estos tejidos se ha asociado con procesos como la lipogénesis, la modulación de la sensibilidad a la insulina y la señalización digestiva, contribuyendo a un sistema integrado de regulación energética. (Osei-Hyiaman et al., 2005)
Un aspecto clave de estos mecanismos es su carácter dinámico y dependiente del contexto fisiológico. La señalización endocannabinoide aumenta en situaciones de ayuno y disminuye tras la ingesta, lo que sugiere un papel adaptativo en la regulación del balance energético. Sin embargo, alteraciones en este sistema pueden contribuir a desequilibrios metabólicos, reflejando su implicación en procesos complejos más allá del control inmediato del apetito. (Pagotto et al., 2006)
En conjunto, los mecanismos de interacción del SEC en la regulación del apetito reflejan un sistema de control distribuido que integra señales neuronales, hormonales y metabólicas, ajustando de forma continua la conducta alimentaria en función de las necesidades del organismo y del entorno. (Di Marzo & Matias, 2005)
Funciones fisiológicas
La regulación del apetito a través del sistema endocannabinoide (SEC) no se limita a la inducción del hambre, sino que forma parte de un sistema fisiológico más amplio orientado a mantener el equilibrio energético del organismo. En este contexto, el SEC participa en la coordinación entre ingesta, almacenamiento y utilización de energía, integrando señales internas con estímulos ambientales. (Pagotto et al., 2006; Di Marzo & Matias, 2005)
Una de sus funciones principales es la facilitación de la ingesta alimentaria en condiciones de déficit energético. Durante el ayuno, los niveles de endocannabinoides como la anandamida (AEA) y el 2-AG aumentan en regiones clave del cerebro, favoreciendo la activación de circuitos orexigénicos y promoviendo la conducta de búsqueda de alimento. (Kirkham et al., 2002)
El SEC también interviene en la modulación de la saciedad, no como un sistema primario de inhibición de la ingesta, sino como un modulador que ajusta la intensidad de las señales de saciedad en función del contexto metabólico. Esto permite que el organismo mantenga la ingesta incluso cuando las señales de saciedad comienzan a activarse, especialmente en presencia de alimentos altamente palatables. (Harrold et al., 2002)
En el ámbito hedónico, el SEC desempeña un papel clave en la valoración del alimento, aumentando la percepción de recompensa asociada a su consumo. A través de su acción en el sistema mesolímbico, potencia la liberación de dopamina y refuerza la motivación por consumir alimentos energéticamente densos, lo que contribuye a la preferencia por determinados tipos de dieta. (Solinas et al., 2008)
A nivel periférico, el SEC participa en la regulación del metabolismo energético mediante efectos sobre tejidos como el hígado y el tejido adiposo. Su activación se ha relacionado con procesos de almacenamiento energético, incluyendo la lipogénesis, así como con la modulación de la sensibilidad a la insulina, lo que sitúa al SEC en el centro de la regulación metabólica. (Osei-Hyiaman et al., 2005)
Otra función relevante es su papel en la señalización entre el tracto gastrointestinal y el sistema nervioso central. El SEC modula la motilidad intestinal y la liberación de señales aferentes que informan al cerebro sobre el estado digestivo, contribuyendo a la integración de la fase pre-ingestiva y post-ingestiva de la alimentación. (DiPatrizio, 2016)
Además, el SEC participa en la adaptación del comportamiento alimentario frente a cambios en el entorno, como el acceso a alimentos o el estrés. En este sentido, actúa como un sistema de ajuste que permite al organismo modificar su conducta en función de variables externas, reforzando la flexibilidad del sistema de regulación del apetito. (Kirkham, 2009)
En conjunto, las funciones fisiológicas del SEC en la regulación del apetito reflejan un papel integrador que va más allá del simple control del hambre, abarcando procesos que incluyen la motivación, el metabolismo y la adaptación conductual, dentro de un marco dinámico de homeostasis energética. (Pagotto et al., 2006)
Implicaciones en investigación
El estudio del sistema endocannabinoide (SEC) en la regulación del apetito ha generado un interés significativo en el ámbito de la investigación biomédica, especialmente por su papel integrador entre metabolismo, conducta y señalización neuroendocrina. Este interés se centra tanto en comprender los mecanismos fisiológicos básicos como en explorar posibles aplicaciones en el contexto de alteraciones del equilibrio energético. (Pagotto et al., 2006; Di Marzo & Matias, 2005)
Uno de los principales focos de investigación ha sido la relación entre la hiperactividad del sistema endocannabinoide y estados de exceso de ingesta o desequilibrios metabólicos. Diversos estudios han observado niveles elevados de endocannabinoides en modelos de obesidad, lo que sugiere una posible desregulación del sistema en contextos de balance energético positivo. (Matias & Di Marzo, 2007)
En esta línea, el desarrollo de antagonistas del receptor CB1 fue inicialmente planteado como una estrategia para modular la ingesta y el peso corporal. Compuestos como el rimonabant mostraron efectos en la reducción del apetito y del peso en ensayos clínicos, lo que validó el papel funcional del SEC en humanos. Sin embargo, su retirada del mercado debido a efectos adversos a nivel neuropsiquiátrico evidenció la complejidad del sistema y su implicación en múltiples funciones cerebrales más allá del metabolismo. (Christensen et al., 2007)
Actualmente, la investigación se orienta hacia enfoques más selectivos, como la modulación periférica del SEC o la inhibición de enzimas implicadas en la degradación de endocannabinoides, con el objetivo de evitar efectos centrales no deseados. Estas estrategias buscan intervenir en el sistema de forma más precisa, respetando su papel fisiológico en la homeostasis. (Silvestri & Di Marzo, 2013)
Otro campo emergente es el estudio de la interacción entre el SEC y otros sistemas regulatorios, como el eje intestino-cerebro y la microbiota intestinal. La evidencia sugiere que estas interacciones podrían desempeñar un papel relevante en la regulación del apetito y del metabolismo energético, abriendo nuevas líneas de investigación en fisiología integrativa. (DiPatrizio, 2016)
Además, se investiga el papel del SEC en contextos clínicos caracterizados por alteraciones del apetito, como la caquexia o determinados trastornos metabólicos. En estos escenarios, la modulación del sistema se plantea desde una perspectiva de comprensión fisiológica y potencial manejo del balance energético, siempre dentro de un marco de investigación en desarrollo. (Kirkham, 2009)
En conjunto, las implicaciones en investigación del SEC en la regulación del apetito reflejan un campo en evolución, donde el objetivo principal no es simplificar su función, sino entender su papel dentro de redes complejas que integran señales neuronales, hormonales y metabólicas. Este enfoque resulta clave para interpretar su relevancia en fisiología y su potencial en futuras líneas de estudio. (Pagotto et al., 2006)
Véase también
- Sistema endocannabinoide
- Receptor CB1
- Anandamida (AEA)
- 2-araquidonoilglicerol (2-AG)
- Metabolismo energético
Referencias
- Anand BK, Brobeck JR. (1951). Localization of a “feeding center” in the hypothalamus of the rat. Proceedings of the Society for Experimental Biology and Medicine. - Berthoud HR. (2002). Multiple neural systems controlling food intake and body weight. Neuroscience & Biobehavioral Reviews. - Berthoud HR. (2011). Metabolic and hedonic drives in the neural control of appetite. American Journal of Physiology. - Christensen R, Kristensen PK, Bartels EM, Bliddal H, Astrup A. (2007). Efficacy and safety of the weight-loss drug rimonabant: a meta-analysis of randomised trials. The Lancet. - Cone RD. (2005). Anatomy and regulation of the central melanocortin system. Nature Neuroscience. - Cota D, Marsicano G, Tschöp M, et al. (2003). The endogenous cannabinoid system affects energy balance via central orexigenic drive. Journal of Clinical Investigation. - Di Marzo V, Goparaju SK, Wang L, et al. (2001). Leptin-regulated endocannabinoids are involved in maintaining food intake. Nature. - Di Marzo V, Matias I. (2005). Endocannabinoid control of food intake and energy balance. Nature Neuroscience. - DiPatrizio NV. (2016). Endocannabinoids in the gut. Cannabis and Cannabinoid Research. - Grill HJ, Hayes MR. (2012). Hindbrain neurons as an essential hub in the neuroanatomically distributed control of energy balance. Cell Metabolism. - Horvath TL. (2005). The hardship of obesity: a soft-wired hypothalamus. Nature Neuroscience. - Kirkham TC. (2009). Cannabinoids and appetite: food craving and food pleasure. International Review of Psychiatry. - Kirkham TC, Williams CM, Fezza F, Di Marzo V. (2002). Endocannabinoid levels in rat limbic forebrain and hypothalamus in relation to fasting, feeding and satiety. British Journal of Pharmacology. - Kojima M, Hosoda H, Date Y, et al. (1999). Ghrelin is a growth-hormone-releasing acylated peptide from stomach. Nature. - Kola B, Farkas I, Christ-Crain M, et al. (2008). The orexigenic effect of ghrelin is mediated through central activation of the endogenous cannabinoid system. PLoS One. - Matias I, Di Marzo V. (2007). Endocannabinoids and the control of energy balance. Trends in Endocrinology & Metabolism. - Morton GJ, Cummings DE, Baskin DG, Barsh GS, Schwartz MW. (2006). Central nervous system control of food intake and body weight. Nature. - Osei-Hyiaman D, DePetrillo M, Pacher P, et al. (2005). Endocannabinoid activation at hepatic CB1 receptors stimulates fatty acid synthesis. Journal of Clinical Investigation. - Pagotto U, Marsicano G, Cota D, Lutz B, Pasquali R. (2006). The emerging role of the endocannabinoid system in endocrine regulation and energy balance. Endocrine Reviews. - Piomelli D. (2003). The molecular logic of endocannabinoid signalling. Nature Reviews Neuroscience. - Schwartz MW, Woods SC, Porte D, Seeley RJ, Baskin DG. (2000). Central nervous system control of food intake. Nature. - Silvestri C, Di Marzo V. (2013). The endocannabinoid system in energy homeostasis and the regulation of adiposity. Cell Metabolism. - Solinas M, Goldberg SR, Piomelli D. (2008). The endocannabinoid system in brain reward processes. British Journal of Pharmacology. - Zhang Y, Proenca R, Maffei M, et al. (1994). Positional cloning of the mouse obese gene and its human homologue. Nature.