Introducción
El metabolismo energético hace referencia al conjunto de procesos mediante los cuales el organismo capta, transforma, almacena y utiliza energía a partir de nutrientes. Este sistema no es una estructura anatómica única, sino una red funcional distribuida que integra órganos clave como el hígado, el músculo esquelético, el tejido adiposo, el páncreas y el sistema nervioso central.
A nivel fisiológico, el metabolismo energético se organiza en torno a dos grandes estados: el anabólico (almacenamiento de energía, predominante tras la ingesta) y el catabólico (movilización de reservas, predominante en ayuno o demanda energética elevada). La transición entre ambos estados está finamente regulada por señales hormonales —principalmente insulina, glucagón, leptina y grelina— que permiten ajustar el uso de glucosa, lípidos y aminoácidos según las necesidades del organismo. (Saltiel & Kahn, 2001; Rui, 2014)
En este contexto, el sistema endocannabinoide (SEC) actúa como un modulador metabólico de alto nivel, participando en la regulación del apetito, la eficiencia en el almacenamiento energético y el gasto metabólico. A diferencia de otros sistemas regulatorios más específicos, el SEC conecta señales periféricas y centrales, influyendo tanto en el comportamiento alimentario como en procesos celulares como la lipogénesis, la oxidación de ácidos grasos o la sensibilidad a la insulina. (Di Marzo et al., 2001; Silvestri & Di Marzo, 2013)
La relevancia fisiológica del metabolismo energético radica en su papel en la homeostasis global del organismo. Alteraciones en su regulación no solo afectan al balance energético, sino que están asociadas a múltiples estados estudiados en investigación biomédica, como la disfunción metabólica, la resistencia a la insulina o los cambios en la composición corporal. En este sentido, comprender la interacción entre sistemas clásicos (endocrino, nervioso) y moduladores emergentes como el SEC resulta clave para interpretar la complejidad del metabolismo humano en condiciones normales y en contextos de investigación. (Kahn et al., 2006; Hill et al., 2010)
Historia del descubrimiento
El estudio del metabolismo energético se desarrolló progresivamente a lo largo de los siglos XIX y XX, en paralelo al avance de la fisiología y la bioquímica. Uno de los primeros hitos fundamentales fue el trabajo de Claude Bernard, quien en el siglo XIX describió el papel del hígado en la regulación de la glucosa y formuló el concepto de “medio interno”, estableciendo las bases de lo que más tarde se conocería como homeostasis. Este enfoque supuso un cambio de paradigma al entender que el organismo mantiene condiciones internas estables independientemente del entorno. (Bernard, 1865)
A comienzos del siglo XX, el descubrimiento de la insulina por Frederick Banting y Charles Best marcó un punto de inflexión en la comprensión del control metabólico. La insulina fue identificada como una hormona clave en la regulación de la glucosa en sangre y el almacenamiento energético, consolidando el papel del sistema endocrino en el metabolismo. Este hallazgo permitió establecer las bases fisiológicas del estado postprandial y del almacenamiento de energía en forma de glucógeno y lípidos. (Bliss, 1982)
Posteriormente, durante la segunda mitad del siglo XX, se identificaron otras hormonas fundamentales como el glucagón, la leptina y la grelina, que ampliaron la visión del metabolismo energético como un sistema dinámico regulado por múltiples señales. En particular, el descubrimiento de la leptina en 1994 por Jeffrey Friedman permitió comprender los mecanismos de regulación del apetito y el peso corporal desde el tejido adiposo hacia el sistema nervioso central, introduciendo el concepto de señalización energética periférica. (Zhang et al., 1994)
El papel del sistema nervioso central, especialmente del hipotálamo, se consolidó como centro integrador de estas señales metabólicas, coordinando la ingesta y el gasto energético. En este contexto, a finales del siglo XX y principios del XXI, emergió el sistema endocannabinoide como un nuevo modulador del metabolismo energético, inicialmente a partir de estudios sobre el apetito y los efectos del cannabis en la ingesta alimentaria. (Di Marzo et al., 1998)
El descubrimiento de endocannabinoides como la anandamida y el 2-AG, junto con sus receptores CB1 y CB2, permitió integrar este sistema dentro del marco de la regulación energética. Se observó que la activación del receptor CB1 estaba asociada con un aumento del apetito y una mayor eficiencia en el almacenamiento de energía, lo que llevó al desarrollo de antagonistas de CB1 como estrategia de investigación en el control del peso corporal. (Pagotto et al., 2006)
En conjunto, la historia del metabolismo energético refleja una transición desde una visión centrada en órganos aislados hacia una comprensión integrada de redes fisiológicas complejas, en las que el sistema endocrino, el sistema nervioso y el sistema endocannabinoide interactúan de forma coordinada para mantener el equilibrio energético del organismo. (Silvestri & Di Marzo, 2013)
Organización del sistema y distribución del SEC
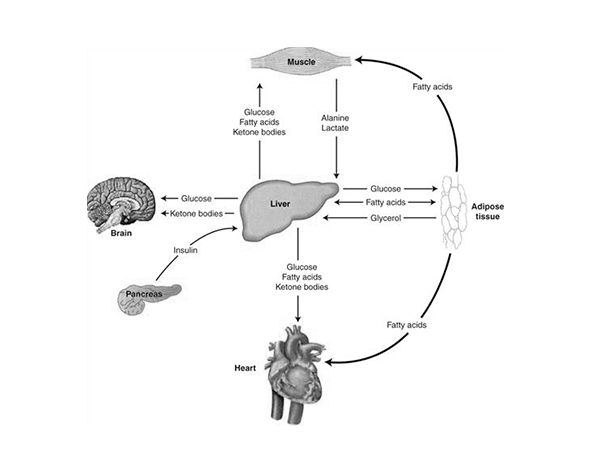
El metabolismo energético no depende de un único órgano, sino de una red coordinada de tejidos con funciones específicas que interactúan entre sí para mantener el equilibrio entre ingesta, almacenamiento y gasto energético. Entre los principales órganos implicados destacan el hígado, el músculo esquelético, el tejido adiposo, el páncreas endocrino y el sistema nervioso central, especialmente el hipotálamo.
El hígado actúa como centro metabólico clave, regulando la glucosa sanguínea mediante procesos como la gluconeogénesis y la glucogenólisis, además de participar en la síntesis y redistribución de lípidos. El músculo esquelético, por su parte, representa uno de los mayores consumidores de energía, utilizando glucosa y ácidos grasos según el estado metabólico. El tejido adiposo funciona como reservorio energético, almacenando triglicéridos y liberándolos en forma de ácidos grasos cuando el organismo lo requiere, mientras que el páncreas regula estos flujos mediante la secreción de insulina y glucagón. (Kahn et al., 2006; Rui, 2014)
En el sistema nervioso central, el hipotálamo actúa como núcleo integrador de señales metabólicas periféricas. Recibe información hormonal (leptina, insulina, grelina) y nutrientes circulantes, y coordina respuestas que afectan tanto al comportamiento alimentario como al gasto energético. Esta integración permite adaptar el metabolismo a diferentes estados fisiológicos como el ayuno, la saciedad o el ejercicio. (Schwartz et al., 2000)
Dentro de esta red, el sistema endocannabinoide (SEC) presenta una distribución amplia y estratégica. El receptor CB1 se expresa de forma predominante en el sistema nervioso central, especialmente en el hipotálamo, donde modula circuitos relacionados con el apetito y la motivación alimentaria. Sin embargo, también se encuentra en tejidos periféricos clave para el metabolismo energético, como el hígado, el tejido adiposo, el músculo esquelético y el tracto gastrointestinal. (Pagotto et al., 2006; Silvestri & Di Marzo, 2013)
El receptor CB2, aunque clásicamente asociado al sistema inmunológico, también se ha identificado en tejidos metabólicos, donde podría desempeñar un papel modulador en procesos inflamatorios asociados al metabolismo. Por su parte, los endocannabinoides —principalmente anandamida (AEA) y 2-araquidonoilglicerol (2-AG)— se sintetizan localmente en función de la demanda y actúan como señales lipídicas de corta duración, permitiendo una regulación fina y contextual del sistema. (Di Marzo et al., 2001)
A nivel funcional, el SEC actúa como un sistema de ajuste que conecta señales energéticas periféricas con respuestas centrales y celulares. Su activación en el sistema nervioso favorece la ingesta, mientras que en tejidos periféricos puede influir en la lipogénesis, la sensibilidad a la insulina y el uso de sustratos energéticos. Esta doble acción central-periférica convierte al SEC en un modulador clave de la eficiencia metabólica del organismo. (Osei-Hyiaman et al., 2005)
En conjunto, la organización del metabolismo energético y la distribución del SEC reflejan un sistema altamente integrado, donde múltiples niveles de regulación —desde el molecular hasta el conductual— interactúan para mantener la homeostasis energética en condiciones cambiantes. (Silvestri & Di Marzo, 2013)
Mecanismos de interacción con el SEC
El sistema endocannabinoide (SEC) modula el metabolismo energético a través de mecanismos que operan tanto a nivel central (sistema nervioso) como periférico (órganos metabólicos), integrando señales nutricionales, hormonales y celulares para ajustar la ingesta, el almacenamiento y el gasto energético.
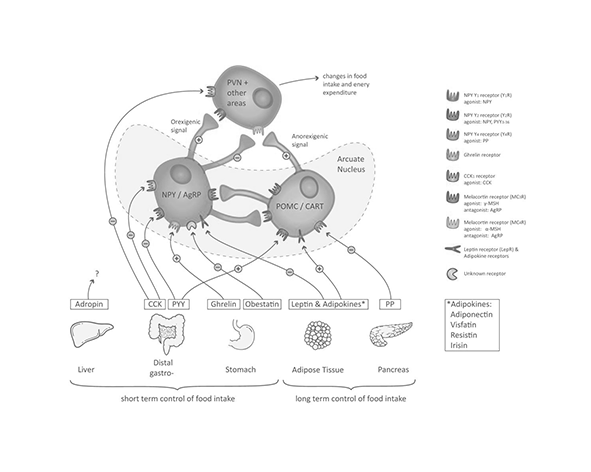
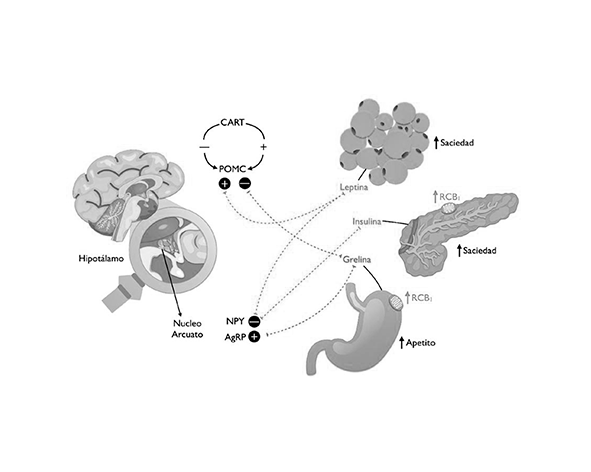
A nivel central, el SEC actúa principalmente en el hipotálamo, donde el receptor CB1 regula circuitos neuronales implicados en el apetito y la motivación alimentaria. La activación de CB1 en neuronas orexigénicas (como las que expresan neuropéptido Y y AgRP) favorece la ingesta, mientras que modula negativamente señales anorexigénicas asociadas a la saciedad. Este efecto se encuentra estrechamente relacionado con la interacción del SEC con hormonas como la leptina y la grelina: la leptina tiende a reducir la señalización endocannabinoide, mientras que la grelina puede potenciarla, generando un equilibrio dinámico entre hambre y saciedad. (Di Marzo et al., 2001; Cota et al., 2003)
Además del control del apetito, el SEC influye en los circuitos de recompensa del sistema nervioso, especialmente en áreas como el núcleo accumbens. Esto implica que su activación no solo afecta cuánto comemos, sino también la preferencia por alimentos energéticamente densos, integrando aspectos hedónicos con necesidades metabólicas. (Mahler et al., 2007)
A nivel periférico, los mecanismos del SEC están directamente implicados en la regulación del almacenamiento y uso de energía. En el hígado, la activación del receptor CB1 se ha asociado con un aumento de la lipogénesis de novo, favoreciendo la síntesis de ácidos grasos y triglicéridos. En el tejido adiposo, el SEC modula tanto la acumulación de lípidos como la liberación de ácidos grasos, influyendo en el balance entre almacenamiento y movilización energética. (Osei-Hyiaman et al., 2005)
En el músculo esquelético, el SEC puede afectar la captación de glucosa y la oxidación de sustratos energéticos, interfiriendo potencialmente con la sensibilidad a la insulina. Este efecto se relaciona con la capacidad del sistema endocannabinoide para modular rutas intracelulares clave, como la señalización de AMPK (proteína quinasa activada por AMP), que actúa como sensor energético celular. (Liu et al., 2005)
Otro aspecto relevante es la participación del SEC en la regulación de la eficiencia energética. Se ha observado que su activación puede favorecer un estado metabólico orientado al almacenamiento, aumentando la eficiencia con la que el organismo convierte el exceso energético en reservas. Este mecanismo, que pudo tener ventajas evolutivas en contextos de escasez, adquiere una nueva dimensión en entornos de disponibilidad energética constante. (Pagotto et al., 2006)
A nivel molecular, los endocannabinoides como la anandamida (AEA) y el 2-AG se sintetizan a partir de lípidos de membrana en respuesta a señales específicas, actuando de forma local y transitoria. Su degradación por enzimas como FAAH y MAGL permite un control preciso de la señalización, evitando una activación sostenida del sistema. Este carácter dinámico convierte al SEC en un modulador fino más que en un sistema de activación sostenida. (Di Marzo et al., 1998)
En conjunto, los mecanismos de interacción del SEC con el metabolismo energético reflejan un sistema complejo que conecta comportamiento, fisiología y bioquímica. Su capacidad para actuar simultáneamente sobre la ingesta, el almacenamiento y el gasto energético lo posiciona como un regulador clave de la homeostasis energética en múltiples niveles. (Silvestri & Di Marzo, 2013)
Funciones fisiológicas
El metabolismo energético cumple una función central en la fisiología humana al garantizar el suministro continuo de energía necesario para el mantenimiento de funciones vitales, la actividad física y la adaptación a cambios en el entorno nutricional. Este sistema no solo regula la disponibilidad de energía, sino también su distribución eficiente entre tejidos, ajustándose dinámicamente a estados como el ayuno, la ingesta o el ejercicio.
Una de sus funciones principales es la regulación del balance energético, es decir, el equilibrio entre la energía ingerida y la energía gastada. Este balance determina en gran medida el mantenimiento del peso corporal y la composición corporal. El sistema integra señales periféricas (nutrientes, hormonas) y centrales (circuitos neuronales) para ajustar tanto la ingesta como el gasto energético, manteniendo la estabilidad del medio interno. (Hill et al., 2012)
En este contexto, el sistema endocannabinoide (SEC) desempeña un papel relevante al modular la ingesta alimentaria y la eficiencia metabólica. La activación del receptor CB1 en el sistema nervioso central favorece la ingesta, especialmente de alimentos energéticamente densos, mientras que su actividad en tejidos periféricos contribuye a optimizar el almacenamiento energético. Esta doble acción permite al organismo adaptarse a situaciones de disponibilidad energética variable. (Di Marzo & Matias, 2005)
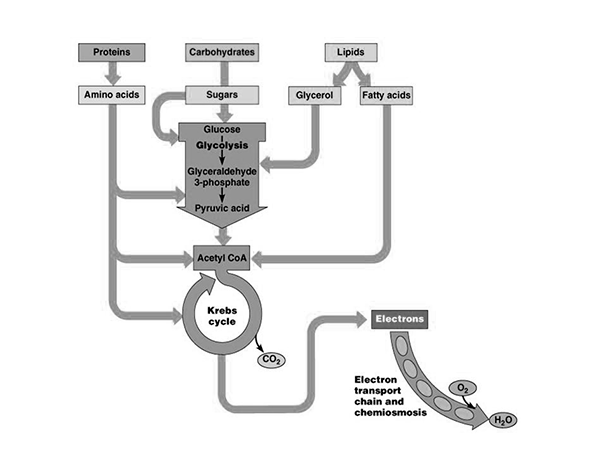
Otra función clave es la gestión de sustratos energéticos, que implica la selección y utilización de diferentes fuentes de energía como glucosa, ácidos grasos y aminoácidos. En condiciones de abundancia, predomina el uso y almacenamiento de glucosa, mientras que en ayuno se favorece la movilización de lípidos y la producción de cuerpos cetónicos. El SEC puede influir en esta flexibilidad metabólica modulando rutas como la lipogénesis y la oxidación de grasas. (Osei-Hyiaman et al., 2005)
El metabolismo energético también participa en la termogénesis y el gasto energético basal, procesos que determinan cuánta energía consume el organismo en reposo y en respuesta a estímulos como el frío o la ingesta. Se ha observado que la señalización endocannabinoide puede influir en estos procesos, favoreciendo estados de mayor eficiencia energética, lo que implica un menor gasto relativo en determinadas condiciones. (Pagotto et al., 2006)
Otra función relevante es la integración del comportamiento alimentario con necesidades fisiológicas. El metabolismo energético no opera de forma aislada, sino que está estrechamente vinculado a circuitos de recompensa y motivación en el cerebro. El SEC participa en esta integración, modulando tanto el hambre homeostática (necesidad energética) como el hambre hedónica (placer asociado a la comida), lo que añade una dimensión conductual al control metabólico. (Mahler et al., 2007)
Además, el metabolismo energético está implicado en la adaptación a cambios ambientales y fisiológicos, como el ejercicio físico, el estrés o variaciones en la disponibilidad de nutrientes. Esta capacidad adaptativa depende de la coordinación entre múltiples sistemas, incluido el SEC, que actúa como modulador flexible ajustando la respuesta metabólica a corto y medio plazo. (Silvestri & Di Marzo, 2013)
Finalmente, el metabolismo energético contribuye a la homeostasis sistémica, conectando con otros sistemas fisiológicos como el sistema endocrino, el sistema nervioso y el sistema inmunológico. Esta interconexión permite que cambios en el estado energético tengan repercusiones amplias en el organismo, reforzando la idea de que el metabolismo no es un proceso aislado, sino un eje central de la fisiología humana. (Kahn et al., 2006)
Implicaciones en investigación
El metabolismo energético constituye uno de los ejes centrales de la investigación biomédica contemporánea, debido a su implicación en múltiples procesos fisiológicos y su relación con estados de disfunción metabólica ampliamente estudiados. La comprensión de sus mecanismos ha evolucionado desde modelos simples centrados en órganos individuales hacia una visión integrada que considera redes complejas de señalización hormonal, neuronal y molecular.
En este contexto, el sistema endocannabinoide (SEC) ha adquirido un papel relevante como modulador del metabolismo energético. La investigación ha mostrado que la hiperactivación del receptor CB1 se asocia con un aumento de la ingesta, una mayor eficiencia en el almacenamiento energético y alteraciones en la utilización de sustratos, lo que ha llevado a explorar este sistema como posible diana en estudios sobre regulación del peso corporal y metabolismo. (Pagotto et al., 2006; Silvestri & Di Marzo, 2013)
Uno de los desarrollos más significativos fue la investigación sobre antagonistas del receptor CB1, como Rimonabant, que mostraron efectos sobre la reducción del apetito y el peso corporal. Sin embargo, su retirada del mercado debido a efectos adversos a nivel psiquiátrico evidenció la complejidad del SEC y la dificultad de intervenir en este sistema sin afectar otros procesos fisiológicos, especialmente a nivel del sistema nervioso central. Este caso se ha convertido en un ejemplo paradigmático de los retos asociados a la modulación farmacológica del metabolismo energético. (Christensen et al., 2007)
Actualmente, la investigación se orienta hacia enfoques más selectivos, como la modulación periférica del SEC, con el objetivo de evitar efectos centrales no deseados. En este sentido, se estudian compuestos que actúan sobre CB1 en tejidos periféricos (hígado, tejido adiposo, músculo) o que modulan enzimas implicadas en la síntesis y degradación de endocannabinoides, como FAAH y MAGL. (Tam et al., 2010)
Además, el metabolismo energético se investiga en estrecha relación con otros sistemas fisiológicos, como el sistema endocrino y el sistema inmunológico, especialmente en el contexto de la inflamación metabólica. La interacción entre señalización energética y procesos inflamatorios representa un área activa de estudio, donde el SEC también podría desempeñar un papel modulador. (Hotamisligil, 2006)
Otro campo emergente es el estudio de la flexibilidad metabólica, es decir, la capacidad del organismo para adaptarse a diferentes fuentes de energía. Alteraciones en esta flexibilidad se han asociado a diversos estados estudiados en investigación, y el SEC podría influir en esta capacidad a través de su acción sobre rutas metabólicas clave y la regulación del balance energético. (Goodpaster & Sparks, 2017)
Asimismo, el análisis del metabolismo energético se ha ampliado hacia niveles más finos de organización, incluyendo la bioenergética celular, la función mitocondrial y la señalización intracelular. En estos niveles, el SEC interactúa con rutas como AMPK, mTOR y PPARs, integrando señales energéticas con respuestas celulares adaptativas. (Liu et al., 2005)
En conjunto, las implicaciones del metabolismo energético en investigación reflejan un campo dinámico y en expansión, donde la integración de sistemas y la comprensión de moduladores como el SEC son fundamentales para avanzar en el conocimiento de la fisiología humana y sus alteraciones. Este enfoque integrador permite abordar el metabolismo no solo como un conjunto de reacciones bioquímicas, sino como un sistema complejo que conecta múltiples niveles de organización biológica. (Silvestri & Di Marzo, 2013)
Véase también
Referencias
- Bernard, C. (1865). Introduction à l'étude de la médecine expérimentale. Baillière. - Bliss, M. (1982). The discovery of insulin. University of Chicago Press. - Cota, D., Marsicano, G., Tschöp, M., Grübler, Y., Flachskamm, C., Schubert, M., Auer, D., Yassouridis, A., Thöne-Reineke, C., Ortmann, S., Tomassoni, F., Cervino, C., Nisoli, E., Linthorst, A. C. E., Pasquali, R., Lutz, B., Stalla, G. K., & Pagotto, U. (2003). The endogenous cannabinoid system affects energy balance via central orexigenic drive. Nature, 423, 377–381. - Di Marzo, V., Goparaju, S. K., Wang, L., Liu, J., Bátkai, S., Járai, Z., Fezza, F., Miura, G. I., Palmiter, R. D., Sugiura, T., & Kunos, G. (2001). Leptin-regulated endocannabinoids are involved in maintaining food intake. Nature, 410, 822–825. - Di Marzo, V. (2008). Targeting the endocannabinoid system: To enhance or reduce? Nature Reviews Drug Discovery, 7, 438–455. - Di Marzo, V., & Matias, I. (2005). Endocannabinoid control of food intake and energy balance. Nature Neuroscience, 8, 585–589. - Goodpaster, B. H., & Sparks, L. M. (2017). Metabolic flexibility in health and disease. Cell Metabolism, 25, 1027–1036. - Hill, J. O., Wyatt, H. R., & Peters, J. C. (2012). Energy balance and obesity. Circulation, 126, 126–132. - Hotamisligil, G. S. (2006). Inflammation and metabolic disorders. Nature, 444, 860–867. - Kahn, S. E., Hull, R. L., & Utzschneider, K. M. (2006). Mechanisms linking obesity to insulin resistance and type 2 diabetes. Nature, 444, 840–846. - Liu, Y. L., Connoley, I. P., Wilson, C. A., & Stock, M. J. (2005). Effects of the cannabinoid CB1 receptor antagonist on energy balance and metabolism. International Journal of Obesity, 29, 182–187. - Mahler, S. V., Smith, K. S., & Berridge, K. C. (2007). Endocannabinoid hedonic hotspot for sensory pleasure. Neuropsychopharmacology, 32, 2267–2278. - Osei-Hyiaman, D., DePetrillo, M., Pacher, P., Liu, J., Radaeva, S., Bátkai, S., Harvey-White, J., Mackie, K., Offertáler, L., Wang, L., & Kunos, G. (2005). Endocannabinoid activation at hepatic CB1 receptors stimulates fatty acid synthesis. Journal of Clinical Investigation, 115, 1298–1305. - Pagotto, U., Marsicano, G., Cota, D., Lutz, B., & Pasquali, R. (2006). The emerging role of the endocannabinoid system in endocrine regulation and energy balance. Endocrine Reviews, 27, 73–100. - Rui, L. (2014). Energy metabolism in the liver. Comprehensive Physiology, 4, 177–197. - Schwartz, M. W., Woods, S. C., Porte, D., Seeley, R. J., & Baskin, D. G. (2000). Central nervous system control of food intake. Nature, 404, 661–671. - Silvestri, C., & Di Marzo, V. (2013). The endocannabinoid system in energy homeostasis and metabolic disorders. Cell Metabolism, 17, 475–490. Tam, J., Vemuri, V. K., Liu, J., Bátkai, S., Mukhopadhyay, B., Godlewski, G., Osei-Hyiaman, D., Ohnuma, S., Ambudkar, S. V., Pickel, J., Makriyannis, A., & Kunos, G. (2010). Peripheral CB1 blockade improves metabolic profile. Proceedings of the National Academy of Sciences, 107, 10821–10826. - Zhang, Y., Proenca, R., Maffei, M., Barone, M., Leopold, L., & Friedman, J. M. (1994). Positional cloning of the mouse obese gene and its human homologue. Nature, 372, 425–432.