Introducción
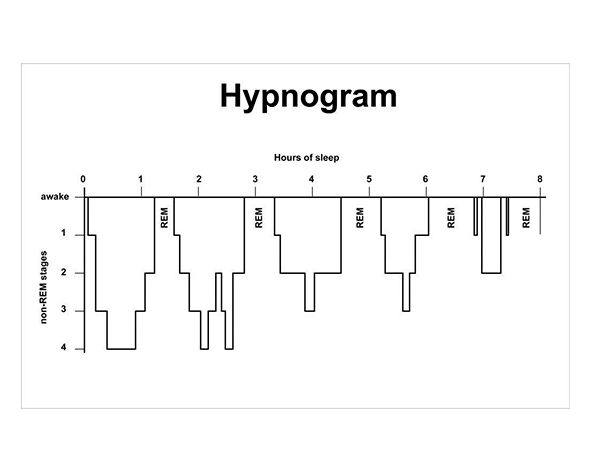
El sueño es un proceso fisiológico activo, altamente regulado y esencial para la homeostasis del organismo. Lejos de ser un estado pasivo de desconexión, implica una reorganización dinámica de la actividad neuronal, endocrina e inmunológica, con funciones críticas en la consolidación de la memoria, la regulación emocional, el metabolismo energético y la reparación tisular. Su arquitectura se organiza en ciclos que alternan fases de sueño no REM (NREM) y sueño REM, cada una con patrones electrofisiológicos y funciones biológicas diferenciadas. (Carskadon & Dement, 2011)
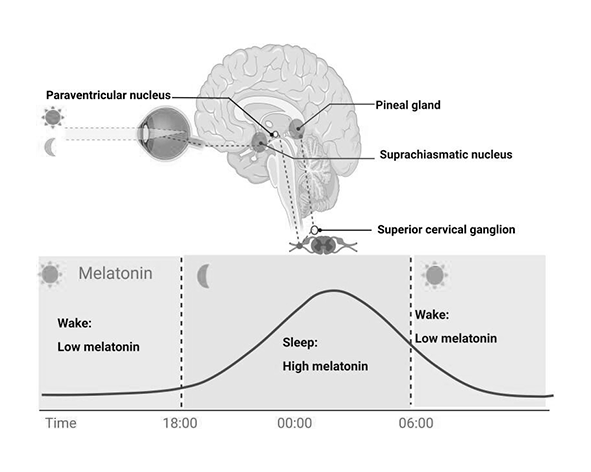
El control del sueño depende de la interacción entre dos sistemas principales: el proceso circadiano (regulado por el núcleo supraquiasmático del hipotálamo) y el proceso homeostático del sueño (que refleja la presión acumulada para dormir en función del tiempo de vigilia). Esta interacción permite ajustar los ritmos de sueño-vigilia a las condiciones ambientales, especialmente al ciclo luz-oscuridad. (Borbély et al., 2016)
En este contexto, el sistema endocannabinoide (SEC) emerge como un modulador relevante de la fisiología del sueño. Sus componentes —receptores CB1, endocannabinoides como la anandamida (AEA) y el 2-AG, y enzimas como FAAH— se expresan en regiones clave implicadas en la regulación del ciclo sueño-vigilia, incluyendo el hipotálamo, el tronco encefálico y estructuras límbicas. A través de estos mecanismos, el SEC participa en la modulación del inicio del sueño, la estabilidad de las fases y la transición entre estados de vigilia y sueño. (Pava et al., 2016; Murillo-Rodríguez, 2008)
Además, la señalización endocannabinoide interactúa con otros sistemas neuroquímicos implicados en el sueño, como los sistemas GABAérgico, glutamatérgico, serotoninérgico y orexinérgico. Esta interacción sugiere un papel integrador del SEC dentro de la red neurobiológica que regula los estados de conciencia. (Babson et al., 2017)
La investigación sobre sueño y sistema endocannabinoide ha crecido de forma significativa en las últimas décadas, impulsada tanto por estudios preclínicos como por el interés en comprender cómo los fitocannabinoides pueden influir en estos procesos. No obstante, la evidencia disponible muestra una elevada complejidad, con efectos dependientes de dosis, contexto fisiológico y tipo de compuesto, lo que requiere una interpretación cautelosa desde el punto de vista científico. (Suraev et al., 2020)
Historia del descubrimiento del sueño
El estudio científico del sueño comenzó a consolidarse a finales del siglo XIX y principios del XX, cuando se abandonó la idea de que dormir era simplemente una “desconexión pasiva” del cerebro. Investigaciones tempranas en neurofisiología ya sugerían que el sueño implicaba mecanismos activos del sistema nervioso central, especialmente a nivel del tronco encefálico y el diencéfalo. (Bremer, 1935)
Un punto de inflexión clave se produjo con los experimentos de lesiones en animales, que demostraron que ciertas regiones del encéfalo eran críticas para la regulación del estado de vigilia. Por ejemplo, estudios clásicos mostraron que la interrupción de conexiones en el tronco cerebral podía inducir estados persistentes de sueño, lo que llevó al desarrollo del concepto de “sistema reticular activador ascendente” como modulador de la vigilia. (Moruzzi & Magoun, 1949)
El avance más importante llegó en la década de 1950 con la introducción de la electroencefalografía (EEG) aplicada al estudio del sueño. Esto permitió identificar patrones eléctricos específicos asociados a diferentes fases, diferenciando el sueño en estados NREM (con actividad sincronizada y ondas lentas) y REM, caracterizado por actividad cerebral similar a la vigilia pero con atonía muscular. (Aserinsky & Kleitman, 1953)
A partir de estas observaciones, el sueño dejó de entenderse como un fenómeno uniforme y pasó a concebirse como un proceso cíclico y estructurado. Durante las décadas siguientes, se desarrollaron modelos que integraban tanto la regulación neural como los ritmos biológicos, destacando el modelo de dos procesos propuesto por Alexander Borbély, que describe la interacción entre la presión homeostática del sueño y el ritmo circadiano. (Borbély, 1982)
En paralelo, el estudio neuroquímico del sueño avanzó con la identificación de múltiples sistemas implicados en su regulación, incluyendo neurotransmisores como GABA, serotonina, noradrenalina y acetilcolina. Este enfoque permitió entender el sueño como el resultado de un equilibrio dinámico entre sistemas promotores de la vigilia y del sueño. (Saper et al., 2005)
El papel del sistema endocannabinoide en la fisiología del sueño comenzó a explorarse más tarde, a partir de finales del siglo XX, tras la identificación de los receptores cannabinoides (CB1 en 1990) y de los endocannabinoides como la anandamida. Estudios preclínicos mostraron que la administración de AEA podía inducir cambios en la latencia y la duración del sueño, lo que abrió una nueva línea de investigación centrada en la modulación endógena del ciclo sueño-vigilia. (Devane et al., 1992; Murillo-Rodríguez et al., 2001)
Desde entonces, el estudio del sueño ha evolucionado hacia un enfoque integrador que combina neurobiología, cronobiología y sistemas de señalización moduladores como el SEC, reflejando la complejidad de este proceso fisiológico fundamental.
Organización del sistema y distribución del SEC en la fisiología del sueño
La regulación del sueño se basa en una red distribuida de estructuras cerebrales que integran señales circadianas, homeostáticas y neuroquímicas. Entre los núcleos más relevantes se encuentra el núcleo supraquiasmático (NSQ) del hipotálamo, considerado el principal marcapasos circadiano, que sincroniza los ritmos de sueño-vigilia con el ciclo luz-oscuridad. Este núcleo modula la actividad de otras regiones hipotalámicas y del tronco encefálico implicadas en la inducción y mantenimiento del sueño. (Saper et al., 2005)
El hipotálamo lateral y el núcleo tuberomamilar participan en la promoción de la vigilia mediante sistemas excitadores, mientras que el área preóptica ventrolateral (VLPO) actúa como un centro promotor del sueño, principalmente a través de neurotransmisión GABAérgica e inhibición de los sistemas de activación. La interacción entre estos sistemas se ha descrito como un “interruptor flip-flop”, que permite transiciones rápidas y estables entre sueño y vigilia. (Saper et al., 2010)
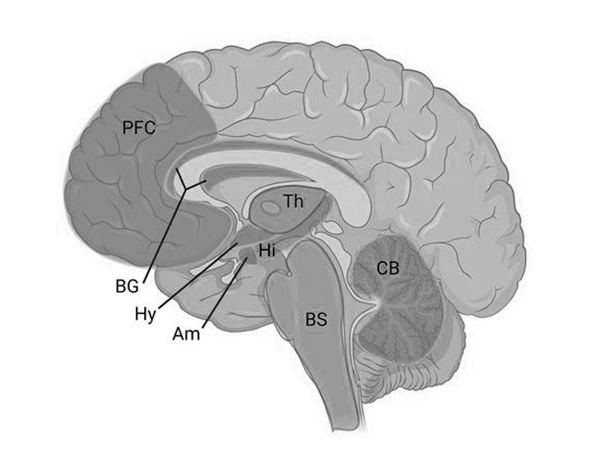
En este contexto, el sistema endocannabinoide se distribuye de forma estratégica en múltiples regiones clave para la regulación del sueño. Los receptores CB1 presentan una alta densidad en el sistema nervioso central, incluyendo el hipotálamo, el tronco encefálico, el hipocampo, la amígdala y la corteza cerebral, todas ellas implicadas en la arquitectura del sueño y en la modulación de estados de conciencia. (Herkenham et al., 1990)
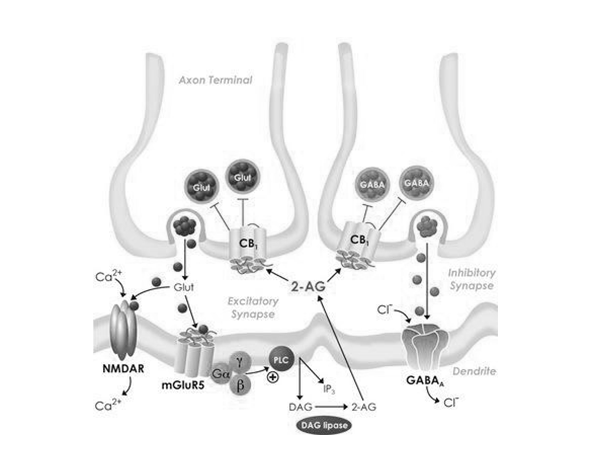
La anandamida (AEA) y el 2-araquidonoilglicerol (2-AG), principales endocannabinoides, se sintetizan de manera local “a demanda” en neuronas postsinápticas y actúan como mensajeros retrógrados, modulando la liberación de neurotransmisores en terminales presinápticas. Este mecanismo permite al SEC influir en la excitabilidad neuronal y en el equilibrio entre sistemas promotores de vigilia y sueño. (Castillo et al., 2012)
A nivel del hipotálamo, el SEC interactúa con sistemas clave en la regulación del sueño, como las neuronas orexinérgicas (implicadas en la vigilia) y las neuronas del VLPO. La activación de receptores CB1 puede modular la liberación de neurotransmisores excitadores e inhibidores, alterando así la dinámica del “interruptor” sueño-vigilia. (Pava et al., 2016)
Además, se ha observado que los niveles de endocannabinoides fluctúan a lo largo del ciclo circadiano. Por ejemplo, la concentración de anandamida presenta variaciones diurnas en regiones cerebrales relacionadas con el sueño, lo que sugiere un papel del SEC en la regulación temporal del ciclo sueño-vigilia. (Murillo-Rodríguez et al., 2006)
En el tronco encefálico, el SEC también participa en la modulación de los circuitos responsables del sueño REM, interfiriendo en sistemas colinérgicos y monoaminérgicos que controlan la transición entre fases del sueño. Esta distribución amplia y funcionalmente relevante refuerza la idea de que el sistema endocannabinoide actúa como un modulador global de la arquitectura del sueño.
Mecanismos de interacción del SEC en la fisiología del sueño
El sistema endocannabinoide (SEC) actúa como un modulador neuromodulador de amplio espectro en la regulación del ciclo sueño-vigilia, principalmente a través de mecanismos de señalización retrógrada que afectan la liberación de neurotransmisores en circuitos clave del sistema nervioso central. Este tipo de señalización permite ajustar de forma dinámica el equilibrio entre sistemas promotores de la vigilia y del sueño. (Castillo et al., 2012)
Uno de los mecanismos principales implica la liberación de endocannabinoides como la anandamida (AEA) desde la neurona postsináptica en respuesta a la actividad neuronal. Una vez liberados, estos compuestos activan receptores CB1 en terminales presinápticas, inhibiendo la liberación de neurotransmisores excitadores como el glutamato o modulando la liberación de neurotransmisores inhibidores como el GABA. Este control fino de la excitabilidad neuronal es esencial para la transición entre estados de vigilia y sueño. (Kano et al., 2009)
En el contexto del sueño, este mecanismo se traduce en una capacidad del SEC para favorecer la inducción del sueño al reducir la actividad de circuitos excitadores. Por ejemplo, la activación de CB1 en regiones hipotalámicas y del tronco encefálico puede disminuir la señalización de sistemas que promueven la vigilia, facilitando la entrada en fases NREM. (Murillo-Rodríguez, 2008)
El SEC también interactúa con sistemas neuroquímicos clave en la regulación del sueño. A nivel GABAérgico, puede potenciar la inhibición neuronal en regiones como el área preóptica ventrolateral (VLPO), favoreciendo la estabilidad del sueño. En paralelo, la modulación de la neurotransmisión glutamatérgica contribuye a la reducción de la excitación cortical durante el inicio del sueño. (Pava et al., 2016)
Otro eje relevante es la interacción con el sistema orexinérgico (hipocretinas), fundamental en la promoción de la vigilia. Los endocannabinoides pueden modular la actividad de neuronas orexinérgicas en el hipotálamo lateral, influyendo en la estabilidad del estado de vigilia y en la transición hacia el sueño. Esta interacción sugiere un papel del SEC en el “interruptor” funcional que regula los cambios entre estados de conciencia. (Huang et al., 2007)
En relación con el sueño REM, el SEC parece influir en los circuitos colinérgicos del tronco encefálico, que son esenciales para la generación de esta fase. Estudios experimentales han mostrado que la administración de endocannabinoides o agonistas cannabinoides puede alterar la duración y la latencia del sueño REM, aunque estos efectos son altamente dependientes de la dosis y del contexto fisiológico. (Murillo-Rodríguez et al., 2001)
Además, la enzima FAAH, responsable de la degradación de la anandamida, juega un papel clave en la regulación temporal de estos efectos. La inhibición de FAAH aumenta los niveles de AEA, lo que se ha asociado con un aumento de la presión del sueño y modificaciones en la arquitectura del mismo en modelos preclínicos. (Cravatt et al., 2001)
En conjunto, estos mecanismos posicionan al SEC como un sistema modulador que no actúa de forma aislada, sino integrándose en la red neurobiológica del sueño para ajustar la excitabilidad neuronal, la sincronización de circuitos y la transición entre fases del ciclo sueño-vigilia.
Funciones fisiológicas del sueño y papel del SEC
El sueño cumple funciones esenciales para el mantenimiento de la homeostasis del organismo, actuando sobre múltiples niveles fisiológicos que incluyen el sistema nervioso, el metabolismo, la función inmune y la regulación emocional. Estas funciones no son homogéneas, sino que se distribuyen entre las diferentes fases del sueño, especialmente entre el sueño NREM y REM. (Carskadon & Dement, 2011)
Una de las funciones más estudiadas del sueño es la consolidación de la memoria. Durante el sueño NREM, particularmente en las fases de ondas lentas, se produce una reactivación coordinada de circuitos neuronales implicados en el aprendizaje, facilitando la estabilización de la memoria declarativa. Por su parte, el sueño REM se asocia con la integración emocional y la memoria procedimental. (Diekelmann & Born, 2010)
En este contexto, el sistema endocannabinoide participa en la modulación de la plasticidad sináptica, un proceso clave para la consolidación de la memoria. La señalización endocannabinoide regula fenómenos como la depresión a largo plazo (LTD), influyendo en la eficiencia de las conexiones sinápticas durante el sueño. Este papel conecta directamente la actividad del SEC con procesos cognitivos dependientes del sueño. (Castillo et al., 2012)
Otra función fundamental del sueño es la regulación emocional. Durante el sueño REM, se produce una reorganización de la actividad en estructuras límbicas como la amígdala y la corteza prefrontal, lo que contribuye al procesamiento de experiencias emocionales. El SEC, ampliamente distribuido en estas regiones, modula la reactividad emocional y la respuesta al estrés, lo que sugiere una interacción funcional entre sueño y regulación emocional mediada por este sistema. (Babson et al., 2017)
El sueño también desempeña un papel clave en el metabolismo energético. La privación de sueño se ha asociado con alteraciones en el equilibrio energético, incluyendo cambios en hormonas como la leptina y la grelina. El SEC, que también regula el apetito y el metabolismo, podría actuar como un nexo entre sueño y balance energético, integrando señales metabólicas y neuroendocrinas. (Pava et al., 2016)
A nivel inmunológico, el sueño favorece la función del sistema inmune, promoviendo la liberación de citoquinas y facilitando procesos de reparación tisular. La alteración crónica del sueño se asocia con estados proinflamatorios. Dado que el SEC también modula la respuesta inmune, su papel en este contexto podría contribuir a la regulación de la inflamación en relación con el ciclo sueño-vigilia. (Irwin, 2015)
Otra función relevante es la eliminación de metabolitos cerebrales a través del sistema glinfático, especialmente durante el sueño profundo. Este proceso permite la eliminación de productos de desecho acumulados durante la vigilia, contribuyendo a la homeostasis neuronal. Aunque la relación directa con el SEC aún se encuentra en investigación, la modulación de la actividad neuronal por este sistema podría influir indirectamente en estos mecanismos. (Xie et al., 2013)
En conjunto, el sueño emerge como un proceso integrador que afecta a múltiples sistemas fisiológicos, y el sistema endocannabinoide se posiciona como un modulador que influye en varias de estas funciones, desde la plasticidad sináptica hasta la regulación emocional y metabólica.
Implicaciones en investigación
El estudio de la fisiología del sueño y su interacción con el sistema endocannabinoide (SEC) ha generado un creciente interés en las últimas décadas, especialmente por su potencial como modulador de procesos complejos relacionados con la regulación del ciclo sueño-vigilia. Sin embargo, la evidencia disponible muestra una elevada variabilidad, lo que obliga a interpretar los resultados con cautela y dentro de un contexto estrictamente científico. (Suraev et al., 2020)
Gran parte del conocimiento actual proviene de estudios preclínicos en modelos animales, donde se ha observado que la manipulación del SEC —ya sea mediante la administración de endocannabinoides, agonistas o inhibidores enzimáticos— puede alterar parámetros del sueño como la latencia, la duración y la arquitectura de las fases NREM y REM. Estos hallazgos han permitido establecer una relación funcional entre la señalización endocannabinoide y la regulación del sueño, aunque su extrapolación directa a humanos presenta limitaciones. (Murillo-Rodríguez, 2008)
En humanos, los estudios clínicos disponibles son aún limitados y heterogéneos. Las diferencias en diseño experimental, tipo de compuesto, dosis, vía de administración y características de la población estudiada dificultan la obtención de conclusiones consistentes. Además, los efectos observados pueden variar en función del contexto fisiológico, incluyendo factores como el estado basal del sueño, la presencia de alteraciones previas o la interacción con otros sistemas neuroquímicos. (Babson et al., 2017)
Un aspecto clave en investigación es la diferenciación entre los efectos de los endocannabinoides endógenos y los fitocannabinoides exógenos. Mientras que el SEC actúa como un sistema modulador fisiológico fino y localizado, los compuestos exógenos pueden generar efectos más amplios y menos específicos, dependiendo de su perfil farmacológico. Esta distinción es esencial para interpretar los resultados y evitar simplificaciones en la comprensión de estos mecanismos. (Pertwee, 2008)
Otro reto importante es la caracterización del papel del SEC en la arquitectura del sueño a nivel temporal. Las variaciones circadianas en los niveles de endocannabinoides sugieren que su función no es estática, sino que cambia a lo largo del día. Comprender esta dinámica podría aportar información relevante sobre cómo se regulan las transiciones entre estados de vigilia y sueño en condiciones fisiológicas. (Murillo-Rodríguez et al., 2006)
Además, la investigación futura deberá integrar enfoques multidisciplinares que combinen neuroimagen, electrofisiología y análisis molecular para mapear con mayor precisión la interacción entre el SEC y los circuitos del sueño. Este tipo de aproximación permitirá avanzar hacia una comprensión más completa de la regulación del sueño como un sistema distribuido y altamente dinámico. (Saper et al., 2010)
En conjunto, el estudio del sueño y el sistema endocannabinoide representa un campo en expansión que refleja la complejidad de los sistemas biológicos implicados. Aunque los avances son significativos, aún existen múltiples preguntas abiertas que requieren investigación adicional para ser abordadas con rigor.
Véase también
- Sistema endocannabinoide (SEC)
- Señalización endocannabinoide
- Homeostasis
- Sistema nervioso
- Regulación del apetito
Referencias
- Aserinsky, E., & Kleitman, N. (1953). Regularly occurring periods of eye motility, and concomitant phenomena, during sleep. Science, 118(3062), 273–274. - Babson, K. A., Sottile, J., & Morabito, D. (2017). Cannabis, cannabinoids, and sleep: a review of the literature. Current Psychiatry Reports, 19(4), 23. - Borbély, A. A. (1982). A two process model of sleep regulation. Human Neurobiology, 1(3), 195–204. - Borbély, A. A., Daan, S., Wirz-Justice, A., & Deboer, T. (2016). The two-process model of sleep regulation: a reappraisal. Journal of Sleep Research, 25(2), 131–143. - Bremer, F. (1935). Cerveau isolé et physiologie du sommeil. Comptes Rendus des Séances de la Société de Biologie, 118, 1235–1241 . - Carskadon, M. A., & Dement, W. C. (2011). Normal human sleep: an overview. In Principles and Practice of Sleep Medicine (5th ed.). Elsevier. - Castillo, P. E., Younts, T. J., Chávez, A. E., & Hashimotodani, Y. (2012). Endocannabinoid signaling and synaptic function. Neuron, 76(1), 70–81. - Cravatt, B. F., Giang, D. K., Mayfield, S. P., Boger, D. L., Lerner, R. A., & Gilula, N. B. (2001). Molecular characterization of an enzyme that degrades neuromodulatory fatty-acid amides. Nature, 384(6604), 83–87. - Devane, W. A., Hanus, L., Breuer, A., et al. (1992). Isolation and structure of a brain constituent that binds to the cannabinoid receptor. Science, 258(5090), 1946–1949. - Diekelmann, S., & Born, J. (2010). The memory function of sleep. Nature Reviews Neuroscience, 11(2), 114–126. - Herkenham, M., Lynn, A. B., Little, M. D., et al. (1990). Cannabinoid receptor localization in brain. Proceedings of the National Academy of Sciences, 87(5), 1932–1936. - Huang, H., Acuna-Goycolea, C., Li, Y., Cheng, H. M., Obrietan, K., & van den Pol, A. N. (2007). Cannabinoids modulate excitatory inputs to hypocretin/orexin neurons. Journal of Neuroscience, 27(18), 4870–4881. - Irwin, M. R. (2015). Why sleep is important for health: a psychoneuroimmunology perspective. Annual Review of Psychology, 66, 143–172. - Kano, M., Ohno-Shosaku, T., Hashimotodani, Y., Uchigashima, M., & Watanabe, M. (2009). Endocannabinoid-mediated control of synaptic transmission. Physiological Reviews, 89(1), 309–380. - Moruzzi, G., & Magoun, H. W. (1949). Brain stem reticular formation and activation of the EEG. Electroencephalography and Clinical Neurophysiology, 1(1–4), 455–473. - Murillo-Rodríguez, E. (2008). The role of the CB1 receptor in the regulation of sleep. Progress in Neuro-Psychopharmacology & Biological Psychiatry, 32(6), 1420–1427. - Murillo-Rodríguez, E., Blanco-Centurion, C., Sánchez, C., Piomelli, D., & Shiromani, P. J. (2001). Anandamide enhances extracellular levels of adenosine and induces sleep: an in vivo microdialysis study. Sleep, 24(8), 869–877. - Murillo-Rodríguez, E., Millán-Aldaco, D., Palomero-Rivero, M., et al. (2006). Anandamide levels fluctuate with the sleep–wake cycle. NeuroReport, 17(11), 1091–1094. - Pava, M. J., Makriyannis, A., & Lovinger, D. M. (2016). Endocannabinoid signaling regulates sleep stability. Sleep, 39(4), 757–768. - Pertwee, R. G. (2008). The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids. British Journal of Pharmacology, 153(2), 199–215. - Saper, C. B., Fuller, P. M., Pedersen, N. P., Lu, J., & Scammell, T. E. (2010). Sleep state switching. Neuron, 68(6), 1023–1042. - Saper, C. B., Scammell, T. E., & Lu, J. (2005). Hypothalamic regulation of sleep and circadian rhythms. Nature, 437(7063), 1257–1263. - Suraev, A. S., Marshall, N. S., Vandrey, R., et al. (2020). Cannabinoid therapies in the management of sleep disorders: a systematic review. Sleep Medicine Reviews, 53, 101339. - Xie, L., Kang, H., Xu, Q., et al. (2013). Sleep drives metabolite clearance from the adult brain. Science, 342(6156), 373–377.