Introducción
El sistema nervioso constituye una red altamente organizada de células especializadas cuya función principal es la recepción, procesamiento e integración de información, así como la generación de respuestas adaptativas frente a estímulos internos y externos. Esta red se divide clásicamente en sistema nervioso central (SNC), que incluye el cerebro y la médula espinal, y sistema nervioso periférico (SNP), encargado de conectar el SNC con el resto del organismo. La actividad coordinada de estos sistemas permite funciones tan diversas como la percepción sensorial, el control motor, la regulación autónoma y los procesos cognitivos complejos. (Kandel et al., 2021)
A nivel celular, la unidad funcional del sistema nervioso es la neurona, una célula excitable capaz de generar y transmitir señales eléctricas y químicas. La comunicación entre neuronas ocurre principalmente en las sinapsis, donde la liberación de neurotransmisores desde la terminal presináptica modula la actividad de la célula postsináptica. Este proceso no es estático, sino dinámico y altamente regulado, permitiendo fenómenos como la plasticidad sináptica, que subyace a procesos como el aprendizaje y la memoria. (Purves et al., 2018)
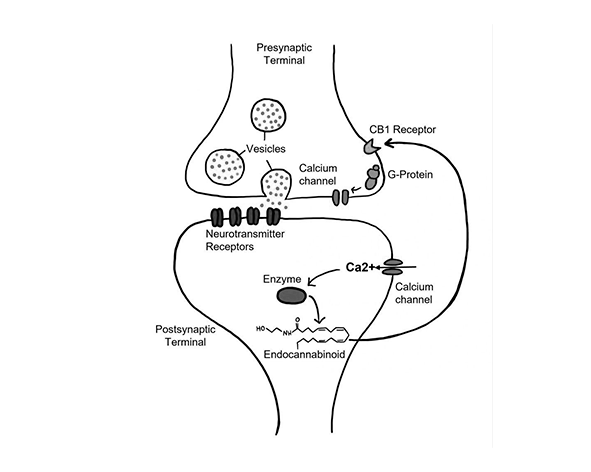
En este contexto de complejidad y regulación fina, el sistema endocannabinoide (SEC) se integra como un sistema modulador clave de la neurotransmisión. A diferencia de otros sistemas de señalización, los endocannabinoides no se almacenan en vesículas sinápticas, sino que se sintetizan “a demanda” en la neurona postsináptica y actúan de forma retrógrada sobre receptores presinápticos, principalmente el receptor CB1. Este mecanismo permite una regulación precisa de la liberación de neurotransmisores, ajustando la intensidad de la señal sináptica en función del estado fisiológico del sistema. (Kano et al., 2009; Castillo et al., 2012)
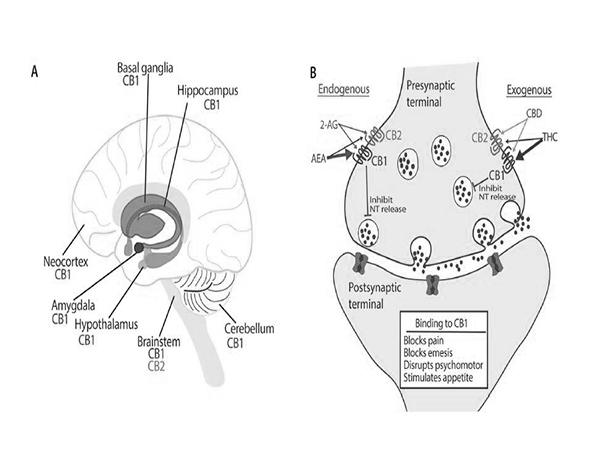
El receptor CB1 es especialmente abundante en el sistema nervioso central, con una distribución destacada en regiones como la corteza cerebral, el hipocampo, los ganglios basales y el cerebelo. Esta localización sugiere una implicación directa del SEC en funciones como la coordinación motora, la memoria, la percepción del dolor y la regulación emocional. Además, su presencia en interneuronas inhibitorias y excitatorias permite una modulación bidireccional de los circuitos neuronales, contribuyendo al equilibrio entre excitación e inhibición. (Herkenham et al., 1990; Freund et al., 2003)
Más allá de su papel en la neurotransmisión clásica, el SEC participa en la regulación de procesos neuronales de mayor escala, incluyendo la respuesta al estrés, la adaptación a estímulos ambientales y la neuroprotección en condiciones de desequilibrio fisiológico. Este enfoque sitúa al SEC no como un sistema aislado, sino como un componente integrador dentro de la fisiología del sistema nervioso, implicado en la preservación de la homeostasis neuronal. (Lutz, 2020; Morena et al., 2016)
En conjunto, el estudio del sistema endocannabinoide en el sistema nervioso permite comprender cómo los mecanismos de señalización lipídica contribuyen a la regulación fina de la actividad neuronal. Esta perspectiva ha abierto nuevas líneas de investigación en neurobiología, especialmente en relación con la plasticidad sináptica, la modulación del comportamiento y la respuesta del organismo frente a perturbaciones internas y externas. (Lu & Mackie, 2016)
Historia del descubrimiento
El entendimiento del sistema endocannabinoide en el contexto del sistema nervioso es relativamente reciente dentro de la historia de la neurobiología, a pesar de que sus bases se asientan sobre décadas de investigación en farmacología del cannabis. Durante gran parte del siglo XX, los efectos del cannabis sobre el sistema nervioso eran conocidos a nivel fenomenológico —alteraciones en la percepción, la memoria o la coordinación—, pero se desconocían los mecanismos moleculares responsables de estos efectos. La ausencia de un receptor identificado dificultaba interpretar estos fenómenos dentro de los marcos clásicos de la neurotransmisión. (Mechoulam, 1986; Pertwee, 2006)
Un punto de inflexión se produjo en 1964, cuando Raphael Mechoulam y Yechiel Gaoni lograron aislar y caracterizar químicamente el Δ9-tetrahidrocannabinol (THC), el principal compuesto psicoactivo de Cannabis sativa. Este descubrimiento permitió por primera vez estudiar de forma sistemática los efectos de un compuesto definido sobre el sistema nervioso, sentando las bases para la búsqueda de su mecanismo de acción a nivel celular. Sin embargo, durante más de dos décadas, la pregunta clave permaneció sin resolver: ¿cómo interactuaba el THC con el cerebro? (Gaoni & Mechoulam, 1964; Mechoulam, 1986)
La respuesta comenzó a emerger en 1988, cuando Allyn Howlett y su equipo identificaron un sitio de unión específico para cannabinoides en el cerebro de mamíferos, lo que indicaba la presencia de un receptor hasta entonces desconocido. Este hallazgo, basado en técnicas de radioligandos, supuso un cambio conceptual fundamental: el THC no actuaba de manera inespecífica sobre las membranas celulares, sino que ejercía sus efectos a través de un receptor específico, posteriormente denominado CB1. La elevada densidad de estos receptores en regiones cerebrales clave reforzó la hipótesis de un sistema fisiológico endógeno aún por descubrir. (Devane et al., 1988)
Poco después, en 1990, se logró clonar el receptor CB1, confirmando su naturaleza como receptor acoplado a proteína G (GPCR) y permitiendo estudiar su distribución con mayor precisión en el sistema nervioso. Este avance consolidó la idea de que el cerebro disponía de una maquinaria específica para responder a compuestos cannabinoides, lo que planteaba inevitablemente la existencia de ligandos endógenos capaces de activar dicho sistema. (Matsuda et al., 1990)
Este interrogante fue resuelto en 1992, cuando Raphael Mechoulam y su equipo identificaron la anandamida (AEA), el primer endocannabinoide descrito. El nombre deriva del término sánscrito “ananda”, que significa “felicidad” o “bienestar”, en referencia a sus efectos observados en modelos experimentales. La identificación de la anandamida marcó el nacimiento formal del sistema endocannabinoide como sistema biológico endógeno, integrando receptor, ligando y función en un mismo marco conceptual. (Devane et al., 1992; Mechoulam et al., 1995)
Posteriormente, en 1995, se identificó el 2-araquidonoilglicerol (2-AG), un segundo endocannabinoide con mayor abundancia en el cerebro y un papel central en la señalización sináptica. A diferencia de la anandamida, el 2-AG mostró una participación más directa en procesos de neurotransmisión, consolidando la idea de que el SEC no era un sistema accesorio, sino un regulador activo de la comunicación neuronal. (Mechoulam et al., 1995; Sugiura et al., 1995)
Durante la década de 1990 y principios de los 2000, una serie de descubrimientos adicionales completaron el esquema funcional del sistema endocannabinoide, incluyendo la identificación de enzimas responsables de la síntesis y degradación de los endocannabinoides, como la FAAH y la MAGL. Estos hallazgos permitieron entender que el SEC opera mediante un mecanismo altamente dinámico, en el que los ligandos se producen y degradan rápidamente en respuesta a la actividad neuronal. (Cravatt et al., 1996; Dinh et al., 2002)
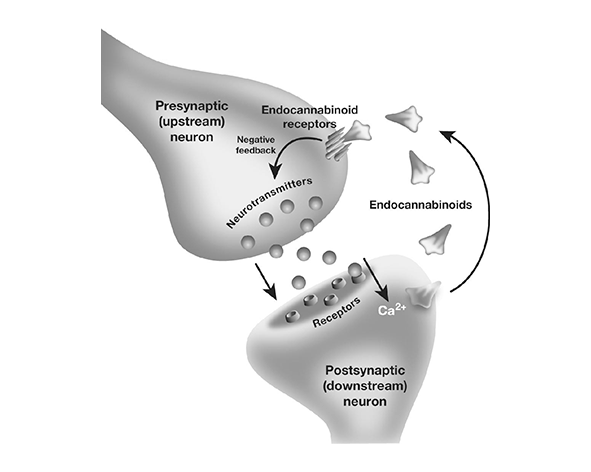
Uno de los avances conceptuales más relevantes en la comprensión del papel del SEC en el sistema nervioso fue el descubrimiento de la señalización retrógrada. A diferencia de la neurotransmisión clásica, en la que la señal fluye de la neurona presináptica a la postsináptica, los endocannabinoides se liberan desde la neurona postsináptica y actúan sobre receptores CB1 en la terminal presináptica, modulando la liberación de neurotransmisores. Este mecanismo, descrito a principios de los años 2000, redefinió la forma en que se entendía la regulación sináptica. (Wilson & Nicoll, 2001; Kano et al., 2009)
En conjunto, estos descubrimientos transformaron la percepción del sistema endocannabinoide, pasando de ser una curiosidad farmacológica asociada al cannabis a constituir un sistema fisiológico fundamental en la regulación del sistema nervioso. Hoy en día, el SEC se considera un componente clave en la modulación de la actividad neuronal, con implicaciones en múltiples procesos biológicos y un papel central en la investigación neurocientífica contemporánea. (Lu & Mackie, 2016; Lutz et al., 2015)
Organización del sistema nervioso y distribución del sistema endocannabinoide
El sistema nervioso se organiza en múltiples niveles estructurales y funcionales que permiten integrar desde respuestas reflejas simples hasta procesos cognitivos complejos. A nivel anatómico, se divide en sistema nervioso central (SNC), compuesto por el encéfalo y la médula espinal, y sistema nervioso periférico (SNP), que incluye los nervios y ganglios que conectan el SNC con el resto del organismo. Esta organización jerárquica permite una distribución eficiente de la información y una coordinación precisa de las funciones fisiológicas. (Kandel et al., 2021)
Dentro del SNC, distintas regiones cumplen funciones específicas. La corteza cerebral está implicada en funciones superiores como la cognición, la percepción y la toma de decisiones; el hipocampo participa en la formación de memoria; los ganglios basales intervienen en el control del movimiento; el cerebelo coordina la actividad motora fina; y el tronco encefálico regula funciones autónomas esenciales como la respiración y la frecuencia cardíaca. Esta especialización regional es clave para entender cómo los sistemas moduladores, como el sistema endocannabinoide, ejercen efectos diferenciados según su localización. (Purves et al., 2018)
El sistema endocannabinoide presenta una distribución amplia y heterogénea en el sistema nervioso, con una densidad particularmente elevada del receptor CB1 en el cerebro. Este receptor es uno de los GPCR más abundantes en el SNC, lo que sugiere un papel central en la regulación de la actividad neuronal. Su expresión es especialmente alta en regiones como el hipocampo, la corteza cerebral, los ganglios basales y el cerebelo, todas ellas implicadas en funciones clave como la memoria, el control motor y la integración sensorial. (Herkenham et al., 1990; Freund et al., 2003)
A nivel celular, el receptor CB1 se localiza predominantemente en terminales presinápticas, tanto de neuronas excitatorias (glutamatérgicas) como inhibitorias (GABAérgicas). Esta localización permite al sistema endocannabinoide modular la liberación de neurotransmisores en ambos tipos de sinapsis, ajustando el equilibrio entre excitación e inhibición dentro de los circuitos neuronales. Este equilibrio es fundamental para el funcionamiento adecuado del sistema nervioso, ya que pequeñas alteraciones pueden afectar significativamente la dinámica de red neuronal. (Katona & Freund, 2012)
Además del SNC, el sistema endocannabinoide también se encuentra presente en el sistema nervioso periférico, incluyendo neuronas sensoriales y fibras nerviosas implicadas en la transmisión de señales desde la periferia hacia el sistema central. Esta distribución sugiere que el SEC no solo modula procesos centrales, sino que también participa en la regulación de la señalización sensorial desde etapas tempranas de procesamiento. (Pertwee, 2008)
Otro aspecto relevante es la distribución diferencial de los endocannabinoides y las enzimas que regulan su metabolismo. La anandamida (AEA) y el 2-AG no se distribuyen de manera uniforme, y su concentración varía según la región cerebral y el estado fisiológico. Asimismo, enzimas como la FAAH y la MAGL presentan patrones de expresión específicos, lo que contribuye a una regulación local y altamente dinámica de la señalización endocannabinoide. (Blankman & Cravatt, 2013)
Esta organización espacial del sistema endocannabinoide permite una modulación fina y localizada de la actividad neuronal. En lugar de actuar como un sistema difuso o global, el SEC opera en microdominios sinápticos específicos, donde regula la transmisión neuronal en función de las necesidades del circuito. Esta característica es clave para entender su papel en procesos como la plasticidad sináptica y la adaptación a estímulos cambiantes. (Castillo et al., 2012)
En conjunto, la distribución del sistema endocannabinoide en el sistema nervioso refleja su papel como sistema modulador integrado, capaz de influir en múltiples niveles de organización neuronal. Desde la regulación local de la liberación de neurotransmisores hasta la modulación de redes neuronales complejas, el SEC actúa como un mecanismo de ajuste fino que contribuye a la estabilidad funcional del sistema nervioso. (Lu & Mackie, 2016)
Mecanismos de interacción entre el sistema endocannabinoide y la neurotransmisión
El sistema endocannabinoide (SEC) actúa como un modulador sináptico cuya principal característica es su capacidad para regular la neurotransmisión de forma dinámica y dependiente de la actividad neuronal. A diferencia de los neurotransmisores clásicos, los endocannabinoides no se almacenan en vesículas presinápticas, sino que se sintetizan “a demanda” en la neurona postsináptica a partir de precursores lipídicos de membrana. Esta síntesis ocurre en respuesta a aumentos en la actividad neuronal, particularmente elevaciones en los niveles intracelulares de calcio o activación de receptores acoplados a proteína G. (Kano et al., 2009; Castillo et al., 2012)
Una vez sintetizados, los endocannabinoides —principalmente anandamida (AEA) y 2-araquidonoilglicerol (2-AG)— difunden a través de la membrana celular y viajan en dirección retrógrada hacia la terminal presináptica. Allí se unen a receptores CB1 localizados en la membrana presináptica, activando una cascada de señalización intracelular que resulta en la inhibición de la liberación de neurotransmisores. Este mecanismo de señalización retrógrada representa una desviación fundamental del modelo clásico de neurotransmisión, introduciendo un sistema de control inverso que permite a la neurona postsináptica modular su propia entrada sináptica. (Wilson & Nicoll, 2001; Kano et al., 2009)
La activación del receptor CB1, un receptor acoplado a proteínas G de tipo Gi/o, conduce a la inhibición de la adenilato ciclasa, la reducción de los niveles de AMPc y la modulación de canales iónicos, incluyendo la inhibición de canales de calcio dependientes de voltaje y la activación de canales de potasio. Estas acciones disminuyen la probabilidad de liberación de vesículas sinápticas, reduciendo la liberación de neurotransmisores como glutamato o GABA. De este modo, el SEC actúa como un regulador negativo de la transmisión sináptica. (Howlett et al., 2002; Pertwee, 2008)
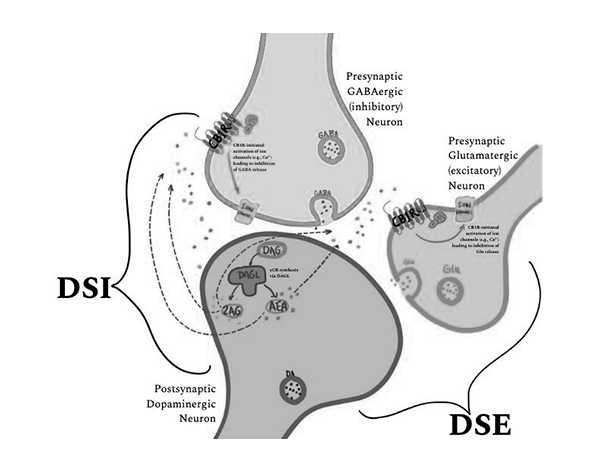
Este mecanismo da lugar a fenómenos conocidos como supresión de la inhibición dependiente de despolarización (DSI) y supresión de la excitación dependiente de despolarización (DSE). En el caso de la DSI, la liberación de endocannabinoides reduce la liberación de GABA desde neuronas inhibitorias, lo que puede resultar en un aumento transitorio de la excitabilidad neuronal. En la DSE, el proceso afecta a sinapsis excitatorias, reduciendo la liberación de glutamato. Ambos fenómenos ilustran cómo el SEC puede modular de forma bidireccional la actividad neuronal dependiendo del contexto sináptico. (Kreitzer & Regehr, 2001; Ohno-Shosaku et al., 2001)
Más allá de estos efectos a corto plazo, el sistema endocannabinoide también participa en formas de plasticidad sináptica a largo plazo, como la depresión a largo plazo (LTD) mediada por endocannabinoides. En este proceso, la activación sostenida del SEC conduce a una reducción duradera en la eficacia sináptica, lo que tiene implicaciones en la reorganización de circuitos neuronales y en procesos como el aprendizaje y la adaptación conductual. Este tipo de plasticidad ha sido ampliamente descrito en regiones como el hipocampo y los ganglios basales. (Gerdeman et al., 2002; Castillo et al., 2012)
Otro aspecto relevante es la especificidad espacial y temporal de la señalización endocannabinoide. Debido a su rápida síntesis y degradación —mediada por enzimas como FAAH para la anandamida y MAGL para el 2-AG—, los endocannabinoides actúan en microdominios sinápticos específicos y durante ventanas temporales limitadas. Esto permite una regulación extremadamente precisa de la neurotransmisión, evitando efectos generalizados o descontrolados en la red neuronal. (Dinh et al., 2002; Blankman & Cravatt, 2013)
Además, el SEC no actúa de forma aislada, sino que interactúa con otros sistemas de neurotransmisión, incluyendo los sistemas dopaminérgico, glutamatérgico y GABAérgico. Estas interacciones permiten que el sistema endocannabinoide influya en procesos complejos como la motivación, la recompensa, la toma de decisiones y la regulación emocional, integrándose en redes neuronales de mayor escala. (Lutz et al., 2015; Lu & Mackie, 2016)
En conjunto, los mecanismos de interacción del sistema endocannabinoide con la neurotransmisión reflejan un sistema de control sofisticado, capaz de ajustar la actividad sináptica en función del contexto fisiológico. Este papel modulador sitúa al SEC como un elemento central en la regulación de la dinámica neuronal, contribuyendo tanto a la estabilidad como a la adaptabilidad del sistema nervioso. (Castillo et al., 2012)
Funciones fisiológicas del sistema endocannabinoide en el sistema nervioso
El sistema endocannabinoide (SEC) participa en la regulación de múltiples funciones del sistema nervioso, actuando como un modulador que ajusta la actividad neuronal en función del estado fisiológico del organismo. Su papel no consiste en iniciar respuestas específicas, sino en modular la intensidad, duración y contexto de la señalización neuronal, contribuyendo a la estabilidad funcional de los circuitos. Esta capacidad de ajuste fino es especialmente relevante en procesos que requieren equilibrio dinámico, como la percepción, la emoción o la respuesta al entorno. (Lu & Mackie, 2016)
Una de las funciones más estudiadas del SEC en el sistema nervioso es su implicación en la plasticidad sináptica, un proceso fundamental para el aprendizaje y la memoria. En regiones como el hipocampo, los endocannabinoides modulan la eficacia de las sinapsis mediante mecanismos como la depresión a largo plazo (LTD), permitiendo la reorganización de circuitos neuronales en función de la experiencia. Este tipo de plasticidad no solo afecta a la formación de recuerdos, sino también a la adaptación del sistema nervioso a estímulos repetidos o cambiantes. (Castillo et al., 2012; Kano et al., 2009)
El SEC también desempeña un papel relevante en la modulación de la percepción del dolor a nivel central. A través de la regulación de la liberación de neurotransmisores en regiones como la médula espinal y estructuras supraspinales, los endocannabinoides influyen en la transmisión de señales nociceptivas. Este efecto no implica una inhibición directa del dolor como mecanismo único, sino una modulación de las vías que procesan la información nociceptiva, integrándose con otros sistemas neuroquímicos implicados en la percepción sensorial. (Pertwee, 2001; Walker & Huang, 2002)
En el ámbito de la regulación emocional, el sistema endocannabinoide interviene en circuitos neuronales asociados al estrés, la ansiedad y la respuesta adaptativa a estímulos aversivos. Regiones como la amígdala y la corteza prefrontal presentan una alta expresión de receptores CB1, lo que permite que el SEC module la excitabilidad neuronal en estos circuitos. Esta modulación contribuye a la adaptación frente a estímulos estresantes, evitando respuestas excesivas o desproporcionadas. (Lutz, 2020; Morena et al., 2016)
Asimismo, el SEC está implicado en la regulación de la motivación y el comportamiento dirigido a objetivos, a través de su interacción con el sistema dopaminérgico. En estructuras como el núcleo accumbens y otras regiones del sistema de recompensa, los endocannabinoides modulan la liberación de dopamina de forma indirecta, influyendo en la evaluación de estímulos y en la toma de decisiones. Este papel integrador sitúa al SEC como un modulador relevante en la dinámica de circuitos asociados a la motivación y el refuerzo. (Lupica et al., 2004; Parsons & Hurd, 2015)
Otra función importante del sistema endocannabinoide es su participación en la regulación del sueño y los ritmos circadianos. Aunque los mecanismos exactos continúan en estudio, se ha observado que los endocannabinoides pueden influir en la arquitectura del sueño mediante la modulación de circuitos neuronales implicados en la transición entre estados de vigilia y descanso. Este efecto se relaciona con la capacidad del SEC para ajustar la excitabilidad neuronal en función de las necesidades fisiológicas del organismo. (Murillo-Rodríguez et al., 2011)
Además, el sistema endocannabinoide contribuye a procesos de neuroprotección en contextos de desequilibrio fisiológico. En situaciones de estrés celular, excitotoxicidad o inflamación neuronal, la activación del SEC puede modular la liberación de neurotransmisores y la actividad de células gliales, reduciendo potencialmente el daño neuronal. Este papel no debe interpretarse como un mecanismo terapéutico directo, sino como una función fisiológica de adaptación frente a condiciones adversas. (Marsicano et al., 2003; Fernández-Ruiz et al., 2007)
En conjunto, las funciones del sistema endocannabinoide en el sistema nervioso reflejan su papel como un sistema modulador transversal, implicado en la regulación de procesos cognitivos, emocionales y sensoriales. Su capacidad para integrar señales a diferentes niveles de organización neuronal lo convierte en un elemento clave en la fisiología del sistema nervioso, especialmente en la adaptación del organismo a un entorno cambiante. (Lu & Mackie, 2016)
Implicaciones en investigación y contexto científico actual
El estudio del sistema endocannabinoide (SEC) en el sistema nervioso ha experimentado una expansión significativa en las últimas décadas, consolidándose como un área de investigación relevante dentro de la neurobiología y la farmacología. Este interés no se debe únicamente a su relación con compuestos derivados de Cannabis sativa, sino a su papel intrínseco como sistema modulador de la actividad neuronal. En este sentido, el SEC ha pasado de ser un objeto de estudio periférico a convertirse en un componente central en la comprensión de la regulación sináptica y la homeostasis neuronal. (Lu & Mackie, 2016; Castillo et al., 2012)
Uno de los principales focos de investigación se centra en la caracterización detallada de los mecanismos mediante los cuales los endocannabinoides regulan la plasticidad sináptica. Aunque procesos como la depresión a largo plazo (LTD) mediada por endocannabinoides han sido ampliamente descritos, persisten interrogantes sobre su papel específico en diferentes tipos de neuronas y circuitos. Asimismo, se investiga cómo estas formas de plasticidad interactúan con otros mecanismos sinápticos, lo que resulta clave para comprender la dinámica global de las redes neuronales. (Castillo et al., 2012; Kano et al., 2009)
Otro ámbito relevante es el estudio de la heterogeneidad del sistema endocannabinoide en el cerebro. La expresión de receptores CB1, así como la distribución de enzimas como FAAH y MAGL, varía significativamente entre regiones y tipos celulares. Esta diversidad sugiere que el SEC no actúa como un sistema uniforme, sino como un conjunto de módulos funcionales con roles específicos dependiendo del contexto neuronal. La comprensión de esta variabilidad es fundamental para interpretar los efectos diferenciales observados en distintos modelos experimentales. (Katona & Freund, 2012; Blankman & Cravatt, 2013)
Además, existe un creciente interés en la interacción del sistema endocannabinoide con otros sistemas de señalización, incluyendo sistemas neurotransmisores clásicos y vías de señalización intracelular. Estas interacciones permiten que el SEC participe en procesos complejos como la integración sensorial, la regulación emocional y la adaptación conductual. Sin embargo, la naturaleza de estas interacciones es altamente dependiente del contexto, lo que dificulta establecer modelos generalizables. (Lutz et al., 2015)
Desde una perspectiva metodológica, el estudio del SEC plantea desafíos específicos debido a la naturaleza lipídica de los endocannabinoides y su rápida degradación. La medición precisa de sus niveles, así como la manipulación selectiva de sus rutas metabólicas, requiere técnicas avanzadas que continúan evolucionando. Estos aspectos limitan en parte la interpretación de resultados y explican la variabilidad observada entre estudios. (Di Marzo, 2008)
En el contexto actual, la investigación sobre el sistema endocannabinoide en el sistema nervioso se orienta hacia una comprensión más integrada de su papel en la fisiología neuronal. Esto implica no solo el estudio de componentes individuales —receptores, ligandos o enzimas—, sino también su interacción dentro de redes complejas. Este enfoque sistémico refleja una tendencia más amplia en biología, donde los sistemas de señalización se entienden como redes dinámicas en lugar de vías lineales. (Lu & Mackie, 2016)
Es importante destacar que, aunque el conocimiento sobre el SEC ha avanzado considerablemente, muchas de sus funciones aún están en fase de investigación. La mayoría de los datos disponibles provienen de modelos preclínicos, lo que requiere cautela al interpretar su relevancia en contextos fisiológicos complejos. Este marco sitúa al sistema endocannabinoide como un campo activo de investigación, en constante evolución y sujeto a revisión a medida que emergen nuevas evidencias. (Pertwee, 2008)
En conjunto, el sistema endocannabinoide representa un ejemplo paradigmático de cómo un sistema de señalización inicialmente asociado a un compuesto exógeno puede revelar una función fisiológica fundamental. Su estudio continúa aportando nuevas perspectivas sobre la organización y regulación del sistema nervioso, consolidando su papel como uno de los sistemas moduladores más relevantes en la neurobiología contemporánea. (Lu & Mackie, 2016)
Véase también
- Sistema endocannabinoide — Visión general del sistema de señalización endógeno, incluyendo sus componentes principales, organización y función en la homeostasis fisiológica.
- Receptor CB1 — Receptor cannabinoide predominante en el sistema nervioso central, implicado en la modulación de la neurotransmisión y la plasticidad sináptica.
- Anandamida (AEA) — Endocannabinoide derivado de lípidos de membrana, implicado en la señalización retrógrada y la regulación de la actividad sináptica.
- 2-araquidonoilglicerol (2-AG) — Endocannabinoide abundante en el cerebro, con un papel central en la modulación de la neurotransmisión excitatoria e inhibitoria.
Referencias
- Blankman JL, Simon GM, Cravatt BF. (2007). A comprehensive profile of brain enzymes that hydrolyze the endocannabinoids 2-arachidonoylglycerol and anandamide. Chemistry & Biology, 14(12), 1347–1356. - Castillo PE, Younts TJ, Chávez AE, Hashimotodani Y. (2012). Endocannabinoid signaling and synaptic function. Neuron, 76(1), 70–81. - Cravatt BF, Giang DK, Mayfield SP, Boger DL, Lerner RA, Gilula NB. (1996). Molecular characterization of an enzyme that degrades neuromodulatory fatty-acid amides. Nature, 384, 83–87. - Devane WA, Dysarz FA, Johnson MR, Melvin LS, Howlett AC. (1988). Determination and characterization of a cannabinoid receptor in rat brain. Molecular Pharmacology, 34(5), 605–613. - Devane WA, Hanus L, Breuer A, Pertwee RG, Stevenson LA, Griffin G, Gibson D, Mandelbaum A, Etinger A, Mechoulam R. (1992). Isolation and structure of a brain constituent that binds to the cannabinoid receptor. Science, 258(5090), 1946–1949. - Dinh TP, Carpenter D, Leslie FM, Freund TF, Katona I, Sensi SL, Kathuria S, Piomelli D. (2002). Brain monoglyceride lipase participating in endocannabinoid inactivation. Proceedings of the National Academy of Sciences USA, 99(16), 10819–10824. - Freund TF, Katona I, Piomelli D. (2003). Role of endogenous cannabinoids in synaptic signaling. Physiological Reviews, 83(3), 1017–1066. - Gerdeman G, Ronesi J, Lovinger DM. (2002). Postsynaptic endocannabinoid release is critical to long-term depression in the striatum. Nature Neuroscience, 5(5), 446–451. - Herkenham M, Lynn AB, Little MD, Johnson MR, Melvin LS, de Costa BR, Rice KC. (1990). Cannabinoid receptor localization in brain. Proceedings of the National Academy of Sciences USA, 87(5), 1932–1936. - Howlett AC, Barth F, Bonner TI, Cabral G, Casellas P, Devane WA, Felder CC, Herkenham M, Mackie K, Martin BR, Mechoulam R, Pertwee RG. (2002). International Union of Pharmacology. XXVII. - Classification of cannabinoid receptors. Pharmacological Reviews, 54(2), 161–202. - Kano M, Ohno-Shosaku T, Hashimotodani Y, Uchigashima M, Watanabe M. (2009). Endocannabinoid-mediated control of synaptic transmission. Physiological Reviews, 89(1), 309–380. - Katona I, Freund TF. (2012). Multiple functions of endocannabinoid signaling in the brain. Annual Review of Neuroscience, 35, 529–558. - Kreitzer AC, Regehr WG. (2001). Retrograde inhibition of presynaptic calcium influx by endogenous cannabinoids at excitatory synapses. Neuron, 29(3), 717–727. - Lu HC, Mackie K. (2016). An introduction to the endogenous cannabinoid system. Biological Psychiatry, 79(7), 516–525. - Lupica CR, Riegel AC, Hoffman AF. (2004). Marijuana and cannabinoid regulation of brain reward circuits. British Journal of Pharmacology, 143(2), 227–234. - Lutz B, Marsicano G, Maldonado R, Hillard CJ. (2015). The endocannabinoid system in guarding against fear, anxiety and stress. Nature Reviews Neuroscience, 16(12), 705–718. - Lutz B. (2020). Neurobiology of cannabinoid receptor signaling. Dialogues in Clinical Neuroscience, 22(3), 207–222. - Marsicano G, Goodenough S, Monory K, Hermann H, Eder M, Cannich A, Azad SC, Cascio MG, Gutierrez SO, van der Stelt M, López-Rodríguez ML, Casanova E, Schütz G, Zieglgänsberger W, Di Marzo V, - - Behl C, Lutz B. (2003). CB1 cannabinoid receptors and on-demand defense against excitotoxicity. Science, 302(5642), 84–88. - Morena M, Patel S, Bains JS, Hill MN. (2016). Neurobiological interactions between stress and the endocannabinoid system. Neuropsychopharmacology, 41(1), 80–102. - Murillo-Rodríguez E, Millán-Aldaco D, Palomero-Rivero M, Mechoulam R, Drucker-Colín R. (2011). The role of the CB1 receptor in the regulation of sleep. Progress in Neuro-Psychopharmacology & Biological Psychiatry, 35(2), 476–483. Ohno-Shosaku T, Maejima T, Kano M. (2001). Endogenous cannabinoids mediate retrograde signals from depolarized postsynaptic neurons to presynaptic terminals. Neuron, 29(3), 729–738. - Parsons LH, Hurd YL. (2015). Endocannabinoid signaling in reward and addiction. Nature Reviews Neuroscience, 16(10), 579–594. - Pertwee RG. (2001). Cannabinoid receptors and pain. Progress in Neurobiology, 63(5), 569–611. - Pertwee RG. (2008). The diverse CB1 and CB2 receptor pharmacology. British Journal of Pharmacology, 153(2), 199–215. - Purves D, Augustine GJ, Fitzpatrick D, Hall WC, LaMantia AS, Mooney RD, Platt ML, White LE. (2018). Neuroscience (6th ed.). Oxford University Press. - Wilson RI, Nicoll RA. (2001). Endogenous cannabinoids mediate retrograde signalling at hippocampal synapses. Nature, 410, 588–592. - Kandel ER, Koester JD, Mack SH, Siegelbaum SA. (2021). Principles of Neural Science (6th ed.). McGraw-Hill.