Introducción
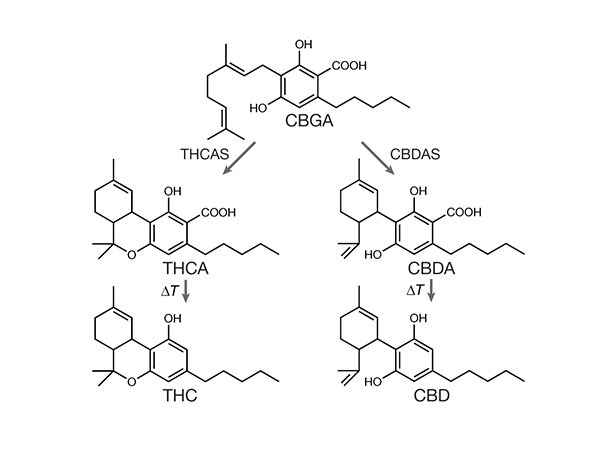
El ácido cannabigerólico (CBGA) es uno de los compuestos más importantes de la bioquímica del cannabis, no tanto por su abundancia final en los productos comerciales, sino por su posición central dentro de la ruta biosintética de la planta. En términos sencillos, el CBGA actúa como el gran precursor a partir del cual se originan varios de los principales cannabinoides ácidos, entre ellos el ácido tetrahidrocannabinólico (THCA), el ácido cannabidiólico (CBDA) y el ácido cannabicroménico (CBCA). Esta función nodal explica que en la literatura científica se le describa con frecuencia como el “cannabinoide madre”, una expresión informal pero útil para resumir su relevancia metabólica dentro de Cannabis sativa L. (Taura et al., 2007; Gülck & Møller, 2020).
A diferencia de cannabinoides más conocidos desde el punto de vista popular, como el CBD o el THC, el CBGA no suele ocupar el centro del discurso comercial ni mediático. Sin embargo, desde una perspectiva botánica y farmacognósica, su papel es más fundamental que accesorio. La planta no “empieza” fabricando THC o CBD en sentido estricto; lo que produce primero, dentro de una secuencia enzimática bien definida, es CBGA, que posteriormente puede ser transformado por distintas sintasas en otros cannabinoides ácidos. Por ello, comprender el CBGA equivale en buena medida a comprender cómo la planta construye su identidad química y por qué distintas variedades pueden acabar presentando perfiles cannabinoides tan diferentes entre sí (Gülck & Møller, 2020; Zirpel et al., 2018).
Desde el punto de vista estructural, el CBGA es un fitocannabinoide ácido prenilado, generado a partir de la condensación entre ácido olivetólico y geranil pirofosfato (GPP). Esa reacción constituye uno de los pasos clave de la vía biosintética cannabinoide y conecta el metabolismo de los policétidos con el de los terpenoides. Esta naturaleza híbrida, a medio camino entre ambas rutas metabólicas, ayuda a entender por qué los cannabinoides comparten rasgos químicos con otros compuestos fenólicos vegetales y, al mismo tiempo, mantienen una singularidad estructural propia del género Cannabis (Fellermeier & Zenk, 1998; Gülck & Møller, 2020).
El grupo carboxilo presente en el CBGA es una característica decisiva tanto para su comportamiento químico como para su destino biológico. Como ocurre con otros cannabinoides ácidos, el CBGA puede sufrir descarboxilación cuando se expone al calor, la luz o al simple paso del tiempo, dando lugar a su forma neutra correspondiente, el cannabigerol (CBG). Esto significa que una parte importante de la química observable en extractos, flores curadas o productos transformados depende no solo de lo que la planta sintetiza, sino también de lo que ocurre después durante el secado, almacenamiento o procesado. En consecuencia, diferenciar entre CBGA y CBG no es una cuestión menor de nomenclatura, sino una distinción esencial para interpretar correctamente tanto los análisis fitoquímicos como la literatura experimental (Hanuš et al., 2016; Wang et al., 2016).
En la planta, el CBGA se localiza principalmente en los tricomas glandulares, donde se concentra la maquinaria biosintética de cannabinoides y terpenos. Estos tricomas no son simples depósitos pasivos, sino microestructuras secretoras altamente especializadas que participan en la producción y acumulación de metabolitos secundarios. El estudio del CBGA, por tanto, no solo remite a la química de una molécula concreta, sino también a la biología celular del cannabis, a la regulación genética de sus enzimas y a la ecología química que pudo favorecer la evolución de estos compuestos en la planta (Livingston et al., 2020; Gülck & Møller, 2020).
Durante mucho tiempo, el interés científico en el CBGA fue principalmente biosintético, es decir, centrado en su función como precursor. Sin embargo, en años recientes también ha crecido la atención hacia sus posibles propiedades farmacológicas propias. Aunque la mayor parte de la evidencia sigue siendo preclínica y debe interpretarse con cautela, diversos trabajos han explorado su interacción con dianas moleculares relacionadas con inflamación, metabolismo energético, señalización intracelular y canales iónicos. Esto ha contribuido a desplazar la visión del CBGA como un simple “eslabón intermedio” y a considerarlo también como una molécula con interés experimental por derecho propio, aunque todavía lejos del nivel de caracterización alcanzado para otros fitocannabinoides más estudiados (Navarro et al., 2020; Borrelli et al., 2013).
Otro aspecto relevante es que el CBGA ayuda a explicar la enorme variabilidad química observada entre quimiotipos de cannabis. La cantidad de CBGA disponible y, sobre todo, la actividad relativa de las enzimas que lo convierten en THCA, CBDA o CBCA, condicionan de forma decisiva el perfil final de cannabinoides de cada planta. En otras palabras, el CBGA se sitúa en un auténtico cruce metabólico: según qué enzimas predominen, el flujo biosintético se desplazará hacia unas familias cannabinoides u otras. Este punto resulta especialmente importante en genética vegetal, mejora de cultivares y producción controlada de biomasa con fines científicos o industriales (Taura et al., 2007; Zirpel et al., 2018).
En conjunto, el CBGA debe entenderse como una molécula central en tres niveles distintos. Primero, como precursor químico de los principales cannabinoides ácidos del cannabis. Segundo, como pieza clave de la organización biosintética de la planta y de la diversidad entre quimiotipos. Y tercero, como objeto emergente de investigación farmacológica, cuyo estudio todavía se encuentra en una fase comparativamente temprana. Por ello, analizar el CBGA no consiste solo en describir otro cannabinoide más, sino en examinar uno de los puntos de partida fundamentales sobre los que se construye gran parte de la complejidad química y biológica de Cannabis sativa (Gülck & Møller, 2020; Hanuš et al., 2016).
Historia y descubrimiento
El reconocimiento del ácido cannabigerólico (CBGA) como pieza central en la bioquímica del cannabis no fue inmediato, sino el resultado de varias décadas de avances progresivos en química orgánica y análisis de productos naturales. En las primeras etapas del estudio científico del cannabis, durante mediados del siglo XX, la atención se centró principalmente en los cannabinoides neutros, especialmente el Δ9-tetrahidrocannabinol (THC), debido a su relevancia farmacológica y psicoactiva. Sin embargo, estas investigaciones iniciales no reflejaban con precisión la composición química real de la planta fresca, donde predominan las formas ácidas (Mechoulam & Gaoni, 1965; Hanuš et al., 2016).
Fue a partir de los años 60 y 70 cuando comenzó a consolidarse la idea de que los cannabinoides presentes en la planta no eran productos finales, sino intermediarios dentro de rutas biosintéticas más complejas. En este contexto, el CBGA empezó a emerger como una molécula clave, al observarse que compuestos como THCA o CBDA podían generarse a partir de un precursor común. Este cambio de paradigma fue fundamental, ya que desplazó la visión estática de los cannabinoides como sustancias aisladas hacia una comprensión dinámica de la química del cannabis como un sistema metabólico interconectado (Shoyama et al., 1975; Turner et al., 1980).
El verdadero salto conceptual llegó con la identificación de las enzimas responsables de transformar el CBGA en otros cannabinoides ácidos. La caracterización de la THCA sintasa, seguida de la CBDA sintasa y la CBCA sintasa, permitió establecer con claridad que el CBGA actúa como sustrato común en una serie de reacciones oxidativas que generan la diversidad cannabinoide observada en la planta. Este modelo enzimático no solo explicaba la variabilidad química entre diferentes variedades de cannabis, sino que también abría la puerta a estudios genéticos y biotecnológicos más precisos (Taura et al., 1995; Taura et al., 2007).
A medida que mejoraban las técnicas analíticas, especialmente con la introducción de la cromatografía líquida de alta resolución (HPLC), se hizo evidente que el CBGA estaba presente de forma consistente en los tejidos productores de cannabinoides, particularmente en los tricomas glandulares. Estas herramientas permitieron cuantificar con mayor precisión los perfiles cannabinoides sin necesidad de descarboxilar las muestras, lo que resultó clave para distinguir entre formas ácidas y neutras y para confirmar el papel central del CBGA en la planta (De Backer et al., 2009; Hanuš et al., 2016).
En las últimas dos décadas, el estudio del CBGA ha experimentado un nuevo impulso gracias a los avances en genómica, metabolómica y biología sintética. La secuenciación de genes implicados en la biosíntesis cannabinoide y la expresión heteróloga de enzimas en sistemas experimentales han permitido reproducir y estudiar estas rutas fuera de la planta. Esto ha consolidado definitivamente al CBGA como el nodo inicial de la vía biosintética principal de cannabinoides y ha reforzado su interés tanto desde el punto de vista científico como aplicado (Gülck & Møller, 2020; Zirpel et al., 2018).
En conjunto, la historia del CBGA refleja la evolución del conocimiento científico sobre el cannabis: desde una visión centrada en compuestos aislados y sus efectos, hacia un entendimiento sistémico de la planta como una fábrica química compleja. El CBGA, en este sentido, no solo es importante por lo que es, sino por lo que permitió descubrir: la lógica interna que organiza la diversidad de los cannabinoides (Taura et al., 2007; Hanuš et al., 2016).
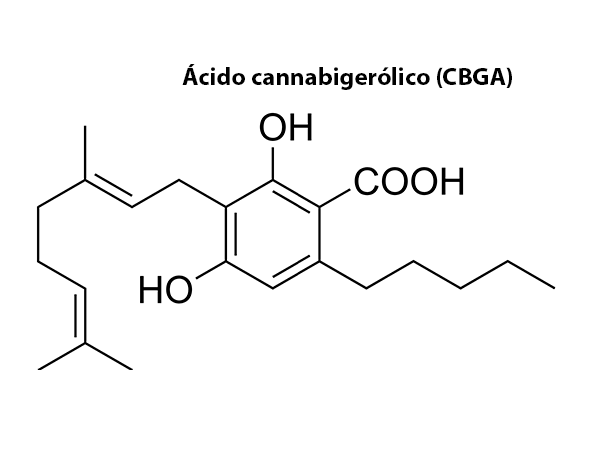
Estructura química
El ácido cannabigerólico (CBGA) es un fitocannabinoide con una estructura híbrida que combina elementos de dos grandes rutas metabólicas vegetales: la vía de los policétidos y la de los terpenoides. Esta dualidad estructural no es un detalle menor, sino una de las claves para entender tanto su origen biosintético como su papel dentro de la química del cannabis. A nivel general, el CBGA está formado por un núcleo fenólico derivado del ácido olivetólico al que se une una cadena lateral prenilada procedente del geranil pirofosfato (GPP), dando lugar a una molécula con propiedades químicas y biológicas características (Fellermeier & Zenk, 1998; Gülck & Møller, 2020).
El esqueleto base del CBGA puede describirse como un sistema aromático resorcinólico sustituido, en el que dos grupos hidroxilo se encuentran en posiciones meta dentro del anillo bencénico. Este patrón es típico de los cannabinoides y contribuye a su capacidad para establecer interacciones mediante enlaces de hidrógeno y fuerzas de Van der Waals con distintas dianas moleculares. Unido a este núcleo aromático aparece una cadena alquílica (pentilo, en la mayoría de los casos), cuya longitud y naturaleza influyen de forma importante en la actividad biológica de los cannabinoides (Hanuš et al., 2016; Pertwee, 2008).
El rasgo diferencial del CBGA frente a su forma neutra (CBG) es la presencia de un grupo carboxilo (-COOH). Este grupo confiere a la molécula un carácter ácido y modifica tanto su polaridad como su estabilidad térmica. Desde un punto de vista químico, el grupo carboxilo puede perderse en forma de dióxido de carbono (CO₂) mediante un proceso de descarboxilación, que transforma el CBGA en cannabigerol (CBG). Este proceso puede ocurrir de forma lenta a temperatura ambiente, pero se acelera significativamente con la exposición al calor, lo que explica por qué en productos procesados predominan las formas neutras (Hanuš et al., 2016; Wang et al., 2016).
Otro elemento clave en la estructura del CBGA es su cadena prenilada, derivada del geranil pirofosfato. Esta porción de la molécula introduce un componente lipofílico importante, favoreciendo su afinidad por membranas biológicas y entornos hidrofóbicos. La combinación de un núcleo fenólico polar y una cadena lipídica apolar convierte al CBGA en una molécula anfipática, capaz de interactuar con diferentes microambientes dentro de sistemas biológicos. Esta característica es compartida por otros cannabinoides y está relacionada con su capacidad para modular proteínas de membrana y canales iónicos (Gülck & Møller, 2020).
Desde una perspectiva tridimensional, el CBGA presenta una cierta flexibilidad conformacional, especialmente en su cadena lateral, lo que le permite adoptar distintas orientaciones espaciales al interactuar con proteínas. Aunque no posee la estructura tricíclica más rígida del THC, esta flexibilidad puede ser relevante en términos de afinidad y selectividad hacia distintas dianas moleculares. La relación entre estructura y función en cannabinoides sigue siendo un campo activo de investigación, donde pequeñas variaciones estructurales pueden dar lugar a cambios significativos en la actividad biológica (Pertwee, 2008; Navarro et al., 2020).
Es importante señalar que el CBGA no presenta aún el cierre de anillo característico de otros cannabinoides como el THCA o el CBDA. Este detalle estructural refleja su condición de precursor biosintético, ya que son precisamente las enzimas sintasas las que catalizan reacciones de ciclación oxidativa a partir del CBGA para generar estructuras más complejas. En este sentido, el CBGA puede considerarse una molécula “abierta” desde el punto de vista estructural, lista para ser transformada en múltiples direcciones dentro de la planta (Taura et al., 2007).
Finalmente, la estructura del CBGA también permite entender su posición dentro de la clasificación de los fitocannabinoides. Al igual que otros cannabinoides, pertenece a la familia de los meroterpenoides, compuestos que resultan de la combinación de una fracción terpenoide con otra de origen no terpénico (en este caso, policétido). Esta categoría refleja su naturaleza biosintética mixta y lo diferencia de otros metabolitos vegetales más homogéneos en su origen (Gülck & Møller, 2020).
En conjunto, la estructura química del CBGA no solo define sus propiedades físico-químicas, sino que anticipa su comportamiento dentro de la planta y su capacidad de transformación en otros cannabinoides. Comprender esta arquitectura molecular es un paso esencial para abordar su biosíntesis, su función biológica y su relevancia en la investigación actual sobre cannabis (Hanuš et al., 2016; Gülck & Møller, 2020).
Biosíntesis en la planta
La biosíntesis del ácido cannabigerólico (CBGA) constituye uno de los procesos más relevantes dentro del metabolismo secundario de Cannabis sativa L., ya que representa el punto de convergencia entre dos grandes rutas metabólicas vegetales: la vía de los policétidos y la vía de los terpenoides. Esta convergencia no solo es esencial desde el punto de vista químico, sino que define la base sobre la cual se construye toda la diversidad de cannabinoides en la planta (Fellermeier & Zenk, 1998; Gülck & Møller, 2020).
El proceso comienza con la formación del ácido olivetólico, un compuesto fenólico que se genera a partir de unidades de malonil-CoA mediante una serie de reacciones catalizadas por enzimas tipo policétido sintasa. Este paso inicial pertenece claramente al metabolismo de los policétidos y da lugar al núcleo aromático que posteriormente formará parte del CBGA. La correcta formación del ácido olivetólico es crítica, ya que determina la base estructural sobre la que se ensamblará el resto de la molécula (Fellermeier & Zenk, 1998).
En paralelo, la planta produce geranil pirofosfato (GPP) a través de la vía de los terpenoides, concretamente mediante la ruta del metileritritol fosfato (MEP) en los plastidios. El GPP es un intermediario clave en la biosíntesis de monoterpenos y actúa como donador de la cadena prenilada que caracteriza a los cannabinoides. Esta molécula aporta la porción lipofílica que, al unirse al ácido olivetólico, dará lugar a la estructura híbrida típica de los fitocannabinoides (Gülck & Møller, 2020; Lange & Ahkami, 2013).
La reacción central que conduce a la formación del CBGA es la prenilación del ácido olivetólico, catalizada por una enzima conocida como geraniltransferasa (también denominada olivetolato geraniltransferasa). Esta enzima facilita la unión del GPP con el ácido olivetólico, dando lugar directamente al CBGA. Este paso es considerado uno de los cuellos de botella de la ruta biosintética, ya que regula en gran medida la cantidad total de cannabinoides que la planta puede producir (Fellermeier & Zenk, 1998; Gülck & Møller, 2020).
Una vez formado, el CBGA actúa como sustrato común para varias enzimas oxidativas específicas, conocidas como sintasas de cannabinoides. Entre ellas destacan la THCA sintasa, la CBDA sintasa y la CBCA sintasa, cada una responsable de transformar el CBGA en su correspondiente cannabinoide ácido mediante reacciones de ciclación oxidativa. Estas enzimas no compiten de forma aleatoria, sino que su expresión genética y actividad relativa determinan el perfil final de cannabinoides de cada planta o quimiotipo (Taura et al., 2007; Zirpel et al., 2018).
Este punto es clave: el CBGA no se acumula en grandes cantidades en la mayoría de las variedades de cannabis porque es rápidamente transformado por estas sintasas. Solo en determinadas condiciones —como en cultivares específicos o en mutaciones donde estas enzimas tienen baja actividad— puede observarse una acumulación significativa de CBGA. Esto explica la existencia de variedades denominadas “CBG-dominantes”, en las que el flujo metabólico se queda bloqueado en este punto (Zirpel et al., 2018).
Desde una perspectiva celular, la biosíntesis del CBGA tiene lugar principalmente en los tricomas glandulares, estructuras especializadas que funcionan como verdaderas fábricas bioquímicas. Dentro de estos tricomas, los precursores, enzimas y productos se organizan de manera altamente coordinada, lo que permite una producción eficiente y localizada de cannabinoides. Esta compartimentalización también protege a la planta de posibles efectos tóxicos de estos compuestos (Livingston et al., 2020).
Además, la regulación de esta ruta biosintética está influida por múltiples factores, incluyendo la genética de la planta, las condiciones ambientales (luz, temperatura, nutrientes) y el estado de desarrollo. La expresión de las enzimas clave, como las sintasas, puede variar significativamente, lo que se traduce en diferencias notables en la producción de cannabinoides incluso entre plantas genéticamente similares (Gülck & Møller, 2020).
En conjunto, la biosíntesis del CBGA representa el núcleo funcional del metabolismo cannabinoide. Es en este punto donde convergen las rutas metabólicas y donde se decide, en gran medida, la identidad química final de la planta. Por ello, el CBGA no solo es el precursor de los principales cannabinoides, sino también el verdadero nodo de control que define la diversidad química del cannabis (Taura et al., 2007; Gülck & Møller, 2020).
Distribución y acumulación en la planta
El ácido cannabigerólico (CBGA) se localiza principalmente en los tricomas glandulares de Cannabis sativa L., estructuras epidérmicas especializadas que actúan como centros de síntesis, secreción y acumulación de metabolitos secundarios. Estos tricomas, especialmente los de tipo capitado-pedunculado, son los responsables de la producción de cannabinoides y terpenos, y constituyen el microambiente donde se concentra la maquinaria enzimática implicada en la biosíntesis del CBGA (Livingston et al., 2020; Happyana et al., 2013).
Dentro de los tricomas, el CBGA no se distribuye de manera uniforme, sino que se acumula en la cavidad subcuticular, un espacio extracelular formado entre la pared celular y la cutícula. Esta cavidad actúa como reservorio donde se depositan los cannabinoides en forma ácida, evitando su acumulación directa en el citoplasma celular, lo que podría resultar potencialmente tóxico. Este sistema de secreción y almacenamiento refleja un alto grado de especialización celular en la planta (Sirikantaramas et al., 2005; Livingston et al., 2020).
La distribución del CBGA a nivel macroscópico no es homogénea en toda la planta. Las mayores concentraciones se encuentran en las inflorescencias femeninas, particularmente en las brácteas que rodean las flores, donde la densidad de tricomas es significativamente más alta. En contraste, otras partes de la planta como tallos, hojas grandes (hojas de abanico) o raíces presentan niveles mucho más bajos o prácticamente insignificantes de CBGA (Happyana et al., 2013; Gülck & Møller, 2020).
Las hojas cercanas a las flores (hojas de azúcar) pueden contener cantidades apreciables de CBGA debido a la presencia de tricomas, aunque generalmente en menor proporción que las inflorescencias. Esta distribución diferencial tiene implicaciones tanto ecológicas como prácticas, ya que determina qué partes de la planta son más relevantes desde el punto de vista fitoquímico y de extracción (Happyana et al., 2013).
Desde una perspectiva temporal, la acumulación de CBGA está estrechamente ligada al estado de desarrollo de la planta. Durante las primeras fases de la floración, el CBGA puede detectarse en niveles relativamente altos como intermediario biosintético. Sin embargo, a medida que la planta madura, este compuesto tiende a ser rápidamente convertido en otros cannabinoides ácidos, lo que reduce su concentración relativa en etapas más avanzadas. Este patrón refleja su papel como precursor más que como producto final (Taura et al., 2007; Zirpel et al., 2018).
En ciertos quimiotipos o variedades específicas, especialmente aquellas seleccionadas por su contenido en CBG, la acumulación de CBGA puede ser más elevada debido a una menor actividad de las enzimas sintasas que lo transforman. En estos casos, el CBGA no es completamente metabolizado hacia THCA, CBDA o CBCA, lo que permite su detección en mayores concentraciones. Este fenómeno es de especial interés en programas de mejora genética y en la producción de extractos con perfiles cannabinoides específicos (Zirpel et al., 2018).
A nivel subcelular, la biosíntesis del CBGA implica la interacción de compartimentos como los plastidios (donde se genera el GPP) y el citosol (donde se forma el ácido olivetólico), lo que requiere una coordinación metabólica precisa. Una vez sintetizado, el CBGA es transportado hacia la cavidad subcuticular, donde queda almacenado junto a otros cannabinoides y terpenos, contribuyendo a la composición final de la resina (Gülck & Møller, 2020).
Además, factores ambientales como la intensidad lumínica, la temperatura, el estrés biótico y abiótico o la disponibilidad de nutrientes pueden influir en la producción y acumulación de CBGA. Aunque estos efectos no son exclusivos de este cannabinoide, sí afectan al flujo metabólico general de la planta, alterando indirectamente su concentración relativa (Lange & Ahkami, 2013).
En conjunto, la distribución del CBGA en la planta refleja su papel como intermediario biosintético clave y su dependencia de estructuras especializadas como los tricomas glandulares. Su localización específica, tanto a nivel tisular como celular, no solo permite entender cómo la planta gestiona la producción de cannabinoides, sino también por qué determinadas partes del cannabis concentran la mayor parte de su actividad química (Livingston et al., 2020; Gülck & Møller, 2020).
Mecanismos moleculares
El ácido cannabigerólico (CBGA), aunque históricamente considerado principalmente como un intermediario biosintético, ha mostrado en estudios preclínicos la capacidad de interactuar con diversas dianas moleculares más allá de los receptores cannabinoides clásicos. Estas interacciones sugieren que el CBGA puede modular procesos celulares complejos a través de múltiples mecanismos, aunque la evidencia disponible sigue siendo limitada y en muchos casos dependiente de modelos experimentales in vitro o animales (Navarro et al., 2020; Borrelli et al., 2013).
A diferencia de otros fitocannabinoides como el THC o el CBD, el CBGA presenta una afinidad baja o moderada por los receptores CB1 y CB2, lo que indica que su actividad no se explica principalmente a través del sistema endocannabinoide clásico. En su lugar, el CBGA parece actuar sobre un conjunto más amplio de proteínas, incluyendo canales iónicos, receptores nucleares y enzimas implicadas en la señalización celular (Pertwee, 2008; Navarro et al., 2020).
Uno de los grupos de dianas más relevantes en el estudio del CBGA son los canales TRP (Transient Receptor Potential). En particular, se ha observado que el CBGA puede interactuar con subtipos como TRPV1, TRPA1 y TRPM8, que están implicados en la detección de estímulos térmicos, químicos y nociceptivos. Estas interacciones sugieren que el CBGA podría modular la excitabilidad neuronal y la percepción sensorial, aunque los mecanismos exactos y su relevancia fisiológica aún no están completamente definidos (De Petrocellis et al., 2011; Cascio et al., 2010).
Además de los canales TRP, el CBGA ha mostrado capacidad para interactuar con receptores nucleares de la familia PPAR (Peroxisome Proliferator-Activated Receptors), especialmente PPARα y PPARγ. Estos receptores actúan como factores de transcripción que regulan la expresión génica relacionada con el metabolismo lipídico, la inflamación y la homeostasis energética. La activación de PPARs por cannabinoides ácidos sugiere un posible mecanismo indirecto mediante el cual estas moléculas podrían influir en procesos metabólicos y celulares a largo plazo (O’Sullivan, 2016; Borrelli et al., 2013).
Otro aspecto relevante es la posible interacción del CBGA con enzimas implicadas en la degradación de endocannabinoides, como la FAAH (fatty acid amide hydrolase). Aunque la evidencia es menos consistente que en el caso de otros cannabinoides, algunos estudios sugieren que el CBGA podría modular la actividad de estas enzimas, alterando indirectamente los niveles de endocannabinoides como la anandamida. Este tipo de mecanismo, conocido como modulación “indirecta”, es característico de varios fitocannabinoides (Pertwee, 2008; Navarro et al., 2020).
El CBGA también ha mostrado actividad en modelos relacionados con la señalización inflamatoria, donde podría influir en la producción de mediadores proinflamatorios a través de rutas como NF-κB o la modulación de citoquinas. Sin embargo, estos efectos deben interpretarse con cautela, ya que dependen en gran medida del contexto experimental y no pueden extrapolarse directamente a sistemas fisiológicos complejos sin evidencia adicional (Borrelli et al., 2013; Navarro et al., 2020).
Desde un punto de vista fisicoquímico, la estructura anfipática del CBGA —con un núcleo fenólico polar y una cadena lipofílica— le permite interactuar con membranas biológicas, lo que puede alterar propiedades como la fluidez o la organización de microdominios lipídicos. Este tipo de interacción no específica también puede influir en la función de proteínas de membrana, contribuyendo a efectos celulares indirectos difíciles de atribuir a una única diana molecular (Gülck & Møller, 2020).
Es importante destacar que muchos de estos mecanismos no son exclusivos del CBGA, sino que se solapan con los observados en otros cannabinoides. Sin embargo, pequeñas diferencias estructurales —como la presencia del grupo carboxilo— pueden modificar de forma significativa la afinidad y eficacia en distintas dianas, lo que convierte al CBGA en un compuesto con un perfil farmacológico propio, aún en proceso de caracterización (Hanuš et al., 2016).
En conjunto, el CBGA puede entenderse como un modulador molecular multidiana, cuya actividad no se limita al sistema endocannabinoide clásico, sino que se extiende a canales iónicos, receptores nucleares y enzimas clave en la señalización celular. No obstante, la mayoría de estos hallazgos se encuentran en fases preliminares, por lo que su relevancia fisiológica y su posible aplicación en contextos clínicos requieren aún una investigación más profunda y sistemática (Navarro et al., 2020; O’Sullivan, 2016).
Interacción con el sistema endocannabinoide
El ácido cannabigerólico (CBGA) presenta una interacción con el sistema endocannabinoide (SEC) que puede considerarse indirecta y de baja afinidad en comparación con otros fitocannabinoides más estudiados. A diferencia del Δ9-THC, que actúa como agonista parcial de los receptores CB1 y CB2, el CBGA no muestra una actividad significativa sobre estos receptores en condiciones fisiológicas, lo que sugiere que su perfil de acción dentro del SEC es más sutil y menos dependiente de la activación directa de estas dianas (Pertwee, 2008; Navarro et al., 2020).
Los estudios disponibles indican que el CBGA puede comportarse como un ligando débil o modulador de los receptores cannabinoides, con afinidades relativamente bajas en ensayos in vitro. Esto implica que, aunque puede interactuar con CB1 y CB2, es poco probable que estos receptores constituyan su principal vía de acción. Esta característica lo sitúa dentro del grupo de cannabinoides con actividad “no clásica”, cuya influencia sobre el SEC se produce a través de mecanismos indirectos o complementarios (Pertwee, 2008).
Una de las posibles vías de interacción indirecta del CBGA con el sistema endocannabinoide es la modulación del metabolismo de los endocannabinoides. En particular, se ha sugerido que podría influir sobre enzimas como la FAAH, responsable de la degradación de la anandamida (AEA), o la MAGL, implicada en el catabolismo del 2-AG. Aunque la evidencia es todavía limitada y en algunos casos contradictoria, este tipo de interacción podría alterar los niveles endógenos de ligandos cannabinoides, modulando así la señalización del SEC sin necesidad de activar directamente sus receptores (Navarro et al., 2020; Pertwee, 2008).
Además, la actividad del CBGA sobre canales TRP y otros sistemas de señalización puede generar efectos que se solapan funcionalmente con los del sistema endocannabinoide. Por ejemplo, la modulación de TRPV1 o TRPA1, implicados en procesos sensoriales y nociceptivos, puede interactuar de forma indirecta con rutas donde también participan los endocannabinoides. Esta interconexión refleja la naturaleza integrada de las redes de señalización celular, donde múltiples sistemas convergen y se regulan mutuamente (De Petrocellis et al., 2011; Cascio et al., 2010).
Otra dimensión relevante es la posible interacción del CBGA con receptores nucleares como PPARα y PPARγ, que, aunque no forman parte del sistema endocannabinoide clásico, están funcionalmente relacionados con él. Los endocannabinoides pueden activar estos receptores, y algunos fitocannabinoides, incluido el CBGA, parecen compartir esta capacidad. Esto amplía el concepto de “sistema endocannabinoide ampliado” o endocannabinoidome, donde se incluyen múltiples dianas moleculares más allá de CB1 y CB2 (O’Sullivan, 2016).
Desde una perspectiva más amplia, el CBGA puede considerarse un modulador del SEC en un sentido ecosistémico, más que como un ligando directo. Su capacidad para influir en enzimas, canales iónicos y receptores asociados contribuye a modificar el entorno en el que opera el sistema endocannabinoide, afectando potencialmente a la intensidad, duración y contexto de la señalización endocannabinoide (Navarro et al., 2020).
Es importante subrayar que gran parte de la evidencia disponible sobre la interacción del CBGA con el SEC procede de estudios preclínicos, y que su relevancia fisiológica en humanos aún no está completamente establecida. Por ello, cualquier interpretación debe realizarse con cautela, evitando extrapolaciones directas a contextos clínicos sin respaldo experimental suficiente (Hanuš et al., 2016).
En conjunto, la relación del CBGA con el sistema endocannabinoide se caracteriza por una baja actividad directa sobre CB1/CB2 y una posible modulación indirecta a través de enzimas, canales iónicos y receptores relacionados. Este perfil lo sitúa dentro de una categoría de fitocannabinoides que, más que activar el sistema de forma directa, parecen influir en su regulación global y en su interacción con otros sistemas de señalización celular (Pertwee, 2008; O’Sullivan, 2016).
Importancia en investigación
El ácido cannabigerólico (CBGA) ha pasado en las últimas décadas de ser considerado un simple intermediario biosintético a convertirse en un objeto de estudio con interés propio dentro de la investigación en cannabinoides. Aunque su papel como precursor de otros fitocannabinoides sigue siendo su característica más conocida, el desarrollo de nuevas herramientas analíticas y biotecnológicas ha permitido explorar con mayor profundidad sus propiedades químicas, biológicas y potenciales aplicaciones (Gülck & Møller, 2020; Hanuš et al., 2016).
Uno de los principales focos de investigación en torno al CBGA es su función como nodo central en la biosíntesis cannabinoide. Comprender cómo se regula su producción y conversión en otros cannabinoides permite no solo explicar la diversidad química del cannabis, sino también intervenir en ella mediante técnicas de mejora genética o biología sintética. En este contexto, el CBGA se sitúa como una diana estratégica para optimizar cultivos con perfiles cannabinoides específicos, lo que tiene implicaciones tanto científicas como industriales (Zirpel et al., 2018; Gülck & Møller, 2020).
Además, el estudio del CBGA ha cobrado relevancia en el ámbito de la biotecnología vegetal y microbiana, donde se han desarrollado sistemas capaces de producir cannabinoides fuera de la planta mediante la expresión heteróloga de enzimas clave. En estos modelos, el CBGA suele representar el punto de partida de la ruta biosintética, lo que refuerza su papel como molécula central en la ingeniería de cannabinoides. Este enfoque abre la puerta a la producción controlada de compuestos específicos sin depender directamente del cultivo de cannabis (Gülck & Møller, 2020).
Desde el punto de vista farmacológico, el interés por el CBGA ha aumentado debido a su perfil como modulador multidiana. Aunque la mayor parte de la evidencia sigue siendo preclínica, los estudios disponibles han explorado su interacción con canales iónicos, receptores nucleares y rutas de señalización celular relacionadas con procesos como la inflamación, el metabolismo o la excitabilidad neuronal. Sin embargo, este campo se encuentra aún en una fase temprana, y es necesario avanzar hacia modelos más complejos y estudios clínicos para determinar su relevancia fisiológica real (Navarro et al., 2020; Borrelli et al., 2013).
Otro aspecto importante es el papel del CBGA en la comprensión del endocannabinoidome, un concepto que amplía el sistema endocannabinoide clásico para incluir un conjunto más amplio de mediadores lipídicos, enzimas y dianas moleculares. El hecho de que el CBGA interactúe con múltiples sistemas sugiere que su estudio puede contribuir a una visión más integrada de la señalización celular, más allá de los receptores CB1 y CB2 (O’Sullivan, 2016).
El CBGA también ha despertado interés en el ámbito de la química medicinal, donde se investiga su estructura como base para el desarrollo de nuevos compuestos. La presencia del grupo carboxilo y su estructura relativamente flexible ofrecen oportunidades para modificaciones químicas que podrían dar lugar a derivados con propiedades farmacológicas diferenciadas. En este sentido, el CBGA no solo es relevante como molécula natural, sino también como punto de partida para el diseño de nuevas entidades químicas (Hanuš et al., 2016).
A nivel metodológico, el estudio del CBGA ha contribuido a mejorar las técnicas de análisis de cannabinoides, especialmente en lo que respecta a la diferenciación entre formas ácidas y neutras. La utilización de métodos como la HPLC ha permitido analizar muestras sin inducir descarboxilación, lo que ha sido clave para entender la composición real de la planta y el papel de compuestos como el CBGA en su estado nativo (De Backer et al., 2009).
En el contexto actual, el CBGA representa un punto de convergencia entre varias áreas de investigación: la botánica, la bioquímica, la farmacología y la biotecnología. Su estudio no solo aporta información sobre un compuesto específico, sino que permite entender mejor la organización metabólica del cannabis y su potencial como sistema químico complejo (Gülck & Møller, 2020).
En conjunto, la importancia del CBGA en investigación radica en su doble condición: por un lado, como precursor fundamental en la biosíntesis de cannabinoides, y por otro, como molécula emergente con actividad propia en diversos sistemas biológicos. Esta combinación lo convierte en una pieza clave para avanzar en el conocimiento del cannabis desde una perspectiva científica rigurosa y multidisciplinar (Hanuš et al., 2016; Navarro et al., 2020).
Referencias
- Borrelli, F., Fasolino, I., Romano, B., Capasso, R., Maiello, F., Coppola, D., Orlando, P., Battista, G., Pagano, E., Di Marzo, V., & Izzo, A. A. (2013). Beneficial effect of the non-psychotropic plant cannabinoid cannabigerol on experimental inflammatory bowel disease. Biochemical Pharmacology, 85(9), 1306–1316. - Cascio, M. G., Gauson, L. A., Stevenson, L. A., Ross, R. A., & Pertwee, R. G. (2010). Evidence that the plant cannabinoid cannabigerol is a highly potent α2-adrenoceptor agonist and moderately potent 5HT1A receptor antagonist. British Journal of Pharmacology, 159(1), 129–141. - De Backer, B., Debrus, B., Lebrun, P., Theunis, L., Dubois, N., Decock, L., Verstraete, A., Hubert, P., & Charlier, C. (2009). Innovative development and validation of an HPLC/DAD method for the qualitative and quantitative determination of major cannabinoids in cannabis plant material. Journal of Chromatography B, 877(32), 4115–4124. - De Petrocellis, L., Ligresti, A., Moriello, A. S., Allarà, M., Bisogno, T., Petrosino, S., Stott, C. G., & Di Marzo, V. (2011). Effects of cannabinoids and cannabinoid-enriched Cannabis extracts on TRP channels and endocannabinoid metabolic enzymes. British Journal of Pharmacology, 163(7), 1479–1494. - Fellermeier, M., & Zenk, M. H. (1998). Prenylation of olivetolate by a hemp transferase yields cannabigerolic acid, the precursor of tetrahydrocannabinol. FEBS Letters, 427(2), 283–285. - Gülck, T., & Møller, B. L. (2020). Phytocannabinoids: Origins and biosynthesis. Trends in Plant Science, 25(10), 985–1004. - Hanuš, L. O., Meyer, S. M., Muñoz, E., Taglialatela-Scafati, O., & Appendino, G. (2016). Phytocannabinoids: A unified critical inventory. Natural Product Reports, 33(12), 1357–1392. - Happyana, N., Agnolet, S., Muntendam, R., van Dam, A., Schneider, B., & Kayser, O. (2013). Analysis of cannabinoids in laser-microdissected trichomes of Cannabis sativa using LCMS and cryogenic NMR. Phytochemistry, 87, 51–59. - Lange, B. M., & Ahkami, A. (2013). Metabolic engineering of plant monoterpenes, sesquiterpenes and diterpenes—current status and future opportunities. Plant Biotechnology Journal, 11(2), 169–196. - Livingston, S. J., Quilichini, T. D., Booth, J. K., Wong, D. C. J., Rensing, K. H., Laflamme-Yonkman, J., Castellarin, S. D., Bohlmann, J., & Page, J. E. (2020). Cannabis glandular trichomes alter morphology and metabolite content during flower maturation. The Plant Journal, 101(1), 37–56. - Navarro, G., Varani, K., Reyes-Resina, I., Sánchez de Medina, V., Rivas-Santisteban, R., Sánchez-Carnerero, C., Vincenzi, F., Casano, S., Ferreiro-Vera, C., Canela, E. I., Franco, R., & - - Martínez-Pinilla, E. (2020). Cannabigerol action at cannabinoid CB1 and CB2 receptors and at CB1–CB2 heteroreceptor complexes. Frontiers in Pharmacology, 11, 102. - O’Sullivan, S. E. (2016). An update on PPAR activation by cannabinoids. British Journal of Pharmacology, 173(12), 1899–1910. - Pertwee, R. G. (2008). The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids. British Journal of Pharmacology, 153(2), 199–215. - Sirikantaramas, S., Taura, F., Morimoto, S., & Shoyama, Y. (2005). Recent advances in Cannabis sativa research: Biosynthesis of phytocannabinoids and their regulatory mechanisms. Plant Biotechnology, 22(3), 231–240. - Taura, F., Morimoto, S., & Shoyama, Y. (1995). Purification and characterization of cannabidiolic-acid synthase from Cannabis sativa L. Journal of Biological Chemistry, 270(35), 21462–21467. - Taura, F., Sirikantaramas, S., Shoyama, Y., Yoshikai, K., Shoyama, Y., & Morimoto, S. (2007). Cannabidiolic-acid synthase, the chemotype-determining enzyme in the fiber-type Cannabis sativa. FEBS Letters, 581(16), 2929–2934. - Turner, C. E., Elsohly, M. A., & Boeren, E. G. (1980). Constituents of Cannabis sativa L. XVII. A review of the natural constituents. Journal of Natural Products, 43(2), 169–234. - Wang, M., Wang, Y. H., Avula, B., Radwan, M. M., Wanas, A. S., van Antwerp, J., Parcher, J. F., ElSohly, M. A., & Khan, I. A. (2016). Decarboxylation study of acidic cannabinoids: A novel approach using ultra-high-performance supercritical fluid chromatography/photodiode array-mass spectrometry. Cannabis and Cannabinoid Research, 1(1), 262–271. - Zirpel, B., Degenhardt, F., Martin, C., Kayser, O., & Stehle, F. (2018). Engineering yeast for the production of cannabinoids. Biotechnology Letters, 40(7), 1031–1040.