Introducción
Los tricomas glandulares son estructuras epidérmicas secretoras especializadas que recubren distintas superficies aéreas de Cannabis sativa, especialmente las flores femeninas y, en menor medida, hojas bracteales y tejidos jóvenes. Desde el punto de vista botánico, no representan una simple característica superficial, sino microórganos altamente diferenciados cuya función principal es la síntesis, acumulación y secreción de metabolitos secundarios, incluyendo fitocannabinoides y terpenos. En este contexto, el tricoma glandular constituye la unidad funcional donde se materializa gran parte de la química característica del cannabis. (Happyana et al., 2013; Livingston et al., 2020)
En el caso del cannabis, el interés científico por los tricomas glandulares es particularmente elevado debido a su papel como principal sitio de acumulación de compuestos bioactivos. Estudios recientes han demostrado que estas estructuras no son compartimentos pasivos, sino sistemas celulares dinámicos con una organización interna altamente especializada, adaptada a la producción y almacenamiento de metabolitos lipofílicos. Este enfoque ha sido reforzado por análisis mediante microscopía avanzada, transcriptómica y proteómica, que evidencian una regulación metabólica activa dentro del tricoma. (Gülck & Møller, 2020; Livingston et al., 2020)
Desde una perspectiva bioquímica, los tricomas glandulares concentran la maquinaria enzimática implicada en la biosíntesis de cannabinoides y terpenos. En estas estructuras convergen rutas metabólicas fundamentales como la vía del mevalonato (MVA) y la vía del metileritritol fosfato (MEP), responsables de la generación de precursores isoprenoides. A partir de estos, se forman monoterpenos, sesquiterpenos y cannabinoides prenilados, estableciendo al tricoma como punto de integración entre metabolismo primario y secundario. (Booth et al., 2017; Gülck & Møller, 2020)
Además de su función biosintética, los tricomas glandulares cumplen un papel relevante en la ecología de la planta. La secreción resinosa puede actuar como mecanismo de defensa frente a herbívoros, radiación ultravioleta, desecación y estrés ambiental, además de influir en interacciones con microorganismos e insectos. En cannabis, esta función se manifiesta especialmente en los órganos reproductivos femeninos, donde la protección del tejido floral adquiere un valor adaptativo clave. (Werker, 2000; Livingston et al., 2020)
A nivel morfológico, los tricomas glandulares de Cannabis sativa presentan distintos tipos estructurales, principalmente bulbosos, sésiles y capitados pedunculados. Cada uno de ellos muestra diferencias en tamaño, arquitectura y capacidad secretora, siendo los tricomas capitados pedunculados los más relevantes en la acumulación de cannabinoides en flores maduras. Esta clasificación permite relacionar la estructura del tricoma con su función metabólica y su distribución en la planta. (Kim & Mahlberg, 1997; Sirikantaramas et al., 2005)
Dentro del marco de Tantrum Knowledge, los tricomas glandulares ocupan una posición estratégica al conectar la biología vegetal con la farmacología de los fitocannabinoides. Aunque el sistema endocannabinoide pertenece a organismos animales, los compuestos que interactúan con él tienen su origen en estas estructuras vegetales. Por tanto, comprender los tricomas no implica únicamente identificar el lugar de producción de cannabinoides, sino entender la base biológica que permite su existencia. (Di Marzo, 1998; Booth et al., 2017)
Finalmente, los tricomas glandulares representan un modelo de especialización celular dentro de la biología vegetal. La capacidad de producir y almacenar metabolitos potencialmente reactivos sin comprometer la integridad celular sugiere la existencia de mecanismos avanzados de compartimentalización y secreción. Este aspecto ha convertido a los tricomas en un objeto de estudio relevante no solo en cannabis, sino en el contexto más amplio del metabolismo secundario en plantas. (Gülck & Møller, 2020; Livingston et al., 2020)
Historia del descubrimiento
El estudio de los tricomas en plantas tiene sus raíces en la botánica clásica del siglo XIX, donde estas estructuras fueron inicialmente descritas desde un enfoque morfológico como extensiones epidérmicas con posibles funciones protectoras. En este contexto temprano, los tricomas se clasificaban principalmente en función de su forma (glandulares vs no glandulares) y su distribución en la superficie vegetal, sin que se comprendiera todavía su papel en la síntesis de metabolitos especializados. (Werker, 2000)
A lo largo del siglo XX, el avance en técnicas de microscopía óptica y posteriormente electrónica permitió una caracterización más detallada de los tricomas glandulares, revelando su organización celular interna y su capacidad secretora. En diversas especies vegetales, estos estudios comenzaron a asociar los tricomas con la producción de compuestos secundarios como aceites esenciales, resinas y metabolitos defensivos. Este cambio de paradigma marcó el paso de una visión puramente estructural a una interpretación funcional de estas estructuras. (Fahn, 2000; Werker, 2000)
En el caso específico del cannabis, el interés científico por los tricomas glandulares se intensificó significativamente tras el aislamiento de los principales fitocannabinoides en la segunda mitad del siglo XX. El trabajo pionero de Raphael Mechoulam y colaboradores en la década de 1960, que permitió la identificación estructural del Δ9-tetrahidrocannabinol (THC), generó nuevas preguntas sobre el origen biosintético de estos compuestos dentro de la planta. Este punto marcó el inicio de una investigación más dirigida hacia la localización anatómica de la producción de cannabinoides. (Mechoulam & Gaoni, 1964)
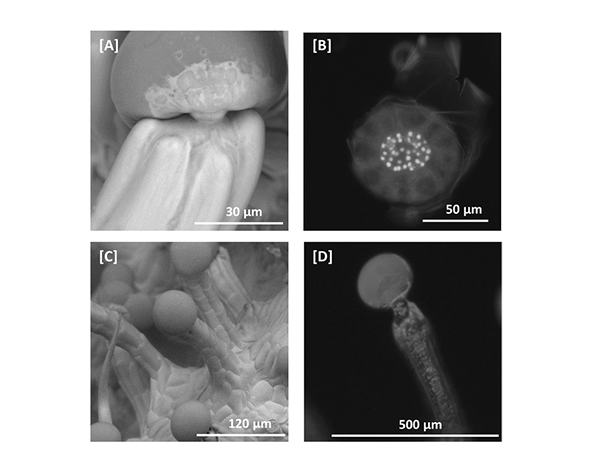
Durante las décadas siguientes, estudios mediante microscopía electrónica de barrido y transmisión permitieron observar con mayor precisión los tricomas glandulares de Cannabis sativa, especialmente los tricomas capitados presentes en flores femeninas. Estos trabajos demostraron que la resina rica en cannabinoides no se encontraba distribuida de forma homogénea en los tejidos vegetales, sino acumulada en cavidades subcuticulares formadas por la separación de la cutícula en la cabeza del tricoma. Este hallazgo fue clave para entender la organización espacial de la secreción. (Kim & Mahlberg, 1997)
A finales del siglo XX y principios del XXI, el desarrollo de técnicas bioquímicas y moleculares permitió avanzar en la comprensión del metabolismo asociado a los tricomas. Se identificaron enzimas clave implicadas en la biosíntesis de cannabinoides, como la THCA sintasa y la CBDA sintasa, cuya expresión se localiza predominantemente en células del tricoma glandular. Este avance consolidó la idea de que estas estructuras no solo almacenan, sino que también participan activamente en la producción de metabolitos. (Sirikantaramas et al., 2005; Taura et al., 2007)
Más recientemente, la integración de enfoques transcriptómicos, proteómicos y metabolómicos ha permitido caracterizar los tricomas glandulares como sistemas altamente regulados, con perfiles de expresión génica específicos y diferenciados respecto a otros tejidos de la planta. Estos estudios han demostrado que los tricomas representan unidades metabólicas especializadas con una regulación coordinada de rutas biosintéticas complejas, lo que refuerza su papel como centros de producción de metabolitos secundarios. (Booth et al., 2017; Gülck & Møller, 2020)
En paralelo, la investigación moderna ha ampliado el interés por los tricomas más allá del cannabis, utilizándolos como modelo para estudiar la compartimentalización metabólica, la secreción extracelular y la evolución de estructuras especializadas en plantas. En este sentido, los tricomas glandulares de Cannabis sativa se han convertido en un sistema de referencia para comprender cómo las plantas organizan espacialmente la producción de compuestos complejos, especialmente aquellos con funciones ecológicas y farmacológicas relevantes. (Livingston et al., 2020)
Estructura y tipos de tricomas glandulares
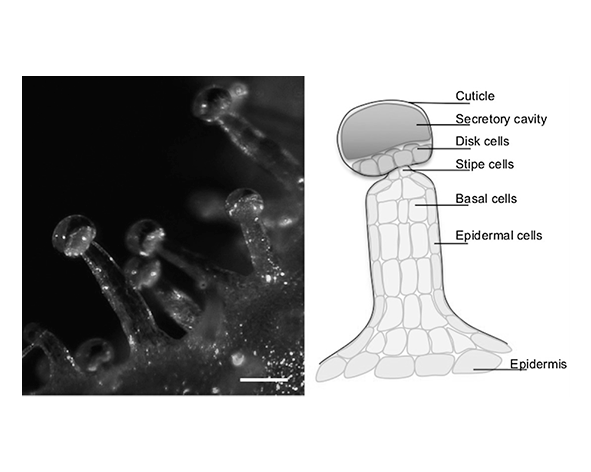
Los tricomas glandulares de Cannabis sativa presentan una organización morfológica compleja que refleja su función como estructuras secretoras especializadas. Desde un punto de vista anatómico, estos tricomas están formados por varias regiones diferenciadas: una célula basal, un tallo (cuando está presente) y una cabeza glandular compuesta por células secretoras. Esta arquitectura permite la síntesis intracelular de metabolitos y su posterior acumulación en una cavidad extracelular delimitada por la cutícula. (Kim & Mahlberg, 1997; Livingston et al., 2020)
La célula basal se encuentra anclada en la epidermis de la planta y actúa como punto de conexión estructural entre el tricoma y el tejido vegetal subyacente. Aunque su papel metabólico es menos activo que el de las células secretoras, participa en el soporte fisiológico del tricoma, facilitando el intercambio de nutrientes y precursores necesarios para la biosíntesis de compuestos. (Werker, 2000)
Por encima de la célula basal se sitúa el tallo, cuya longitud varía dependiendo del tipo de tricoma. En tricomas sésiles, el tallo es prácticamente inexistente, mientras que en tricomas capitados pedunculados puede estar formado por varias células alargadas que elevan la cabeza glandular por encima de la superficie de la planta. Esta elevación no es casual, ya que puede favorecer la dispersión de compuestos volátiles y mejorar la interacción con el entorno. (Livingston et al., 2020)
La cabeza glandular constituye la región más relevante desde el punto de vista funcional. Está formada por un conjunto de células secretoras dispuestas en forma de disco, responsables de la síntesis de cannabinoides y terpenos. Estas células presentan una alta densidad de orgánulos asociados al metabolismo secundario, incluyendo plastidios modificados y retículo endoplasmático desarrollado, lo que refleja su intensa actividad biosintética. (Sirikantaramas et al., 2005; Gülck & Møller, 2020)
Uno de los aspectos más característicos de los tricomas glandulares es la formación de una cavidad subcuticular en la cabeza del tricoma. Durante el proceso de secreción, la cutícula se separa de la pared celular, generando un espacio donde se acumula la resina rica en cannabinoides y terpenos. Este mecanismo permite almacenar compuestos lipofílicos fuera del citoplasma, evitando su acumulación intracelular potencialmente tóxica. (Kim & Mahlberg, 1997)
En Cannabis sativa, se describen generalmente tres tipos principales de tricomas glandulares: bulbosos, sésiles y capitados pedunculados. Los tricomas bulbosos son los más pequeños y simples, con una estructura reducida y menor capacidad secretora. Se distribuyen ampliamente en la planta, pero su contribución a la producción total de cannabinoides es limitada. (Werker, 2000)
Los tricomas sésiles presentan una cabeza glandular más desarrollada, pero carecen de un tallo prominente. Se encuentran principalmente en hojas y tejidos vegetativos, y aunque participan en la producción de metabolitos, su capacidad es inferior a la de los tricomas más especializados. Su estructura sugiere una función intermedia entre defensa y secreción metabólica. (Livingston et al., 2020)
Los tricomas capitados pedunculados representan el tipo más complejo y relevante en términos de producción de cannabinoides. Están formados por un tallo multicelular y una cabeza glandular bien desarrollada, donde se produce la mayor parte de la resina acumulada en flores femeninas maduras. Este tipo de tricoma es el principal responsable del perfil químico del cannabis, lo que explica su importancia tanto en investigación como en aplicaciones agronómicas. (Kim & Mahlberg, 1997; Booth et al., 2017)
La diferenciación entre estos tipos de tricomas no es únicamente morfológica, sino también funcional. Existen diferencias en la expresión génica, la actividad enzimática y la capacidad de acumulación de metabolitos, lo que sugiere una especialización progresiva dentro de la planta. Esta variabilidad permite a Cannabis sativa modular su producción química en función del tejido, el estadio de desarrollo y las condiciones ambientales. (Gülck & Møller, 2020)
En conjunto, la estructura de los tricomas glandulares refleja una adaptación evolutiva altamente eficiente para la producción y almacenamiento de metabolitos secundarios. Su organización multicelular, junto con la formación de cavidades subcuticulares, permite a la planta generar grandes cantidades de compuestos bioactivos sin comprometer la integridad celular, consolidando a estas estructuras como el núcleo funcional del metabolismo especializado en cannabis. (Livingston et al., 2020)
Mecanismos moleculares y biosíntesis en tricomas glandulares
Los tricomas glandulares de Cannabis sativa funcionan como unidades metabólicas altamente especializadas en las que convergen múltiples rutas biosintéticas responsables de la producción de fitocannabinoides y terpenos. Estas estructuras presentan una organización celular optimizada para integrar metabolismo primario y secundario, permitiendo la conversión eficiente de precursores básicos en metabolitos complejos característicos de la planta. (Booth et al., 2017; Gülck & Møller, 2020)
El proceso biosintético comienza con la generación de unidades isoprenoides fundamentales, concretamente isopentenil pirofosfato (IPP) y dimetilalil pirofosfato (DMAPP). Estas moléculas se producen a través de dos rutas metabólicas independientes pero complementarias: la vía del mevalonato (MVA), localizada en el citosol, y la vía del metileritritol fosfato (MEP), localizada en los plastidios. Ambas rutas contribuyen al pool de precursores necesarios para la síntesis de terpenos y cannabinoides. (Lichtenthaler, 1999; Booth et al., 2017)
A partir de IPP y DMAPP se forman intermediarios clave como el geranil pirofosfato (GPP) y el farnesil pirofosfato (FPP). El GPP actúa como precursor de monoterpenos, mientras que el FPP da lugar a sesquiterpenos. Estas reacciones están catalizadas por enzimas terpene synthase (TPS), cuya expresión es especialmente elevada en células secretoras de los tricomas glandulares. Este paso define en gran medida el perfil terpénico de la planta. (Booth et al., 2017; Gülck & Møller, 2020)
En paralelo, el GPP también participa en la biosíntesis de cannabinoides mediante su condensación con ácido olivetólico, dando lugar al ácido cannabigerólico (CBGA). Este compuesto representa el precursor central a partir del cual se sintetizan los principales cannabinoides ácidos, como THCA, CBDA y CBCA, mediante la acción de enzimas específicas como THCA sintasa y CBDA sintasa. Este punto metabólico conecta directamente la biosíntesis terpénica con la formación de fitocannabinoides. (Sirikantaramas et al., 2005; Taura et al., 2007)
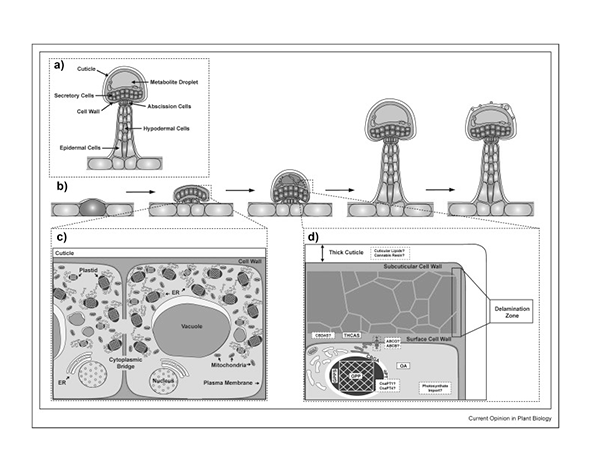
Las enzimas implicadas en estas rutas muestran una localización específica dentro de las células del tricoma, lo que sugiere un alto grado de compartimentalización metabólica. Por ejemplo, la síntesis de precursores isoprenoides ocurre en plastidios, mientras que etapas posteriores de modificación y secreción pueden implicar el retículo endoplasmático y el espacio extracelular. Esta organización permite una regulación eficiente de la producción de metabolitos y evita interferencias entre rutas metabólicas concurrentes. (Gülck & Møller, 2020)
Uno de los aspectos más relevantes de los tricomas glandulares es su capacidad para exportar los metabolitos sintetizados hacia la cavidad subcuticular. Este proceso implica mecanismos de transporte activo o vesicular que permiten transferir compuestos lipofílicos desde el interior celular hacia el espacio extracelular formado bajo la cutícula. De este modo, la resina se acumula fuera del citoplasma, minimizando el riesgo de toxicidad celular. (Kim & Mahlberg, 1997; Livingston et al., 2020)
La regulación de estas rutas biosintéticas está influenciada por múltiples factores, incluyendo el desarrollo de la planta, señales hormonales y condiciones ambientales como la luz, temperatura y estrés. En particular, la maduración de las flores femeninas se asocia con un incremento significativo en la actividad metabólica de los tricomas, lo que se traduce en una mayor producción de cannabinoides y terpenos. (Booth et al., 2017)
Además, estudios transcriptómicos han demostrado que los tricomas glandulares presentan perfiles de expresión génica diferenciados respecto a otros tejidos de la planta. Esto incluye una sobreexpresión de genes relacionados con metabolismo secundario, transporte de metabolitos y formación de estructuras secretoras. Esta especialización refuerza la idea de que los tricomas no son simplemente sitios de almacenamiento, sino sistemas biológicos activos altamente regulados. (Gülck & Møller, 2020)
En conjunto, los mecanismos moleculares presentes en los tricomas glandulares permiten a Cannabis sativa integrar rutas metabólicas complejas en un espacio celular altamente especializado. Esta organización no solo explica la producción eficiente de fitocannabinoides y terpenos, sino que también sitúa a los tricomas como el punto de convergencia entre la bioquímica vegetal y la diversidad química que caracteriza al cannabis. (Booth et al., 2017; Livingston et al., 2020)
Distribución y contexto fisiológico
Los tricomas glandulares de Cannabis sativa no se distribuyen de forma homogénea en la planta, sino que presentan una localización diferencial altamente regulada en función del tejido, el estadio de desarrollo y el contexto fisiológico. Esta distribución selectiva refleja su papel como estructuras especializadas asociadas principalmente a órganos aéreos y, de forma más marcada, a las estructuras reproductivas femeninas. (Werker, 2000; Livingston et al., 2020)
La mayor densidad y complejidad de tricomas glandulares se observa en las flores femeninas, especialmente en las brácteas que rodean los ovarios. En estas regiones, los tricomas capitados pedunculados alcanzan su máximo desarrollo estructural y funcional, acumulando grandes cantidades de resina rica en cannabinoides y terpenos. Esta concentración no es aleatoria, sino que responde a la necesidad de proteger tejidos reproductivos críticos, lo que sugiere un papel adaptativo en la supervivencia y éxito reproductivo de la planta. (Kim & Mahlberg, 1997; Booth et al., 2017)
En hojas, tallos y otras estructuras vegetativas también se pueden encontrar tricomas glandulares, aunque generalmente en menor densidad y con una menor capacidad biosintética. En estos tejidos predominan los tricomas bulbosos y sésiles, cuya función parece estar más orientada a la defensa general frente a factores ambientales, como herbívoros o radiación, que a la producción intensiva de metabolitos secundarios complejos. (Werker, 2000; Livingston et al., 2020)
El desarrollo de los tricomas glandulares está estrechamente ligado al ciclo de vida de la planta. Durante las primeras fases de crecimiento vegetativo, la densidad y actividad de los tricomas es relativamente baja. Sin embargo, a medida que la planta entra en fase de floración, especialmente en individuos femeninos, se produce una expansión significativa tanto en número como en tamaño de los tricomas, acompañada de un aumento en la actividad metabólica. Este proceso culmina en las fases finales de maduración floral, donde la producción de cannabinoides alcanza su punto máximo. (Booth et al., 2017)
Desde un punto de vista fisiológico, esta regulación temporal y espacial indica que los tricomas glandulares forman parte de una estrategia adaptativa compleja. La acumulación de metabolitos en momentos y tejidos específicos sugiere que la planta optimiza sus recursos en función de necesidades concretas, como la protección del tejido reproductivo o la interacción con el entorno. En este sentido, los tricomas no son estructuras estáticas, sino dinámicas, cuya actividad se ajusta a señales internas y externas. (Gülck & Møller, 2020)
Factores ambientales como la intensidad lumínica, la radiación ultravioleta, la temperatura y el estrés hídrico pueden influir en la densidad y actividad de los tricomas glandulares. Diversos estudios han mostrado que condiciones de estrés moderado pueden inducir un aumento en la producción de metabolitos secundarios, lo que sugiere que los tricomas participan en mecanismos de respuesta adaptativa frente a cambios en el entorno. (Livingston et al., 2020)
Además, la distribución de tricomas puede variar entre diferentes genotipos y quimiotipos de cannabis, reflejando diferencias en la regulación genética del desarrollo y del metabolismo secundario. Esta variabilidad contribuye a la diversidad química observada entre distintas variedades, reforzando la idea de que el perfil de cannabinoides y terpenos no depende únicamente de la biosíntesis, sino también de la arquitectura y densidad de los tricomas. (Booth et al., 2017)
En conjunto, la distribución y el contexto fisiológico de los tricomas glandulares evidencian una organización altamente específica dentro de la planta. Estas estructuras se concentran donde su función resulta más relevante, especialmente en tejidos reproductivos, y su actividad se modula en función del desarrollo y del entorno. Esta integración espacial y temporal refuerza su papel como elementos centrales en la biología del cannabis y en la generación de su perfil químico característico. (Gülck & Møller, 2020)
Interacción con fitocannabinoides y terpenos
Los tricomas glandulares de Cannabis sativa constituyen el principal sitio de síntesis, acumulación y liberación de fitocannabinoides y terpenos, actuando como el punto de convergencia funcional entre ambas familias de compuestos. Esta interacción no es meramente espacial, sino profundamente integrada a nivel biosintético, ya que ambas clases de moléculas comparten precursores metabólicos y maquinaria enzimática dentro de las células secretoras del tricoma. (Booth et al., 2017; Gülck & Møller, 2020)
Desde el punto de vista de los fitocannabinoides, los tricomas glandulares albergan las enzimas responsables de la conversión de precursores en cannabinoides ácidos. El ácido cannabigerólico (CBGA), sintetizado a partir de geranil pirofosfato (GPP) y ácido olivetólico, actúa como intermediario central en la formación de compuestos como THCA, CBDA y CBCA. Estas transformaciones ocurren predominantemente en las células de la cabeza glandular, lo que convierte al tricoma en el entorno bioquímico clave para la producción de cannabinoides. (Sirikantaramas et al., 2005; Taura et al., 2007)
En paralelo, los terpenos se sintetizan a partir de las mismas unidades isoprenoides generadas en las rutas MVA y MEP, dando lugar a monoterpenos y sesquiterpenos mediante la acción de enzimas terpene synthase (TPS). Esta coincidencia en el origen biosintético establece una relación directa entre la producción de cannabinoides y terpenos, no solo en términos de localización, sino también de disponibilidad de precursores y regulación metabólica. (Booth et al., 2017)
Una vez sintetizados, tanto los fitocannabinoides como los terpenos son secretados hacia la cavidad subcuticular del tricoma, donde se acumulan en forma de resina. Este entorno extracelular permite la coexistencia de múltiples compuestos lipofílicos en altas concentraciones, generando el perfil químico característico del cannabis. La composición final de esta resina depende de la actividad enzimática, la regulación génica y factores ambientales que afectan al tricoma. (Kim & Mahlberg, 1997; Livingston et al., 2020)
Aunque en el ámbito popular se ha difundido ampliamente el concepto de “efecto séquito”, la evidencia científica actual sugiere que la interacción entre cannabinoides y terpenos es compleja y no completamente comprendida. Desde una perspectiva estrictamente biológica, lo que sí es claro es que ambos tipos de compuestos coexisten en el mismo microentorno —el tricoma glandular— y comparten origen metabólico, lo que podría facilitar interacciones a distintos niveles, aunque su impacto funcional en sistemas biológicos externos sigue siendo objeto de investigación. (Russo, 2011; Gülck & Møller, 2020)
En términos ecológicos, la combinación de cannabinoides y terpenos en la resina puede desempeñar funciones complementarias. Mientras que los terpenos contribuyen a la volatilidad y a la interacción con el entorno (por ejemplo, atracción o repelencia de insectos), los cannabinoides pueden aportar propiedades adicionales relacionadas con la defensa química. Esta sinergia funcional refuerza la idea de que el tricoma no produce compuestos de forma aislada, sino como parte de una estrategia integrada de la planta. (Booth et al., 2017)
Desde el punto de vista de la investigación, el estudio conjunto de fitocannabinoides y terpenos dentro de los tricomas glandulares ha permitido avanzar en la comprensión del metabolismo secundario del cannabis. La caracterización de estas interacciones ha sido clave para el desarrollo de perfiles químicos específicos y para entender cómo la planta modula la producción de compuestos en función de su genética y del entorno. (Livingston et al., 2020)
En conjunto, la interacción entre fitocannabinoides y terpenos en los tricomas glandulares representa una integración metabólica y funcional que define la identidad química del cannabis. Estas estructuras no solo albergan la producción de ambos tipos de compuestos, sino que actúan como el entorno donde se configura su coexistencia, estableciendo un vínculo directo entre la biología de la planta y la complejidad de sus metabolitos. (Booth et al., 2017; Gülck & Møller, 2020)
Importancia en investigación biomédica
Los tricomas glandulares de Cannabis sativa han adquirido una relevancia creciente en investigación biomédica, no por su función directa en organismos humanos, sino por su papel como origen de los fitocannabinoides que interactúan con el sistema endocannabinoide. En este sentido, los tricomas representan el punto de partida biológico de compuestos que posteriormente son estudiados en contextos neurobiológicos, farmacológicos y fisiológicos. (Di Marzo, 1998; Booth et al., 2017)
Desde una perspectiva científica, el interés principal radica en comprender cómo estas estructuras vegetales producen y acumulan metabolitos capaces de modular sistemas biológicos en otras especies. El estudio de los tricomas permite contextualizar el origen de compuestos como CBD o THC, evitando interpretaciones simplificadas centradas únicamente en sus efectos, y reforzando una visión más completa que integra botánica, bioquímica y farmacología. (Gülck & Møller, 2020)
Además, los tricomas glandulares se han convertido en un modelo útil para investigar procesos fundamentales como la compartimentalización metabólica, la secreción de compuestos lipofílicos y la protección celular frente a metabolitos potencialmente reactivos. Estos aspectos son relevantes en biología vegetal, pero también tienen implicaciones en biotecnología y en el desarrollo de sistemas de producción de compuestos naturales. (Livingston et al., 2020)
En el ámbito de la investigación aplicada, la caracterización de los tricomas ha contribuido a mejorar la comprensión de la variabilidad en la producción de fitocannabinoides. Factores como la densidad de tricomas, su desarrollo y su actividad metabólica influyen directamente en la cantidad y proporción de compuestos presentes en la planta. Esto resulta relevante en estudios que buscan correlacionar perfiles químicos con efectos biológicos, aunque dichas relaciones deben interpretarse con cautela. (Booth et al., 2017)
Asimismo, el análisis de los tricomas ha permitido identificar enzimas clave en la biosíntesis de cannabinoides, lo que ha abierto la puerta a investigaciones en ingeniería metabólica y producción controlada de estos compuestos. Este enfoque no se limita al cannabis, sino que se integra dentro de un campo más amplio orientado a la obtención de metabolitos de interés mediante sistemas biológicos. (Gülck & Møller, 2020)
Sin embargo, es importante señalar que la relevancia biomédica de los tricomas es indirecta. Estas estructuras no actúan sobre el sistema endocannabinoide ni tienen efectos fisiológicos por sí mismas; su importancia reside en ser el origen de los compuestos que posteriormente pueden ser estudiados en modelos experimentales. Esta distinción es clave para mantener un enfoque riguroso y evitar interpretaciones que confundan niveles de análisis. (Di Marzo, 1998)
En conjunto, los tricomas glandulares deben entenderse como elementos fundamentales en la cadena de conocimiento que conecta la biología vegetal con la investigación biomédica. Su estudio permite situar los fitocannabinoides en su contexto natural, aportando una base estructural y funcional imprescindible para comprender su origen, su diversidad química y su papel en la investigación científica. (Livingston et al., 2020)
Referencias
- Booth JK, Page JE, Bohlmann J. (2017). Terpene synthases from Cannabis sativa. Plant Physiology. - Di Marzo V. (1998). ‘Endocannabinoids’ and other fatty acid derivatives with cannabimimetic properties. Biochemical Pharmacology. - Fahn A. (2000). Structure and function of secretory cells. Advances in Botanical Research. - Gülck T, Møller BL. (2020). Phytocannabinoids: Origins and biosynthesis. Trends in Plant Science. - Happyana N, Agnolet S, Muntendam R, et al. (2013). Analysis of cannabinoids in laser-microdissected trichomes of Cannabis sativa. Analytical and Bioanalytical Chemistry. - Kim ES, Mahlberg PG. (1997). Morphogenesis of glandular trichomes of Cannabis sativa. American Journal of Botany. - Lichtenthaler HK. (1999). The 1-deoxy-D-xylulose-5-phosphate pathway of isoprenoid biosynthesis. Annual Review of Plant Physiology and Plant Molecular Biology. - Livingston SJ, Quilichini TD, Booth JK, Wong DCJ, Rensing KH, Laflamme-Yonkman J, Castellarin SD, Bohlmann J, Page JE, Samuels AL. (2020). Cannabis glandular trichomes alter morphology and metabolite content during flower maturation. The Plant Journal. - Mechoulam R, Gaoni Y. (1964). Isolation, structure, and partial synthesis of an active constituent of hashish. Journal of the American Chemical Society. - Russo EB. (2011). Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. British Journal of Pharmacology. - Sirikantaramas S, Taura F, Morimoto S, Shoyama Y. (2005). Recent advances in cannabis sativa research: biosynthesis of cannabinoids. Plant Biotechnology. - Taura F, Sirikantaramas S, Shoyama Y, Yoshikai K, Shoyama Y, Morimoto S. (2007). Cannabidiolic-acid synthase, the chemotype-determining enzyme in the fiber-type cannabis. FEBS Letters. - Werker E. (2000). Trichome diversity and development. Advances in Botanical Research.