Introducción
El ácido cannabicroménico (CBCA) es uno de los principales fitocannabinoides ácidos biosintetizados en la planta de Cannabis sativa, y forma parte del conjunto de compuestos precursores que dan lugar a cannabinoides neutros tras procesos de descarboxilación térmica o envejecimiento. Aunque históricamente ha recibido menos atención que otros ácidos como el CBDA o el THCA, el CBCA desempeña un papel clave dentro de la diversificación metabólica de la planta y en la generación del cannabinoide neutro cannabicromeno (CBC). (Taura et al., 1996; ElSohly et al., 2017)
Desde el punto de vista químico, el CBCA pertenece a la familia de los cannabinoides tipo ácido carboxílico, caracterizados por la presencia de un grupo –COOH que les confiere propiedades fisicoquímicas distintas a sus formas neutras. Esta característica influye en su estabilidad, solubilidad y afinidad por distintas dianas biológicas, lo que ha generado un interés creciente en su estudio como entidad independiente y no solo como precursor metabólico. (Hanus et al., 2016; Pertwee, 2008)
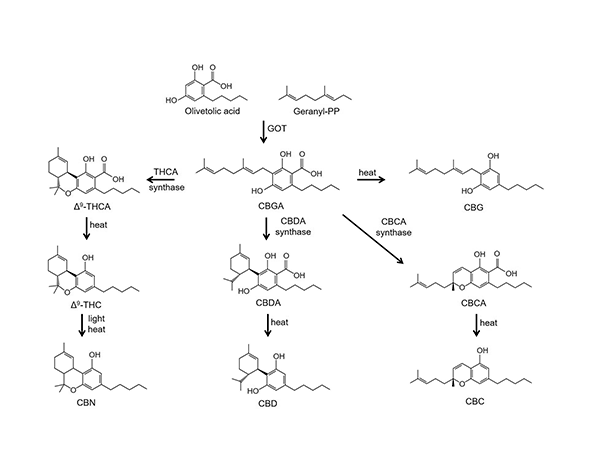
El CBCA se origina a partir del ácido cannabigerólico (CBGA) mediante la acción específica de la enzima CBCA sintasa, en un proceso biosintético altamente regulado que compite con otras rutas enzimáticas responsables de la formación de THCA y CBDA. Este punto de ramificación metabólica convierte al CBGA en un nodo central dentro de la bioquímica del cannabis, determinando en gran medida el perfil final de cannabinoides de la planta. (Taura et al., 2007; Gülck & Møller, 2020)
A nivel histórico, el CBCA ha sido menos caracterizado debido a la baja abundancia relativa en muchas variedades comerciales y a la dificultad técnica para su aislamiento y cuantificación en etapas tempranas de la investigación cannábica. Sin embargo, avances recientes en técnicas analíticas como la cromatografía líquida de alta resolución (HPLC) han permitido una mejor identificación y cuantificación de este compuesto en matrices vegetales complejas. (Citti et al., 2018; Pellati et al., 2018)
En el contexto actual, el interés por el CBCA se enmarca dentro de una tendencia más amplia hacia el estudio de los cannabinoides ácidos como entidades bioactivas propias, más allá de su papel como precursores. Este cambio de paradigma está impulsando nuevas líneas de investigación orientadas a comprender su posible interacción con sistemas fisiológicos humanos, incluyendo dianas no clásicas del sistema endocannabinoide. (Rock et al., 2018; Ligresti et al., 2006)
Historia y descubrimiento
El estudio del ácido cannabicroménico (CBCA) se enmarca dentro del desarrollo temprano de la química de los fitocannabinoides durante la segunda mitad del siglo XX, un periodo caracterizado por la identificación progresiva de los principales compuestos presentes en Cannabis sativa. Aunque el foco inicial de la investigación se centró en cannabinoides neutros como el THC y el CBD, pronto se hizo evidente que muchas de estas moléculas derivaban de precursores ácidos presentes de forma natural en la planta fresca. (Gaoni & Mechoulam, 1964; Mechoulam & Gaoni, 1967)
El cannabicromeno (CBC) fue aislado por primera vez en la década de 1960 como uno de los cannabinoides estructuralmente distintos al THC, lo que despertó interés en su origen biosintético. Sin embargo, la identificación de su forma ácida, el CBCA, no se consolidó hasta años posteriores, cuando los avances en técnicas cromatográficas permitieron distinguir entre las formas neutras y sus correspondientes precursores carboxilados. (Claussen et al., 1966; Shoyama et al., 1975)
Durante las décadas de 1980 y 1990, el desarrollo de metodologías analíticas más precisas, especialmente la cromatografía líquida de alta resolución (HPLC), permitió estudiar los cannabinoides en su estado nativo sin necesidad de descarboxilación térmica, lo que supuso un punto de inflexión en la comprensión del perfil químico real de la planta. En este contexto, el CBCA comenzó a ser reconocido como una entidad diferenciada y no simplemente como un artefacto derivado del CBC. (Hazekamp et al., 2005; Citti et al., 2018)
Un avance clave en la comprensión del CBCA se produjo con la identificación de las enzimas específicas implicadas en su biosíntesis. A finales de los años 90 y principios de los 2000, estudios liderados por investigadores como Fumihiko Taura permitieron caracterizar las sintasas responsables de la conversión del CBGA en distintos cannabinoides ácidos, incluyendo la CBCA sintasa, estableciendo así las bases moleculares de la diversificación cannabinoide en la planta. (Taura et al., 1996; Taura et al., 2007)
A diferencia de otras rutas biosintéticas más estudiadas, como las que conducen al THCA o al CBDA, la vía del CBCA ha recibido históricamente menos atención, en parte debido a la menor prevalencia del CBC en muchas variedades comerciales. No obstante, estudios más recientes han comenzado a explorar quimiotipos ricos en CBC, lo que ha revalorizado el interés por el CBCA como precursor clave en estos perfiles fitoquímicos. (ElSohly et al., 2017; Gülck & Møller, 2020)
En la actualidad, el CBCA se considera un componente integral del metabolismo del cannabis, cuya relevancia científica está aumentando a medida que se profundiza en el estudio de los cannabinoides menores y sus posibles implicaciones biológicas. Este cambio refleja una transición desde un enfoque centrado en unos pocos compuestos dominantes hacia una visión más compleja y sistémica del fitocomplejo cannábico. (Hanus et al., 2016; Pertwee, 2015)
Estructura química y propiedades fisicoquímicas
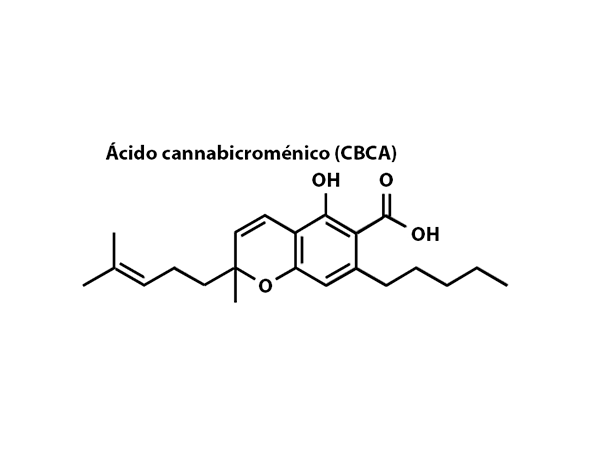
El ácido cannabicroménico (CBCA) es un fitocannabinoide de naturaleza terpenofenólica, cuya estructura deriva de la condensación entre una unidad fenólica (procedente del ácido olivetólico) y una cadena prenilada (geranil pirofosfato), dando lugar al esqueleto característico de los cannabinoides. A diferencia de otros cannabinoides ácidos como el CBDA o el THCA, el CBCA presenta una estructura tricíclica distinta, lo que lo sitúa dentro de una subfamilia estructural específica dentro del fitocomplejo cannábico. (Taura et al., 2007; Hanus et al., 2016)
A nivel molecular, el CBCA mantiene el grupo funcional ácido carboxílico (–COOH), responsable de su clasificación como cannabinoide ácido y de muchas de sus propiedades fisicoquímicas. Este grupo confiere mayor polaridad relativa frente a sus formas neutras y condiciona su comportamiento en disolución, su estabilidad térmica y su reactividad química, especialmente en procesos de descarboxilación que conducen a la formación de cannabicromeno (CBC). (Decorte et al., 2011; Citti et al., 2018)
Una característica distintiva del CBCA es su núcleo croménico, que resulta de la ciclación oxidativa específica catalizada por la CBCA sintasa. Esta ciclación genera un sistema heterocíclico que difiere del anillo dibenzopirano típico del THC o de la estructura abierta característica del CBD, lo que tiene implicaciones tanto en su comportamiento químico como en su posible interacción con dianas biológicas. (Shoyama et al., 1975; Gülck & Møller, 2020)
Desde el punto de vista estereoquímico, el CBCA presenta centros quirales que pueden influir en la conformación tridimensional de la molécula y, potencialmente, en su afinidad por distintos sistemas biológicos. Aunque la estereoquímica de los cannabinoides ácidos ha sido menos explorada que la de sus formas neutras, se reconoce como un factor relevante en estudios farmacológicos avanzados. (Hanus et al., 2016)
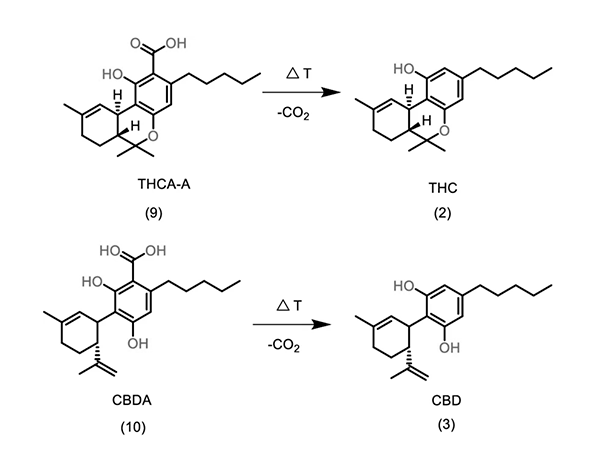
En términos de propiedades fisicoquímicas, el CBCA es termosensible e inestable a temperaturas elevadas, lo que favorece su descarboxilación espontánea o inducida hacia CBC. Este proceso implica la pérdida de dióxido de carbono (CO₂) y constituye una transformación clave tanto en el procesamiento de la planta como en su almacenamiento. La cinética de esta reacción depende de factores como la temperatura, la exposición a la luz y el tiempo. (Perrotin-Brunel et al., 2011; Wang et al., 2016)
Además, el CBCA presenta una baja solubilidad en agua y una alta afinidad por disolventes orgánicos y matrices lipídicas, en línea con otros fitocannabinoides. Esta característica condiciona su extracción, formulación y análisis, siendo la cromatografía líquida (HPLC) la técnica preferida para su cuantificación sin inducir descarboxilación, a diferencia de la cromatografía de gases (GC), que puede transformar el CBCA en CBC durante el análisis. (Citti et al., 2018; Pellati et al., 2018)
En conjunto, la estructura del CBCA no solo define su papel como precursor del CBC, sino que también determina sus propiedades químicas y su comportamiento en sistemas biológicos y tecnológicos, constituyendo una base fundamental para su estudio dentro de la química de los cannabinoides. (Pertwee, 2008; ElSohly et al., 2017)
Biosíntesis y distribución en la planta
El ácido cannabicroménico (CBCA) se biosintetiza en Cannabis sativa a partir del precursor central ácido cannabigerólico (CBGA), considerado el nodo metabólico principal en la producción de fitocannabinoides. Este proceso tiene lugar en los tricomas glandulares de la planta, estructuras especializadas responsables de la síntesis y acumulación de compuestos secundarios lipofílicos, incluyendo cannabinoides y terpenos. (Taura et al., 2007; Gülck & Møller, 2020)
La conversión de CBGA en CBCA está catalizada por la enzima CBCA sintasa, una oxidorreductasa dependiente de flavina que induce una ciclación oxidativa específica, dando lugar al núcleo croménico característico del CBCA. Esta reacción compite directamente con otras rutas enzimáticas paralelas, como las mediadas por la THCA sintasa y la CBDA sintasa, lo que convierte al CBGA en un punto de bifurcación clave que determina el perfil final de cannabinoides de la planta. (Taura et al., 1996; Sirikantaramas et al., 2004)
La expresión diferencial de estas enzimas es uno de los factores principales que define los quimiotipos de cannabis, es decir, las distintas variedades caracterizadas por perfiles específicos de cannabinoides. En este contexto, las plantas con mayor actividad de CBCA sintasa tienden a producir niveles más elevados de CBC tras la descarboxilación, aunque en la mayoría de variedades comerciales esta vía es menos dominante en comparación con las rutas del THCA o CBDA. (ElSohly et al., 2017; Gülck & Møller, 2020)
A nivel subcelular, la biosíntesis de CBCA implica la interacción entre compartimentos celulares diferenciados. El CBGA se forma inicialmente en el citosol a partir de la unión entre el ácido olivetólico y el geranil pirofosfato, mientras que las sintasas cannabinoides, incluida la CBCA sintasa, se localizan en el espacio apoplástico o en compartimentos extracelulares asociados a los tricomas. Esta organización espacial sugiere un sistema altamente regulado que minimiza la toxicidad intracelular y optimiza la acumulación de metabolitos. (Sirikantaramas et al., 2005; Gülck & Møller, 2020)
En términos de distribución, el CBCA se encuentra principalmente en las inflorescencias femeninas, donde la densidad de tricomas es máxima. Su concentración varía en función de factores genéticos, condiciones de cultivo y estado de maduración de la planta. Generalmente, los niveles de CBCA son más elevados en fases tempranas, antes de que procesos naturales de descarboxilación o degradación reduzcan su presencia en favor del CBC. (Aizpurua-Olaizola et al., 2016; Happyana et al., 2013)
Además, factores ambientales como la luz, la temperatura y el estrés abiótico pueden influir en la expresión de las enzimas implicadas en la biosíntesis cannabinoide, modulando indirectamente la producción de CBCA. Este carácter dinámico refuerza la idea de que el perfil cannabinoide de una planta no es estático, sino el resultado de una interacción compleja entre genética y entorno. (Caplan et al., 2017; Gülck & Møller, 2020)
En conjunto, la biosíntesis del CBCA ilustra la complejidad del metabolismo secundario en Cannabis sativa, donde múltiples rutas compiten y coexisten, generando una diversidad química que va más allá de los cannabinoides mayoritarios y abre la puerta a nuevas líneas de investigación sobre compuestos menos estudiados. (Hanus et al., 2016; Pertwee, 2015)
Interacción con el sistema endocannabinoide y dianas moleculares
El conocimiento actual sobre la interacción del ácido cannabicroménico (CBCA) con el sistema endocannabinoide es limitado, y la mayor parte de la evidencia disponible procede de estudios indirectos o extrapolaciones a partir de su forma descarboxilada, el cannabicromeno (CBC). Esta limitación es común en los cannabinoides ácidos, cuya investigación ha sido históricamente secundaria frente a sus homólogos neutros. (Pertwee, 2008; Hanus et al., 2016)
En términos generales, los cannabinoides ácidos como el CBCA muestran una baja afinidad por los receptores cannabinoides clásicos CB1 y CB2, en comparación con compuestos neutros como el THC. Esta menor afinidad se ha atribuido, en parte, a la presencia del grupo carboxilo (–COOH), que altera la lipofilia y la capacidad de atravesar membranas, así como la interacción directa con los sitios de unión de estos receptores. (Pertwee, 2008; Rock et al., 2018)
No obstante, la ausencia de una interacción fuerte con CB1/CB2 no implica falta de actividad biológica. Diversos estudios han puesto de manifiesto que los cannabinoides ácidos pueden interactuar con dianas no clásicas del sistema endocannabinoide ampliado, incluyendo canales iónicos de la familia TRP y receptores nucleares. En el caso del CBC, se ha descrito actividad sobre canales como TRPA1 y TRPV1, lo que sugiere que el CBCA podría compartir, al menos parcialmente, este perfil de interacción, aunque la evidencia directa sigue siendo escasa. (De Petrocellis et al., 2011; Cascio & Pertwee, 2014)
Además, algunos trabajos han explorado la posibilidad de que cannabinoides ácidos modulen indirectamente el sistema endocannabinoide a través de la inhibición de enzimas implicadas en la degradación de endocannabinoides, como la FAAH o la MAGL. Sin embargo, en el caso específico del CBCA, los datos son aún insuficientes para establecer conclusiones firmes, y este aspecto permanece como una línea abierta de investigación. (Ligresti et al., 2006; Bisogno et al., 2001)
Otra vía potencial de interacción se sitúa en el ámbito de los receptores nucleares tipo PPAR, implicados en la regulación del metabolismo energético, la inflamación y la homeostasis celular. Algunos fitocannabinoides, incluyendo formas ácidas, han mostrado capacidad de activar o modular estos receptores, lo que sugiere un mecanismo de acción más difuso y sistémico en comparación con la señalización cannabinoide clásica. (O’Sullivan, 2016; Pertwee, 2015)
Es importante destacar que gran parte de estas hipótesis se basan en estudios in vitro o en modelos preclínicos, y que la evidencia específica sobre CBCA sigue siendo limitada. Por ello, cualquier interpretación de su actividad biológica debe abordarse desde una perspectiva crítica, evitando extrapolaciones directas desde otros cannabinoides sin validación experimental específica. (Hanus et al., 2016)
En conjunto, el CBCA se sitúa dentro de un grupo de compuestos cuyo interés radica no tanto en su interacción directa con los receptores clásicos del sistema endocannabinoide, sino en su posible participación en redes de señalización más amplias, aún en proceso de caracterización. Este enfoque refleja una evolución en la investigación cannabinoide hacia modelos más complejos y menos centrados exclusivamente en CB1 y CB2. (Pertwee, 2008; Rock et al., 2018)
Farmacología y evidencia experimental
La evidencia farmacológica específica sobre el ácido cannabicroménico (CBCA) es, en la actualidad, limitada, y se basa principalmente en estudios preclínicos, análisis in vitro y extrapolaciones a partir de otros cannabinoides estructuralmente relacionados. Esta situación refleja una tendencia general en la investigación de cannabinoides ácidos, que históricamente han recibido menos atención que sus formas neutras debido a su inestabilidad y menor presencia en productos procesados. (Hanus et al., 2016; Pertwee, 2015)
Uno de los principales retos en el estudio del CBCA es su tendencia a la descarboxilación, lo que dificulta su aislamiento y mantenimiento en condiciones experimentales controladas. Como consecuencia, muchos estudios han evaluado indirectamente su actividad a través del cannabicromeno (CBC), su forma neutra, que presenta mayor estabilidad y disponibilidad. Sin embargo, esta aproximación introduce limitaciones importantes, ya que los cannabinoides ácidos pueden presentar perfiles farmacológicos distintos a sus derivados descarboxilados. (Perrotin-Brunel et al., 2011; Rock et al., 2018)
En modelos celulares, algunos cannabinoides ácidos han mostrado capacidad para modular procesos relacionados con la señalización celular, incluyendo la actividad de canales iónicos, enzimas metabólicas y factores de transcripción. Aunque los datos específicos sobre CBCA son escasos, su similitud estructural con otros compuestos sugiere que podría participar en estos mecanismos, particularmente en el contexto de dianas no clásicas del sistema endocannabinoide. (Ligresti et al., 2006; Cascio & Pertwee, 2014)
Desde el punto de vista experimental, el estudio del CBCA se ha visto facilitado por el uso de técnicas analíticas avanzadas como la cromatografía líquida acoplada a espectrometría de masas (LC-MS), que permite detectar y cuantificar cannabinoides ácidos sin inducir su transformación térmica. Estas metodologías han permitido una caracterización más precisa de su presencia en extractos vegetales y han abierto nuevas posibilidades para su investigación farmacológica. (Citti et al., 2018; Pellati et al., 2018)
A nivel in vivo, la información disponible es aún más limitada, y no existen suficientes estudios que evalúen de forma específica los efectos del CBCA en organismos completos. Esta ausencia de datos impide establecer conclusiones sobre su biodisponibilidad, metabolismo o posibles efectos fisiológicos, lo que subraya la necesidad de investigaciones más profundas y controladas. (Hanus et al., 2016)
Otro aspecto relevante es la posibilidad de que el CBCA participe en interacciones sinérgicas dentro del fitocomplejo cannábico, un fenómeno a menudo referido como efecto séquito. Aunque este concepto sigue siendo objeto de debate científico, algunos estudios sugieren que combinaciones de cannabinoides y otros metabolitos pueden modular la actividad biológica de forma conjunta, incluso cuando los compuestos individuales presentan efectos limitados por sí solos. (Russo, 2011; Pertwee, 2015)
En conjunto, el CBCA representa un ejemplo claro de los desafíos y oportunidades asociados al estudio de cannabinoides menores. Su perfil farmacológico permanece en gran medida inexplorado, pero su inclusión en investigaciones futuras podría contribuir a una comprensión más completa del sistema endocannabinoide ampliado y de la complejidad del fitocomplejo del cannabis. (Gülck & Møller, 2020; Hanus et al., 2016)
Importancia en investigación y contexto científico
El ácido cannabicroménico (CBCA) representa uno de los múltiples ejemplos de cómo la investigación en cannabinoides está evolucionando desde un enfoque centrado en compuestos mayoritarios hacia una visión más amplia del fitocomplejo del cannabis. En este contexto, el interés por moléculas como el CBCA no reside únicamente en su abundancia o actividad individual, sino en su contribución a la diversidad química y funcional de la planta. (Hanus et al., 2016; Pertwee, 2015)
Tradicionalmente, la investigación cannábica se ha centrado en unos pocos compuestos dominantes, principalmente THC y CBD, dejando en segundo plano tanto a cannabinoides menores como a sus formas ácidas. Sin embargo, el desarrollo de nuevas herramientas analíticas y el acceso a quimiotipos más diversos han permitido identificar y cuantificar compuestos como el CBCA con mayor precisión, impulsando su incorporación en estudios fitoquímicos más completos. (Citti et al., 2018; ElSohly et al., 2017)
Desde una perspectiva bioquímica, el CBCA es relevante como parte de las rutas biosintéticas competitivas que parten del CBGA, lo que lo convierte en un marcador indirecto de la actividad enzimática dentro de la planta. El estudio de estas rutas no solo permite comprender mejor la producción de cannabinoides, sino que también abre la puerta a estrategias de cultivo y mejora genética orientadas a perfiles fitoquímicos específicos. (Gülck & Møller, 2020; Taura et al., 2007)
En el ámbito farmacológico, el CBCA se sitúa dentro de un grupo de compuestos cuya actividad biológica aún no está completamente caracterizada. Este desconocimiento no debe interpretarse como ausencia de relevancia, sino como una oportunidad científica, especialmente en el contexto del sistema endocannabinoide ampliado y de la identificación de nuevas dianas moleculares. (Rock et al., 2018; O’Sullivan, 2016)
Además, el interés por los cannabinoides ácidos está creciendo en paralelo a un cambio de paradigma en la investigación, que reconoce que estos compuestos pueden poseer propiedades distintas a sus formas neutras. Este enfoque cuestiona la idea tradicional de que los cannabinoides ácidos son meros precursores inactivos, y promueve su estudio como entidades bioquímicas independientes. (Rock et al., 2018; Hanus et al., 2016)
En el contexto más amplio de la ciencia del cannabis, el CBCA contribuye a reforzar una visión más compleja y matizada del fitocomplejo, donde la interacción entre múltiples compuestos —incluyendo cannabinoides, terpenos y flavonoides— puede dar lugar a efectos emergentes que no se explican únicamente por la acción de moléculas individuales. (Russo, 2011; Pertwee, 2015)
Finalmente, el estudio del CBCA también tiene implicaciones metodológicas, ya que pone de relieve la importancia de utilizar técnicas analíticas adecuadas que preserven la integridad de los cannabinoides ácidos. Este aspecto es especialmente relevante en investigación y control de calidad, donde la distinción entre formas ácidas y neutras es fundamental para una caracterización precisa. (Citti et al., 2018)
En conjunto, el CBCA no solo amplía el conocimiento sobre la química del cannabis, sino que también refleja el estado actual de la investigación cannabinoide: un campo en expansión, cada vez más orientado hacia la complejidad molecular y la integración de múltiples niveles de análisis. (Gülck & Møller, 2020; Hanus et al., 2016)
Referencias
- Aizpurua-Olaizola O, Soydaner U, Öztürk E, Schibano D, Simsir Y, Navarro P, Etxebarria N, Usobiaga A. (2016). Evolution of the cannabinoid and terpene content during the growth of Cannabis sativa plants from different chemotypes. Journal of Natural Products. - Bisogno T, Hanus L, De Petrocellis L, Tchilibon S, Ponde DE, Brandi I, Moriello AS, Davis JB, Mechoulam R, Di Marzo V. (2001). Molecular targets for cannabidiol and its synthetic analogues: effect on vanilloid VR1 receptors and on the cellular uptake and enzymatic hydrolysis of anandamide. British Journal of Pharmacology. - Cascio MG, Pertwee RG. (2014). Known pharmacological actions of Δ9-tetrahydrocannabinol and of four other chemical constituents of Cannabis sativa that activate cannabinoid receptors. Handbook of Experimental Pharmacology. - Citti C, Braghiroli D, Vandelli MA, Cannazza G. (2018). Pharmaceutical and biomedical analysis of cannabinoids: A critical review. Journal of Pharmaceutical and Biomedical Analysis. - Claussen U, Spulak F, Korte F. (1966). Constitution of cannabichromene, a new hashish constituent. Tetrahedron Letters. - Decorte T. (2011). Small scale domestic cannabis cultivation: An anonymous web survey among 659 cannabis cultivators in Belgium. (contexto analítico sobre estabilidad y procesamiento de cannabinoides). - De Petrocellis L, Ligresti A, Moriello AS, Allarà M, Bisogno T, Petrosino S, Stott CG, Di Marzo V. (2011). Effects of cannabinoids and cannabinoid-enriched Cannabis extracts on TRP channels and endocannabinoid metabolic enzymes. British Journal of Pharmacology. - ElSohly MA, Radwan MM, Gul W, Chandra S, Galal A. (2017). Phytochemistry of Cannabis sativa L. Progress in the Chemistry of Organic Natural Products. - Gaoni Y, Mechoulam R. (1964). Isolation, structure, and partial synthesis of an active constituent of hashish. Journal of the American Chemical Society. - Gülck T, Møller BL. (2020). Phytocannabinoids: Origins and biosynthesis. Trends in Plant Science. - Hanus LO, Meyer SM, Muñoz E, Taglialatela-Scafati O, Appendino G. (2016). Phytocannabinoids: A unified critical inventory. Natural Product Reports. - Happyana N, Agnolet S, Muntendam R, van Dam A, Schneider B, Kayser O. (2013). Analysis of cannabinoids in laser-microdissected trichomes of medicinal Cannabis sativa using LC-MS and GC-MS. Analytical and Bioanalytical Chemistry. - Hazekamp A, Fischedick JT. (2005). Cannabis—from cultivar to chemovar. Drug Testing and Analysis. - Ligresti A, Moriello AS, Starowicz K, Matias I, Pisanti S, De Petrocellis L, Laezza C, Portella G, Bifulco M, Di Marzo V. (2006). Antitumor activity of plant cannabinoids with emphasis on the effect of cannabidiol. Journal of Pharmacology and Experimental Therapeutics. - Mechoulam R, Gaoni Y. (1967). The isolation and structure of Δ1-tetrahydrocannabinol and other neutral cannabinoids. Journal of the American Chemical Society. - O’Sullivan SE. (2016). An update on PPAR activation by cannabinoids. British Journal of Pharmacology. - Pellati F, Brighenti V, Sperlea J, Marchetti L, Bertelli D, Benvenuti S. (2018). New methods for the comprehensive analysis of cannabinoids in Cannabis sativa L. Molecules. - Perrotin-Brunel H, Kroon MC, van Roosmalen MJ, van Spronsen J, Peters CJ, Witkamp GJ. (2011). Decarboxylation of Δ9-tetrahydrocannabinol: Kinetics and molecular modeling. Journal of Molecular Structure. - Pertwee RG. (2008). The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids. British Journal of Pharmacology. - Pertwee RG. (2015). Endocannabinoids and their pharmacological actions. Handbook of Experimental Pharmacology. - Rock EM, Limebeer CL, Parker LA. (2018). Effect of cannabinoids on nausea and vomiting. Handbook of Experimental Pharmacology. - Russo EB. (2011). Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. British Journal of Pharmacology. - Shoyama Y, Tamada T, Nishioka I. (1975). Cannabis. XIII. Cannabichromenic acid, a genuine substance of cannabis. Chemical & Pharmaceutical Bulletin. - Sirikantaramas S, Morimoto S, Shoyama Y, Ishikawa Y, Wada Y, Shoyama Y, Taura F. (2004). The gene controlling marijuana psychoactivity: molecular cloning and heterologous expression of Δ1-tetrahydrocannabinolic acid synthase. Journal of Biological Chemistry. - Sirikantaramas S, Taura F, Morimoto S, Shoyama Y. (2005). Recent advances in cannabis biosynthetic studies. Plant Biotechnology. - Taura F, Morimoto S, Shoyama Y. (1996). Purification and characterization of cannabidiolic-acid synthase from Cannabis sativa. Journal of Biological Chemistry. - Taura F, Sirikantaramas S, Shoyama Y, Yoshikai K, Shoyama Y, Morimoto S. (2007). Cannabidiolic-acid synthase, the chemotype-determining enzyme in the fiber-type Cannabis sativa. FEBS Letters. - Wang M, Wang YH, Avula B, Radwan MM, Wanas AS, van Antwerp J, Parcher JF, ElSohly MA, Khan IA. (2016). Decarboxylation study of acidic cannabinoids: a novel approach using ultra-high-performance supercritical fluid c hromatography/photodiode array-mass spectrometry. Cannabis and Cannabinoid Research.