Introducción
El TRPV2 (Transient Receptor Potential Vanilloid 2) es un canal iónico no selectivo perteneciente a la familia de los canales TRP (Transient Receptor Potential), específicamente al subgrupo vanilloide. Se caracteriza por su capacidad para responder a estímulos físicos y químicos, incluyendo cambios de temperatura elevada, estrés mecánico y determinadas señales lipídicas endógenas. A diferencia de otros miembros de la familia como TRPV1, TRPV2 presenta un umbral de activación térmica más alto y una farmacología menos definida, lo que ha contribuido a que su estudio sea más complejo y, en muchos aspectos, todavía incompleto (Caterina et al., 1999; Neeper et al., 2007).
A nivel fisiológico, TRPV2 se expresa en una amplia variedad de tejidos, incluyendo sistema nervioso, músculo, células inmunes y tejidos metabólicamente activos, lo que sugiere un papel multifuncional en procesos como la detección de estímulos nocivos, la regulación del volumen celular, la respuesta inflamatoria y la homeostasis tisular. Su localización subcelular dinámica —capaz de translocarse a la membrana plasmática en respuesta a señales específicas— añade una capa adicional de complejidad a su regulación funcional (Kanzaki et al., 1999; Shibasaki et al., 2010).
En el contexto del sistema endocannabinoide, TRPV2 ha emergido como una diana molecular relevante, particularmente por su interacción con fitocannabinoides como el cannabidiol (CBD), que puede modular su actividad de forma indirecta o dependiente del contexto celular. Esta interacción sitúa a TRPV2 dentro del conjunto de dianas no clásicas del sistema endocannabinoide, ampliando el marco conceptual más allá de los receptores CB1 y CB2 y reforzando la idea de una red de señalización distribuida y altamente interconectada (De Petrocellis et al., 2011; Qin et al., 2008).
Desde una perspectiva científica, TRPV2 representa un nodo de interés creciente en investigación básica y aplicada, especialmente en áreas como neurobiología, inmunología y oncología, donde su implicación en procesos de proliferación celular, migración y respuesta al estrés está siendo activamente investigada. Sin embargo, pese al aumento de estudios en los últimos años, su función exacta en muchos contextos fisiológicos y patológicos sigue siendo objeto de debate, reflejando la necesidad de investigaciones más específicas y modelos experimentales más refinados.
Historia del descubrimiento
El canal TRPV2 fue identificado a finales de la década de 1990 en el contexto de la expansión del conocimiento sobre la familia de canales TRP, un grupo de proteínas inicialmente descrito en Drosophila y posteriormente caracterizado en mamíferos como sensores clave de estímulos físicos y químicos. Su descubrimiento se produjo poco después de la caracterización de TRPV1, el primer canal vanilloide identificado, lo que llevó a su clasificación inicial como un homólogo estructural con posibles funciones sensoriales similares (Caterina et al., 1999).
En sus primeras descripciones, TRPV2 fue denominado VRL-1 (Vanilloid Receptor-Like 1) debido a su similitud con TRPV1, aunque rápidamente se observó que su perfil funcional difería de manera significativa. A diferencia de TRPV1, TRPV2 no responde a capsaicina ni a protones en condiciones fisiológicas estándar, lo que sugirió desde el inicio que su activación dependía de mecanismos distintos, incluyendo estímulos térmicos de mayor intensidad (>52 °C) y señales mecánicas o osmóticas (Neeper et al., 2007).
Uno de los hitos clave en su caracterización fue la observación de su translocación dependiente de estímulos desde compartimentos intracelulares hacia la membrana plasmática. Estudios iniciales en células musculares y neuronas demostraron que factores como el factor de crecimiento similar a la insulina (IGF-1) podían inducir esta translocación, permitiendo la activación funcional del canal en respuesta a señales extracelulares (Kanzaki et al., 1999). Este comportamiento dinámico diferenció a TRPV2 de otros canales TRP más constitutivamente localizados en membrana.
Durante la década de 2000, el interés por TRPV2 se amplió hacia su papel en tejidos no neuronales, especialmente en células del sistema inmune, donde se identificó su implicación en procesos como fagocitosis y respuesta inflamatoria. Paralelamente, comenzaron a explorarse sus posibles interacciones con lípidos bioactivos y compuestos derivados del cannabis, situándolo progresivamente dentro del marco más amplio de las dianas moleculares relacionadas con el sistema endocannabinoide (Qin et al., 2008; De Petrocellis et al., 2011).
A pesar de estos avances, la historia de TRPV2 se caracteriza por una evolución más lenta y menos definida que la de otros canales TRP, en parte debido a la ausencia de agonistas selectivos altamente específicos y a la complejidad de sus mecanismos de regulación. En la actualidad, sigue considerándose un canal en fase de caracterización funcional avanzada, con múltiples aspectos aún abiertos en cuanto a su relevancia fisiológica precisa y su potencial como diana terapéutica.
Estructura y organización molecular
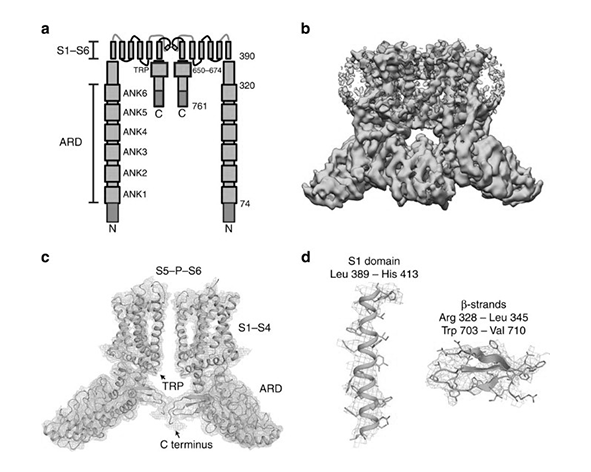
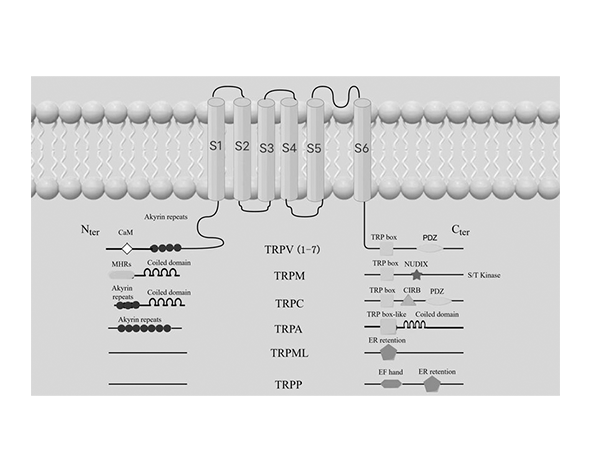
El canal TRPV2 es una proteína transmembrana que forma parte de la superfamilia de canales TRP, caracterizada por su arquitectura tetramérica y su función como canal catiónico no selectivo. Cada subunidad de TRPV2 está compuesta por aproximadamente 760–800 aminoácidos y presenta una organización estructural conservada dentro del subgrupo vanilloide, incluyendo seis dominios transmembrana (S1–S6), un bucle reentrante entre S5 y S6 que conforma el poro del canal, y dominios intracelulares N- y C-terminales implicados en la regulación funcional (Liao et al., 2013).
El canal funcional se organiza como un homotetrámero, en el que cuatro subunidades se ensamblan para formar una estructura central que permite el paso de iones, principalmente calcio (Ca²⁺), sodio (Na⁺) y, en menor medida, otros cationes. La región del poro, situada entre los segmentos S5 y S6, determina la selectividad iónica y las propiedades de conducción del canal, mientras que los dominios transmembrana S1–S4 actúan como sensores estructurales implicados en la detección de estímulos físicos y químicos (Cao et al., 2013).
En el extremo N-terminal, TRPV2 contiene múltiples repeticiones ankyrin (ARDs, Ankyrin Repeat Domains), estructuras proteicas que facilitan interacciones con otras proteínas y participan en la modulación del canal por factores intracelulares. Estas regiones son clave para la integración de señales celulares y la regulación de la actividad del canal en función del contexto fisiológico. Por su parte, el extremo C-terminal incluye dominios implicados en procesos de ensamblaje, tráfico intracelular y anclaje a componentes del citoesqueleto (Gaudet, 2008).
Una característica distintiva de TRPV2 es su localización subcelular dinámica. A diferencia de otros canales TRP que se encuentran predominantemente en la membrana plasmática, TRPV2 puede residir en compartimentos intracelulares (como vesículas o retículo endoplásmico) y translocarse hacia la membrana en respuesta a señales específicas, como factores de crecimiento o cambios en el estado celular. Este comportamiento sugiere que su actividad no depende únicamente de la presencia del canal, sino también de su disponibilidad espacial dentro de la célula (Kanzaki et al., 1999; Shibasaki et al., 2010).
Desde el punto de vista estructural, estudios recientes mediante crio-microscopía electrónica (cryo-EM) han permitido visualizar con mayor precisión la conformación de TRPV2 en diferentes estados funcionales, revelando cambios conformacionales asociados a la apertura del canal y a la interacción con ligandos lipídicos. Estas aproximaciones han puesto de manifiesto la flexibilidad estructural del canal y su capacidad para integrar múltiples señales moduladoras en su activación (Zubcevic et al., 2016).
En conjunto, la estructura de TRPV2 refleja una organización compleja y altamente regulada, en la que dominios proteicos especializados permiten la integración de señales mecánicas, térmicas y químicas, situando a este canal como un sensor multifuncional dentro del entorno celular.
Distribución y expresión tisular
El canal TRPV2 presenta una distribución amplia y heterogénea en el organismo, lo que sugiere un papel funcional diverso en distintos sistemas fisiológicos. A diferencia de otros canales TRP con expresión más restringida, TRPV2 se encuentra tanto en tejidos excitables como no excitables, incluyendo sistema nervioso, músculo, sistema inmune y diversos órganos periféricos (Neeper et al., 2007).
En el sistema nervioso, TRPV2 se expresa en neuronas sensoriales de diámetro medio y grande, especialmente en ganglios de la raíz dorsal (DRG), donde se ha asociado con la detección de estímulos mecánicos y térmicos de alta intensidad. A diferencia de TRPV1, su presencia es menos prominente en neuronas nociceptivas clásicas, lo que ha llevado a plantear que TRPV2 podría estar más implicado en la mecanotransducción y en la percepción de estímulos potencialmente lesivos no convencionales (Caterina et al., 1999; Shibasaki et al., 2010).
En el tejido muscular, tanto esquelético como cardíaco, TRPV2 desempeña un papel relevante en la regulación del calcio intracelular y en la respuesta al estrés mecánico. Se ha observado su participación en procesos de adaptación muscular, regeneración y mantenimiento de la integridad celular, especialmente en condiciones de carga o daño tisular. Alteraciones en su localización o función han sido asociadas con patologías musculares, incluyendo miopatías y disfunción cardíaca (Iwata et al., 2003).
Uno de los aspectos más relevantes de TRPV2 es su expresión en células del sistema inmunológico, como macrófagos, neutrófilos y células dendríticas. En estos contextos, el canal participa en procesos como la fagocitosis, migración celular y respuesta inflamatoria, actuando como un sensor de señales físicas y químicas del entorno. Su activación puede influir en la dinámica del citoesqueleto y en la capacidad de las células inmunes para responder a estímulos externos, lo que lo posiciona como un modulador importante de la inmunidad innata (Link et al., 2010).
Además, TRPV2 se ha identificado en tejidos como hígado, páncreas, pulmón y piel, donde su función aún no está completamente definida, pero se asocia con procesos de homeostasis celular, regulación metabólica y respuesta al estrés. En células epiteliales y endoteliales, su activación puede contribuir a la regulación del volumen celular y a la adaptación frente a cambios osmóticos o mecánicos.
Un rasgo distintivo de TRPV2 es que su actividad funcional depende en gran medida de su localización subcelular. En muchos tipos celulares, el canal se encuentra predominantemente en compartimentos intracelulares y solo se inserta en la membrana plasmática tras la activación de determinadas rutas de señalización, como las mediadas por factores de crecimiento. Esta regulación espacial añade un nivel adicional de control sobre su función, permitiendo que su actividad se module de forma dinámica en función del estado celular (Kanzaki et al., 1999).
En conjunto, la distribución de TRPV2 refleja su papel como un sensor celular multifuncional, implicado en la integración de señales físicas y químicas en múltiples tejidos, con especial relevancia en procesos de adaptación, defensa y mantenimiento de la homeostasis.
Interacción con el sistema endocannabinoide
El canal TRPV2 se considera una de las dianas moleculares no clásicas asociadas al sistema endocannabinoide, ampliando el marco funcional más allá de los receptores cannabinoides tradicionales CB1 y CB2. Su implicación en esta red de señalización deriva principalmente de su capacidad para ser modulado por lípidos bioactivos y determinados fitocannabinoides, lo que lo sitúa dentro del denominado “endocannabinoidome”, un conjunto extendido de mediadores y receptores interconectados (Di Marzo, 2018).
A diferencia de los receptores CB1 y CB2, que pertenecen a la familia de receptores acoplados a proteína G (GPCR), TRPV2 es un canal iónico que permite la entrada de cationes —especialmente Ca²⁺— en respuesta a estímulos específicos. Esta diferencia estructural implica que su activación conduce a respuestas celulares más rápidas y directas, modulando procesos como la excitabilidad celular, la señalización intracelular dependiente de calcio y la dinámica del citoesqueleto.
Entre los compuestos más estudiados en relación con TRPV2 se encuentra el cannabidiol (CBD), que ha demostrado capacidad para modular la actividad de este canal en distintos modelos celulares. A diferencia de su interacción con TRPV1, donde actúa como agonista relativamente bien caracterizado, la relación entre CBD y TRPV2 es más compleja y dependiente del contexto experimental. Algunos estudios sugieren que el CBD puede favorecer la activación o sensibilización de TRPV2, promoviendo la entrada de calcio y desencadenando respuestas celulares específicas, especialmente en células del sistema inmune y en ciertos modelos tumorales (Qin et al., 2008; De Petrocellis et al., 2011).
Además del CBD, otros lípidos endógenos relacionados con el sistema endocannabinoide, como la anandamida (AEA) y derivados del ácido araquidónico, pueden influir indirectamente en la actividad de TRPV2, aunque su afinidad y relevancia fisiológica en este contexto siguen siendo objeto de investigación. Esta interacción indirecta sugiere que TRPV2 podría actuar como un sensor lipídico, integrando señales metabólicas y modulando respuestas celulares adaptativas.
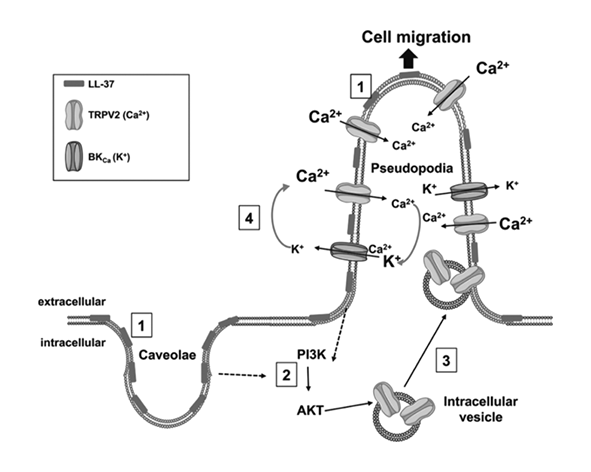
En el ámbito funcional, la activación de TRPV2 en el contexto del sistema endocannabinoide se ha asociado con procesos como la migración celular, la fagocitosis, la regulación de la proliferación y la respuesta inflamatoria. En modelos experimentales, su modulación por cannabinoides ha sido especialmente relevante en estudios sobre células inmunes y células cancerosas, donde la entrada de calcio mediada por TRPV2 puede influir en la viabilidad celular y en la respuesta a estímulos externos.
Sin embargo, es importante destacar que la evidencia disponible es aún heterogénea y en muchos casos preclínica, lo que limita la interpretación directa de estos mecanismos en contextos fisiológicos complejos. La ausencia de agonistas y antagonistas altamente selectivos para TRPV2, junto con su regulación dependiente del entorno celular, dificulta la caracterización precisa de su papel dentro del sistema endocannabinoide.
En conjunto, TRPV2 representa una pieza emergente dentro de la red endocannabinoide ampliada, actuando como un integrador de señales lipídicas y contribuyendo a la complejidad funcional de este sistema más allá de los receptores cannabinoides clásicos.
Farmacología
La farmacología de TRPV2 se caracteriza por ser menos definida y más compleja que la de otros canales TRP, en gran parte debido a la ausencia de ligandos altamente selectivos y a su activación dependiente del contexto celular. A diferencia de TRPV1, que presenta agonistas clásicos bien establecidos como la capsaicina, TRPV2 responde a un conjunto más heterogéneo de estímulos físicos y químicos, lo que ha dificultado la delimitación de su perfil farmacológico (Neeper et al., 2007).
Uno de los rasgos más distintivos de TRPV2 es su activación por temperaturas elevadas, generalmente por encima de los 52 °C, lo que lo sitúa dentro del grupo de termorreceptores de alta intensidad. Sin embargo, en condiciones fisiológicas, esta vía de activación parece tener una relevancia limitada, lo que ha llevado a centrar la investigación en otros mecanismos, como la activación por estrés mecánico, cambios osmóticos y señales lipídicas.
Desde el punto de vista químico, diversos compuestos han mostrado capacidad para modular TRPV2, aunque con baja especificidad. Entre ellos destacan ciertos lípidos endógenos, derivados del ácido araquidónico, que pueden actuar como moduladores indirectos del canal. Asimismo, compuestos sintéticos como el 2-aminoetoxidifenil borato (2-APB) han sido utilizados experimentalmente como activadores de TRPV2, aunque su falta de selectividad —ya que también modula otros canales TRP— limita su utilidad como herramienta farmacológica precisa (Hu et al., 2004).
En el contexto del sistema endocannabinoide ampliado, el cannabidiol (CBD) ha emergido como uno de los moduladores más relevantes de TRPV2. Estudios in vitro han mostrado que el CBD puede facilitar la activación del canal, promoviendo la entrada de calcio en distintos tipos celulares. Esta acción parece depender de múltiples factores, incluyendo la concentración, el tipo celular y la presencia de otras señales intracelulares, lo que sugiere un mecanismo de modulación indirecto o alostérico más que una activación clásica tipo ligando-receptor (Qin et al., 2008; De Petrocellis et al., 2011).
Además, se ha observado que la actividad de TRPV2 puede estar regulada por factores intracelulares, como la fosforilación, la interacción con proteínas del citoesqueleto y la disponibilidad de lípidos de membrana. Estos mecanismos influyen tanto en la sensibilidad del canal como en su localización subcelular, especialmente en su translocación hacia la membrana plasmática, lo que añade una capa adicional de regulación farmacológica.
En modelos experimentales, la modulación de TRPV2 ha sido estudiada en contextos como la respuesta inmunitaria, la función muscular y la proliferación celular, donde la entrada de calcio mediada por este canal puede desencadenar cascadas de señalización relevantes. Sin embargo, la interpretación de estos efectos se ve limitada por la falta de herramientas farmacológicas específicas y por la interacción simultánea con otras dianas moleculares.
En conjunto, la farmacología de TRPV2 refleja un campo en desarrollo, donde la baja selectividad de los moduladores disponibles y la complejidad de su regulación representan desafíos importantes. A pesar de ello, su capacidad para integrar señales físicas y químicas lo posiciona como una diana de interés creciente en investigación básica y aplicada, especialmente en el estudio de procesos celulares dependientes de calcio.
Mecanismos moleculares
El canal TRPV2 actúa como un integrador de señales físicas y químicas a nivel celular, traduciendo estímulos externos en cambios intracelulares principalmente a través de la entrada de calcio (Ca²⁺). Este flujo iónico constituye el evento central de su activación y desencadena una serie de cascadas de señalización que afectan procesos como la dinámica del citoesqueleto, la expresión génica y la respuesta celular adaptativa (Zubcevic et al., 2016).
A diferencia de otros canales TRP más directamente activados por ligandos específicos, TRPV2 presenta un mecanismo de activación multimodal y dependiente del contexto, en el que intervienen factores como la temperatura, el estrés mecánico, señales lipídicas y rutas de señalización intracelular. Esta característica sugiere que TRPV2 no funciona como un sensor aislado, sino como parte de una red de detección integrada que responde a cambios en el entorno celular.
Uno de los aspectos más distintivos de TRPV2 es su translocación regulada hacia la membrana plasmática. En muchas células, el canal se encuentra inicialmente en compartimentos intracelulares y solo se inserta en la membrana tras la activación de determinadas vías de señalización, como las mediadas por factores de crecimiento (por ejemplo, IGF-1). Este proceso implica la reorganización del citoesqueleto y la participación de proteínas de tráfico vesicular, lo que permite que la célula module la disponibilidad funcional del canal en función de sus necesidades (Kanzaki et al., 1999; Shibasaki et al., 2010).
Una vez activado, TRPV2 permite la entrada de Ca²⁺ y otros cationes, lo que conduce a la activación de múltiples rutas intracelulares dependientes de calcio. Entre ellas destacan la activación de quinasas, la modulación de factores de transcripción y la regulación de proteínas implicadas en la migración y adhesión celular. En células inmunes, por ejemplo, este mecanismo está relacionado con procesos como la fagocitosis y la respuesta inflamatoria, mientras que en células musculares puede influir en la contracción y la adaptación al estrés mecánico.
En el contexto del sistema endocannabinoide ampliado, la modulación de TRPV2 por compuestos como el CBD puede alterar estos mecanismos, favoreciendo la entrada de calcio y modificando la señalización intracelular. En modelos celulares, este efecto se ha asociado con cambios en la proliferación, diferenciación y viabilidad celular, especialmente en entornos donde la homeostasis del calcio desempeña un papel crítico (Qin et al., 2008).
Otro componente relevante de los mecanismos moleculares de TRPV2 es su interacción con lípidos de membrana, que pueden influir en su conformación y en su sensibilidad a estímulos. La composición lipídica del entorno celular, incluyendo fosfolípidos y derivados del ácido araquidónico, puede modular la actividad del canal, reforzando su papel como sensor metabólico.
En conjunto, los mecanismos moleculares de TRPV2 reflejan una regulación altamente dinámica y multifactorial, en la que la activación del canal depende tanto de estímulos externos como del estado interno de la célula. Esta complejidad lo sitúa como un elemento clave en la integración de señales celulares, aunque también plantea desafíos significativos para su caracterización experimental precisa.
Importancia en investigación científica
El canal TRPV2 ha emergido como una diana de interés creciente en investigación biomédica debido a su implicación en procesos celulares fundamentales relacionados con la señalización de calcio, la respuesta al estrés y la adaptación tisular. Aunque su caracterización funcional es menos completa que la de otros miembros de la familia TRP, la evidencia acumulada sugiere que TRPV2 desempeña un papel relevante en múltiples contextos fisiológicos y patológicos.
En el ámbito de la inmunología, TRPV2 ha sido estudiado por su participación en procesos como la fagocitosis, la migración celular y la activación de células del sistema inmune. Su capacidad para modular la entrada de calcio en macrófagos y neutrófilos lo posiciona como un regulador potencial de la respuesta inflamatoria y de la inmunidad innata, especialmente en situaciones de daño tisular o infección (Link et al., 2010).
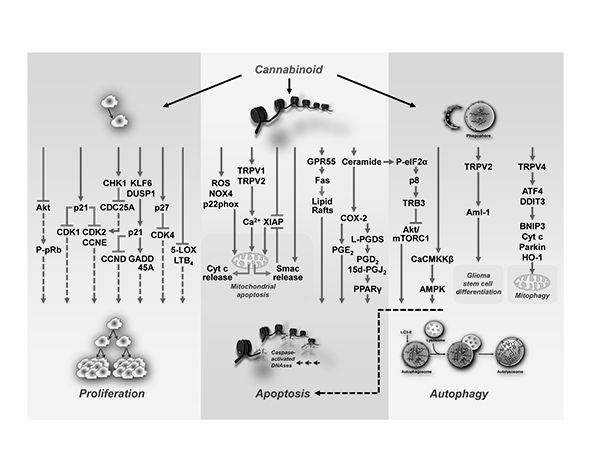
En el campo de la oncología, TRPV2 ha despertado un interés particular debido a su posible implicación en la proliferación, diferenciación y migración de células tumorales. Algunos estudios han observado que la modulación de TRPV2 puede influir en la viabilidad celular y en la sensibilidad a determinados compuestos, incluyendo fitocannabinoides como el CBD. No obstante, estos hallazgos se basan principalmente en modelos preclínicos, y su relevancia clínica aún no está claramente establecida (Qin et al., 2008).
En relación con el sistema muscular y cardiovascular, TRPV2 ha sido vinculado a la regulación del calcio intracelular y a la respuesta al estrés mecánico. Alteraciones en su expresión o localización se han asociado con disfunciones musculares y cardiacas, lo que ha llevado a explorar su papel en patologías como miopatías y enfermedades cardíacas. En estos contextos, TRPV2 podría actuar como un sensor de carga mecánica, contribuyendo a la adaptación estructural del tejido (Iwata et al., 2003).
Además, su integración dentro del concepto de endocannabinoidome ha ampliado el interés por TRPV2 en estudios relacionados con lípidos bioactivos y señalización celular compleja. Su interacción con compuestos endógenos y exógenos refuerza la idea de que los efectos observados en sistemas biológicos no dependen de una única diana, sino de redes interconectadas de receptores, canales y mediadores.
A pesar de estos avances, la investigación sobre TRPV2 se enfrenta a limitaciones importantes, incluyendo la falta de herramientas farmacológicas altamente selectivas y la complejidad de sus mecanismos de regulación. Estas dificultades han contribuido a que su papel fisiológico exacto siga siendo objeto de debate en varios contextos.
En conjunto, TRPV2 representa un campo de estudio en expansión, con implicaciones potenciales en múltiples disciplinas, desde la biología celular básica hasta la investigación traslacional. Su carácter multifuncional y su integración en redes de señalización complejas lo convierten en una diana relevante, aunque aún en fase de consolidación dentro del panorama científico.
Referencias
- Caterina MJ, Rosen TA, Tominaga M, Brake AJ, Julius D. (1999). A capsaicin-receptor homologue with a high threshold for noxious heat. Nature, 398(6726), 436–441. - Neeper MP, Liu Y, Hutchinson TL, Wang Y, Flores CM, Qin N. (2007). Activation properties of heterologously expressed mammalian TRPV2: evidence for species dependence. Journal of Biological Chemistry, 282(21), 15894–15902. - Kanzaki M, Zhang YQ, Mashima H, Li L, Shibata H, Kojima I. (1999). Translocation of a calcium-permeable cation channel induced by insulin-like growth factor-I. Nature Cell Biology, 1(3), 165–170. - Shibasaki K, Murayama N, Ono K, Ishizaki Y, Tominaga M. (2010). TRPV2 enhances axon outgrowth through its activation by membrane stretch in developing sensory and motor neurons. Journal of Neuroscience, 30(13), 4601–4612. - Iwata Y, Katanosaka Y, Arai Y, Shigekawa M, Wakabayashi S. (2003). Dominant-negative inhibition of Ca²⁺ influx via TRPV2 ameliorates muscular dystrophy in animal models. Human Molecular Genetics, 12(24), 2927–2936. - Link TM, Park U, Vonakis BM, Raben DM, Soloski MJ, Caterina MJ. (2010). TRPV2 has a pivotal role in macrophage particle binding and phagocytosis. Nature Immunology, 11(3), 232–239. - Qin N, Neeper MP, Liu Y, Hutchinson TL, Lubin ML, Flores CM. (2008). TRPV2 is activated by cannabidiol and mediates CGRP release in cultured dorsal root ganglion neurons. Journal of Neuroscience, 28(24), 6231–6238. - De Petrocellis L, Ligresti A, Moriello AS, Allarà M, Bisogno T, Petrosino S, Stott CG, Di Marzo V. (2011). Effects of cannabinoids and cannabinoid-enriched Cannabis extracts on TRP channels and endocannabinoid metabolic enzymes. British Journal of Pharmacology, 163(7), 1479–1494. - Hu HZ, Gu Q, Wang C, Colton CK, Tang J, Kinoshita-Kawada M, Lee LY, Wood JD, Zhu MX. (2004). 2-aminoethoxydiphenyl borate is a common activator of TRPV1, TRPV2, and TRPV3. Journal of Biological Chemistry, 279(34), 35741–35748. - Gaudet R. (2008). A primer on ankyrin repeat function in TRP channels and beyond. Molecular BioSystems, 4(5), 372–379. - Liao M, Cao E, Julius D, Cheng Y. (2013). Structure of the TRPV1 ion channel determined by electron cryo-microscopy. Nature, 504(7478), 107–112. - Cao E, Liao M, Cheng Y, Julius D. (2013). TRPV1 structures in distinct conformations reveal activation mechanisms. Nature, 504(7478), 113–118. - Zubcevic L, Herzik MA, Chung BC, Liu Z, Lander GC, Lee SY. (2016). Cryo-electron microscopy structure of the TRPV2 ion channel. Nature Structural & Molecular Biology, 23(2), 180–186. - Di Marzo V. (2018). New approaches and challenges to targeting the endocannabinoid system. Nature Reviews Drug Discovery, 17(9), 623–639.