Introducción
El sistema inmunitario constituye una red altamente especializada de células, tejidos y moléculas encargadas de la defensa del organismo frente a agentes externos y de la vigilancia del equilibrio interno. Su función no se limita únicamente a la eliminación de patógenos, sino que incluye también la detección de células dañadas, la regulación de procesos inflamatorios y la coordinación de respuestas adaptativas que permiten mantener la homeostasis en un entorno biológico dinámico.
En este contexto, el sistema endocannabinoide (SEC) emerge como un modulador clave de la función inmunitaria. A través de receptores, ligandos endógenos y enzimas específicas, el SEC participa en la regulación fina de la activación, proliferación y diferenciación de células inmunes, así como en la modulación de la liberación de citoquinas y mediadores inflamatorios. Esta interacción sitúa al SEC como un sistema de control que contribuye a evitar respuestas inmunes excesivas o desreguladas (Klein, 2005; Turcotte et al., 2016).
La relación entre el sistema inmunitario y el SEC se caracteriza por su carácter bidireccional: mientras el SEC modula la actividad inmune, los procesos inflamatorios pueden alterar la expresión y funcionalidad de los componentes endocannabinoides. Este diálogo dinámico resulta fundamental para comprender fenómenos como la inflamación crónica, la tolerancia inmunológica o la respuesta frente a infecciones, todos ellos objeto de intensa investigación en las últimas décadas (Nagarkatti et al., 2009; Maccarrone et al., 2015).
Historia del descubrimiento
El conocimiento del sistema inmunitario se ha desarrollado a lo largo de más de dos siglos, evolucionando desde observaciones empíricas hasta una comprensión molecular altamente sofisticada. Los primeros avances se remontan a finales del siglo XVIII con los trabajos de Edward Jenner, quien demostró que la exposición controlada a material biológico podía conferir protección frente a infecciones, estableciendo así las bases de la inmunización. Este hito marcó el inicio de una nueva disciplina científica centrada en la defensa del organismo frente a patógenos.
Durante el siglo XIX, figuras como Louis Pasteur y Robert Koch consolidaron la teoría germinal de la enfermedad, identificando microorganismos específicos como causantes de patologías concretas. Este periodo permitió entender que el sistema inmunitario no era un concepto abstracto, sino una respuesta biológica frente a agentes identificables. Paralelamente, Élie Metchnikoff describió la fagocitosis, revelando la existencia de células especializadas capaces de engullir patógenos, lo que dio origen al concepto de inmunidad innata (Metchnikoff, 1905).
A comienzos del siglo XX, el enfoque se amplió con el descubrimiento de la inmunidad humoral, impulsado por investigadores como Paul Ehrlich, quien propuso la teoría de los receptores laterales para explicar la especificidad de los anticuerpos. Este modelo introdujo la idea de reconocimiento molecular específico, base de la inmunidad adaptativa. A partir de este punto, la inmunología comenzó a entenderse como un sistema dual compuesto por mecanismos innatos y adaptativos, interconectados y complementarios (Ehrlich, 1908).
La segunda mitad del siglo XX supuso una revolución conceptual con la identificación de linfocitos T y B, la caracterización del complejo mayor de histocompatibilidad (MHC) y el desarrollo de teorías como la selección clonal propuesta por Frank Macfarlane Burnet. Estos avances permitieron comprender cómo el sistema inmunitario reconoce antígenos específicos y genera memoria inmunológica, consolidando el paradigma moderno de la inmunología (Burnet, 1957).
En paralelo a estos desarrollos, la investigación sobre el cannabis y sus componentes comenzó a revelar conexiones inesperadas con el sistema inmunitario. En la década de 1990, el descubrimiento del receptor CB2, principalmente expresado en células inmunes, marcó un punto de inflexión en la comprensión de la interacción entre el sistema endocannabinoide y la inmunidad. A diferencia del receptor CB1, predominantemente neuronal, CB2 se localiza en linfocitos, macrófagos y otras células del sistema inmunitario, sugiriendo una función reguladora directa sobre la respuesta inmune (Munro et al., 1993).
Posteriormente, la identificación de endocannabinoides como la anandamida (AEA) y el 2-araquidonilglicerol (2-AG) permitió establecer que el organismo produce sus propios ligandos capaces de modular la actividad inmunitaria. Estos compuestos se sintetizan y degradan de forma dinámica en respuesta a estímulos fisiológicos, incluyendo procesos inflamatorios, lo que refuerza la idea de que el SEC actúa como un sistema de ajuste fino dentro del sistema inmunitario (Di Marzo, 1998; Stella, 2010).
En las últimas décadas, la investigación ha profundizado en la interacción entre el SEC y la inmunidad, revelando su papel en la regulación de la inflamación, la migración celular, la liberación de citoquinas y la resolución de procesos inflamatorios. Este enfoque ha llevado a considerar el SEC no como un sistema aislado, sino como un componente integrado dentro de la red inmunológica, con implicaciones en patologías inflamatorias, autoinmunes y neuroinmunológicas (Klein, 2005; Nagarkatti et al., 2009).
Así, la historia del sistema inmunitario no puede entenderse hoy sin incluir la contribución del sistema endocannabinoide como modulador fisiológico, cerrando un ciclo que conecta la inmunología clásica con la biología molecular contemporánea y abriendo nuevas líneas de investigación en el estudio de la homeostasis y la regulación inmunitaria.
Organización del sistema y distribución del SEC
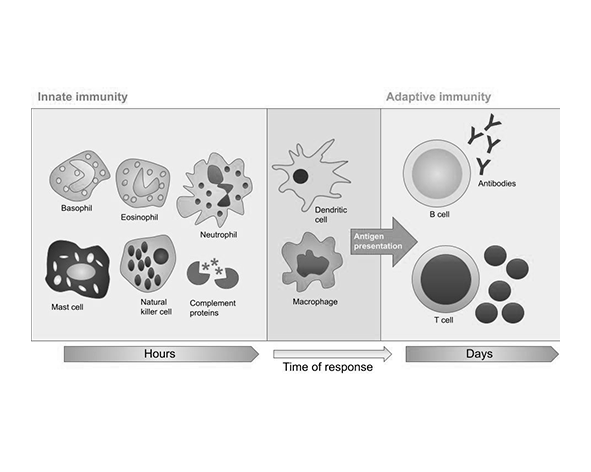
El sistema inmunitario se organiza en una red compleja y jerárquica de órganos, tejidos y células que actúan de forma coordinada para detectar y responder a amenazas, manteniendo al mismo tiempo la tolerancia hacia componentes propios del organismo. Tradicionalmente, se divide en inmunidad innata e inmunidad adaptativa, dos sistemas interdependientes que operan en distintos niveles de especificidad y tiempo de respuesta.
La inmunidad innata constituye la primera línea de defensa y está formada por barreras físicas (piel, mucosas), células fagocíticas como macrófagos y neutrófilos, células dendríticas y células NK (natural killer). Estas células reconocen patrones moleculares conservados mediante receptores de reconocimiento de patrones (PRRs), activando respuestas rápidas e inespecíficas frente a patógenos. Por otro lado, la inmunidad adaptativa, mediada principalmente por linfocitos T y B, se caracteriza por su alta especificidad antigénica y capacidad de generar memoria inmunológica, permitiendo respuestas más eficientes ante exposiciones repetidas (Abbas et al., 2018).
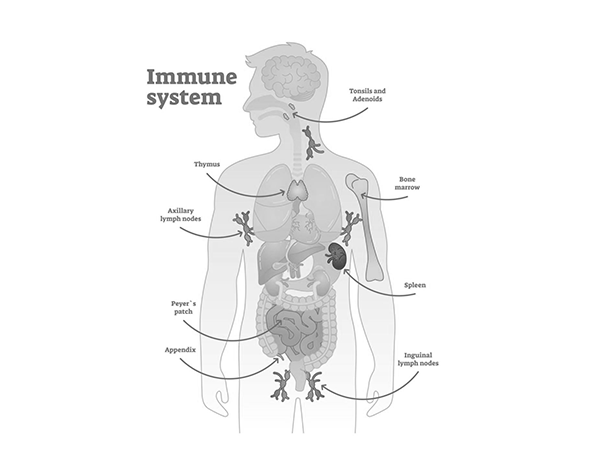
A nivel estructural, el sistema inmunitario se distribuye en órganos primarios y secundarios. Los órganos primarios, como la médula ósea y el timo, son responsables de la generación y maduración de las células inmunes. Los órganos secundarios, incluyendo ganglios linfáticos, bazo y tejido linfoide asociado a mucosas (MALT), actúan como centros de activación y coordinación de la respuesta inmunitaria. Esta organización permite una vigilancia constante del organismo, integrando señales locales y sistémicas en un sistema altamente dinámico.
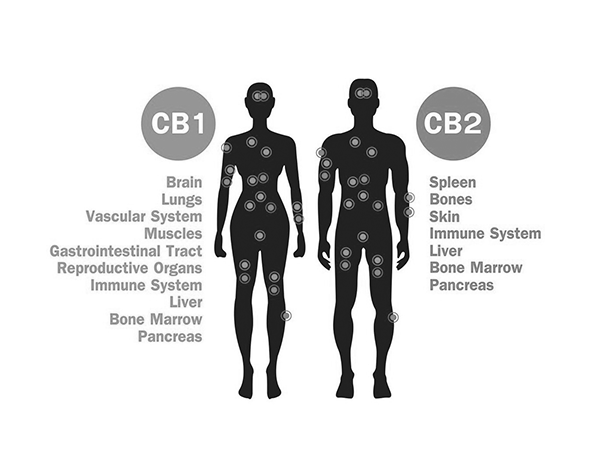
Dentro de esta arquitectura, el sistema endocannabinoide (SEC) se distribuye de manera amplia y estratégica, participando en la regulación de múltiples funciones inmunitarias. El receptor CB2 es el principal mediador del SEC en el sistema inmune y se expresa predominantemente en células inmunitarias como linfocitos B, linfocitos T, macrófagos, monocitos y células dendríticas. Su expresión puede variar en función del estado de activación celular, incrementándose en contextos inflamatorios o de estrés inmunológico (Munro et al., 1993; Turcotte et al., 2016).
Además del CB2, también se ha descrito la presencia de receptores CB1 en ciertas células inmunes, aunque en menor proporción. Este receptor, tradicionalmente asociado al sistema nervioso central, puede desempeñar funciones moduladoras en contextos específicos, lo que sugiere una interconexión funcional entre sistemas fisiológicos aparentemente distintos, como el nervioso y el inmunitario (Klein, 2005).
Los endocannabinoides, principalmente anandamida (AEA) y 2-AG, se sintetizan localmente en células inmunes y tejidos periféricos en respuesta a estímulos fisiológicos. Estas moléculas actúan de forma paracrina o autocrina, modulando procesos como la activación celular, la migración, la fagocitosis y la liberación de mediadores inflamatorios. Su producción no es constante, sino que responde a señales dinámicas del entorno, lo que permite un control preciso y localizado de la respuesta inmunitaria (Di Marzo, 1998; Stella, 2010).
En paralelo, las enzimas responsables de la síntesis y degradación de endocannabinoides, como FAAH y MAGL, también están presentes en células del sistema inmunitario, regulando la disponibilidad de estos ligandos y, por tanto, su efecto biológico. Esta regulación enzimática añade una capa adicional de control que contribuye a la fine-tuning del sistema (Blankman et al., 2007).
Un aspecto especialmente relevante es la expresión diferencial del SEC en distintos estados fisiológicos y patológicos. En situaciones de inflamación crónica, infecciones o enfermedades autoinmunes, se ha observado una alteración en la expresión de receptores cannabinoides y en los niveles de endocannabinoides, lo que sugiere que el SEC forma parte de los mecanismos adaptativos del sistema inmunitario frente a desequilibrios internos (Nagarkatti et al., 2009).
En conjunto, la distribución del SEC dentro del sistema inmunitario no es uniforme ni estática, sino altamente dinámica y dependiente del contexto biológico. Esta integración funcional posiciona al SEC como un modulador clave de la respuesta inmunitaria, actuando como un sistema de ajuste que contribuye a equilibrar activación y resolución, inflamación y tolerancia.
Mecanismos de interacción con el SEC
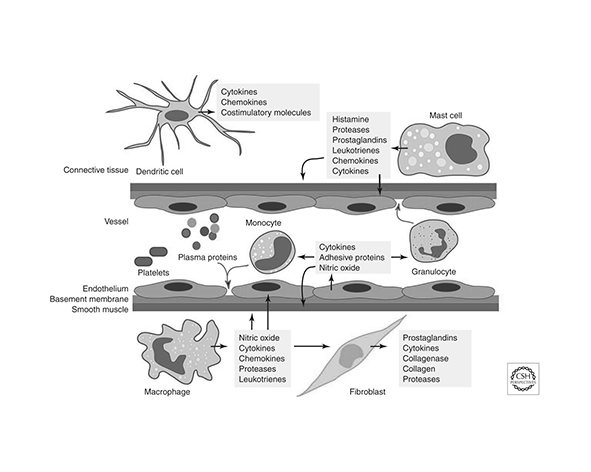
La interacción entre el sistema inmunitario y el sistema endocannabinoide (SEC) se basa en una red de mecanismos moleculares que regulan la activación, comunicación y resolución de la respuesta inmune. Estos mecanismos no actúan como un interruptor binario, sino como un sistema de modulación fina que ajusta la intensidad y duración de la respuesta inmunitaria en función del contexto fisiológico.
Uno de los principales ejes de interacción es la señalización mediada por el receptor CB2, cuya activación en células inmunes induce cambios en cascadas intracelulares asociadas a proteínas G. Esta activación suele traducirse en una inhibición de la adenilato ciclasa, reducción de los niveles de AMPc y modulación de rutas como MAPK y PI3K/Akt, lo que afecta directamente a procesos como la proliferación celular, la supervivencia y la producción de mediadores inflamatorios (Turcotte et al., 2016; Klein, 2005).
A nivel funcional, la activación del SEC tiende a ejercer un efecto inmunomodulador que, en muchos contextos experimentales, se asocia con una disminución de la respuesta inflamatoria. Esto incluye la reducción en la liberación de citoquinas proinflamatorias como TNF-α, IL-1β o IL-6, así como el aumento relativo de citoquinas con perfil regulador. Este equilibrio no implica una supresión completa del sistema inmunitario, sino una reorientación de la respuesta hacia estados menos reactivos y más controlados (Nagarkatti et al., 2009).
Otro mecanismo relevante es la regulación de la migración y reclutamiento celular. Los endocannabinoides pueden influir en la expresión de moléculas de adhesión y quimiocinas, alterando la capacidad de las células inmunes para desplazarse hacia sitios de inflamación o daño tisular. Este efecto tiene implicaciones directas en procesos como la infiltración celular en tejidos inflamados o la resolución de respuestas inmunes prolongadas (Maccarrone et al., 2015).
La fagocitosis y la actividad microbicida de células como macrófagos y neutrófilos también pueden verse moduladas por el SEC. Dependiendo del contexto, la activación de receptores cannabinoides puede alterar la capacidad de estas células para internalizar patógenos o producir especies reactivas de oxígeno, lo que sugiere un papel en la regulación del equilibrio entre defensa y daño tisular (Cabral & Griffin-Thomas, 2009).
En el ámbito de la inmunidad adaptativa, el SEC interviene en la activación y diferenciación de linfocitos T. Se ha observado que puede influir en el balance entre subpoblaciones como Th1, Th2, Th17 y Treg, modulando así la dirección de la respuesta inmunitaria. Este aspecto es especialmente relevante en contextos de inflamación crónica o autoinmunidad, donde un desequilibrio en estas subpoblaciones puede contribuir a la patogénesis (Klein, 2005; Nagarkatti et al., 2009).
Además, el SEC participa en la regulación de la apoptosis y la supervivencia celular. La activación de receptores cannabinoides puede inducir muerte celular programada en determinadas poblaciones inmunes o, por el contrario, favorecer la supervivencia en otros contextos. Esta dualidad depende del tipo celular, del microambiente y del estado de activación, lo que refuerza la idea de que el SEC actúa como un modulador contextual (Maccarrone et al., 2015).
Otro aspecto clave es su papel en la resolución de la inflamación. Más allá de limitar la respuesta inicial, el SEC parece estar implicado en las fases tardías del proceso inflamatorio, favoreciendo la restauración del equilibrio tisular. Este rol lo sitúa dentro de los sistemas que participan en la terminación activa de la inflamación, junto a otros mediadores lipídicos especializados (Serhan et al., 2008).
Por último, la interacción del SEC con otros sistemas de señalización amplía su impacto sobre la inmunidad. Receptores como TRPV1 o GPR55, así como la interacción con vías relacionadas con eicosanoides, refuerzan la idea de que el SEC forma parte de una red más amplia de regulación fisiológica, donde múltiples sistemas convergen para modular la respuesta inmunitaria (Di Marzo, 1998; Pertwee, 2010).
En conjunto, estos mecanismos reflejan que el SEC no actúa como un sistema inmunosupresor clásico, sino como un modulador dinámico que ajusta la respuesta inmunitaria en función de las necesidades del organismo, contribuyendo a mantener el equilibrio entre defensa eficaz y control del daño inflamatorio.
Funciones fisiológicas
El sistema inmunitario desempeña un papel esencial en el mantenimiento de la homeostasis del organismo, no solo como mecanismo de defensa frente a agentes patógenos, sino también como regulador activo de procesos fisiológicos fundamentales. En este contexto, la interacción con el sistema endocannabinoide (SEC) permite ajustar de forma dinámica funciones clave como la inflamación, la vigilancia inmunológica y la reparación tisular.
Una de las funciones centrales del sistema inmunitario es la detección y eliminación de agentes extraños, incluyendo bacterias, virus, hongos y parásitos. A través de mecanismos innatos y adaptativos, el organismo reconoce patrones moleculares asociados a patógenos y activa respuestas coordinadas para neutralizarlos. El SEC interviene en este proceso modulando la intensidad de la respuesta, evitando tanto una activación insuficiente como una reacción excesiva que pueda derivar en daño tisular (Klein, 2005; Turcotte et al., 2016).
La regulación de la inflamación constituye otra función fisiológica crítica. La inflamación es un proceso necesario para contener infecciones y reparar tejidos dañados, pero su desregulación puede conducir a patologías crónicas. El SEC participa en la modulación de este equilibrio, contribuyendo a limitar la producción de mediadores proinflamatorios y favoreciendo la transición hacia fases de resolución. Esta capacidad de ajuste fino resulta especialmente relevante en contextos donde la inflamación persistente puede comprometer la función de órganos y sistemas (Nagarkatti et al., 2009).
El sistema inmunitario también desempeña un papel en la homeostasis tisular y la reparación, eliminando células dañadas y facilitando procesos de regeneración. En este contexto, el SEC puede influir en la actividad de células implicadas en la reparación, como macrófagos y células estromales, modulando la liberación de factores que intervienen en la regeneración tisular. Esta función conecta la inmunidad con procesos más amplios de mantenimiento estructural del organismo (Maccarrone et al., 2015).
Otra función relevante es la vigilancia inmunológica frente a células alteradas, incluyendo aquellas que presentan transformaciones potencialmente tumorales. El sistema inmunitario es capaz de identificar y eliminar células con alteraciones en su superficie, contribuyendo a la prevención de procesos patológicos. El SEC puede modular esta vigilancia, aunque su papel exacto depende del contexto y sigue siendo objeto de investigación activa (Klein, 2005).
La tolerancia inmunológica representa un aspecto fundamental para evitar respuestas contra componentes propios del organismo. Este mecanismo permite distinguir entre lo propio y lo extraño, evitando la activación de respuestas autoinmunes. El SEC participa en la regulación de este equilibrio, influyendo en la actividad de linfocitos reguladores y en la producción de señales que limitan la activación excesiva del sistema inmunitario (Nagarkatti et al., 2009).
Asimismo, el sistema inmunitario interactúa de forma estrecha con otros sistemas fisiológicos, incluyendo el sistema nervioso y el endocrino. Esta comunicación bidireccional permite integrar señales del entorno interno y externo, coordinando respuestas adaptativas a nivel sistémico. El SEC actúa como un puente funcional en esta integración, facilitando la comunicación entre sistemas y contribuyendo a una regulación global del organismo (Di Marzo, 1998).
En conjunto, las funciones fisiológicas del sistema inmunitario no pueden entenderse como procesos aislados, sino como parte de una red interconectada donde el SEC desempeña un papel modulador clave. Esta interacción permite mantener un equilibrio dinámico entre defensa, regulación y reparación, asegurando la estabilidad del entorno interno frente a desafíos constantes.
Implicaciones en investigación
El estudio de la interacción entre el sistema inmunitario y el sistema endocannabinoide (SEC) ha abierto nuevas líneas de investigación en inmunología, biología molecular y medicina traslacional. Lejos de interpretarse como un sistema con funciones aisladas, el SEC se considera actualmente un modulador integrado dentro de las redes de señalización que regulan la respuesta inmunitaria, con implicaciones en múltiples contextos fisiológicos y patológicos.
Uno de los principales focos de investigación es el papel del SEC en la regulación de la inflamación crónica. Diversos estudios han observado que alteraciones en la señalización endocannabinoide pueden asociarse con estados inflamatorios persistentes, característicos de enfermedades complejas. En este sentido, la modulación de receptores como CB2 y de enzimas implicadas en el metabolismo de endocannabinoides se ha estudiado como una vía potencial para comprender cómo se regula la intensidad y duración de la respuesta inflamatoria (Nagarkatti et al., 2009; Turcotte et al., 2016).
Otro campo relevante es la investigación en enfermedades autoinmunes, donde el sistema inmunitario pierde la capacidad de distinguir entre lo propio y lo extraño. El SEC ha sido objeto de estudio en modelos experimentales que analizan su influencia sobre la activación de linfocitos y la producción de citoquinas, así como su posible papel en el equilibrio entre subpoblaciones celulares implicadas en la tolerancia inmunológica. Estos trabajos no establecen aplicaciones clínicas directas, pero sí contribuyen a comprender los mecanismos subyacentes a la desregulación inmunitaria (Klein, 2005; Maccarrone et al., 2015).
En el ámbito de la neuroinmunología, la interacción entre el sistema nervioso y el sistema inmunitario ha cobrado especial relevancia. El SEC, al estar presente en ambos sistemas, actúa como un punto de conexión funcional que puede influir en procesos donde confluyen señales neuronales e inmunes. Este enfoque ha permitido explorar cómo la señalización endocannabinoide participa en la comunicación entre cerebro y sistema inmunitario, especialmente en contextos de inflamación o estrés fisiológico (Di Marzo, 1998; Stella, 2010).
La investigación también ha abordado el papel del SEC en la respuesta frente a infecciones, analizando cómo la modulación de la actividad inmunitaria puede influir en la capacidad del organismo para responder a patógenos. Estos estudios han puesto de manifiesto que el efecto del SEC es altamente dependiente del contexto, pudiendo variar en función del tipo de patógeno, del estado del sistema inmunitario y del entorno tisular (Cabral & Griffin-Thomas, 2009).
Otro aspecto de interés es la participación del SEC en los procesos de resolución de la inflamación, un campo emergente que se centra en cómo el organismo finaliza de forma activa las respuestas inflamatorias. En este sentido, los endocannabinoides se han relacionado con mecanismos que favorecen la restauración del equilibrio tisular, integrándose dentro de redes más amplias de mediadores lipídicos implicados en la homeostasis (Serhan et al., 2008).
Además, el desarrollo de herramientas analíticas y modelos experimentales ha permitido profundizar en la regulación enzimática del SEC, incluyendo enzimas como FAAH y MAGL. La investigación en este ámbito busca comprender cómo la modulación de la disponibilidad de endocannabinoides puede influir en la función inmunitaria, aportando información sobre los mecanismos de control interno del sistema (Blankman et al., 2007).
En conjunto, las implicaciones en investigación del SEC en el sistema inmunitario no apuntan a respuestas simples, sino a un campo en expansión donde convergen múltiples disciplinas. El interés científico se centra en desentrañar cómo este sistema contribuye a la regulación fina de la inmunidad, aportando un marco conceptual que permita entender mejor los procesos de inflamación, tolerancia y homeostasis desde una perspectiva integradora.
Véase también
- Sistema endocannabinoide
- Homeostasis
- Señalización endocannabinoide
- Receptor CB2
- Anandamida
- 2-araquidonilglicerol
Referencias
- Abbas AK, Lichtman AH, Pillai S. (2018). Cellular and Molecular Immunology. Elsevier. - Blankman JL, Simon GM, Cravatt BF. (2007). A comprehensive profile of brain enzymes that hydrolyze the endocannabinoids 2-arachidonoylglycerol and anandamide. Chemistry & Biology. - Burnet FM. (1957). A modification of Jerne’s theory of antibody production using the concept of clonal selection. CA: A Cancer Journal for Clinicians. - Cabral GA, Griffin-Thomas L. (2009). Emerging role of the cannabinoid receptor CB2 in immune regulation. Expert Reviews in Molecular Medicine. - Di Marzo V. (1998). ‘Endocannabinoids’ and other fatty acid derivatives with cannabimimetic properties: biochemistry and possible physiopathological relevance. Biochimica et Biophysica Acta. - Ehrlich P. (1908). The theory of immunity. Nobel Lecture. - Jenner E. (1798). An inquiry into the causes and effects of the variolae vaccinae. - Klein TW. (2005). Cannabinoid-based drugs as anti-inflammatory therapeutics. Nature Reviews Immunology. - Maccarrone M, Bab I, Bíró T, et al. (2015). Endocannabinoid signaling at the periphery: 50 years after THC. Trends in Pharmacological Sciences. - Metchnikoff E. (1905). Immunity in Infectious Diseases. Cambridge University Press. - Munro S, Thomas KL, Abu-Shaar M. (1993). Molecular characterization of a peripheral receptor for cannabinoids. Nature. - Nagarkatti P, Pandey R, Rieder SA, Hegde VL, Nagarkatti M. (2009). Cannabinoids as novel anti-inflammatory drugs. Future Medicinal Chemistry. - Serhan CN, Chiang N, Van Dyke TE. (2008). Resolving inflammation: dual anti-inflammatory and pro-resolution lipid mediators. Nature Reviews Immunology. - Stella N. (2010). Cannabinoid signaling in glial cells. Glia. - Turcotte C, Blanchet MR, Laviolette M, Flamand N. (2016). The CB2 receptor and its role as a regulator of inflammation. Cellular and Molecular Life Sciences.