INTRODUCCIÓN
La señalización endocannabinoide constituye uno de los sistemas de comunicación celular más versátiles del organismo, basado en la síntesis, liberación y reconocimiento de lípidos bioactivos que actúan como mensajeros intercelulares. A diferencia de los neurotransmisores clásicos, los endocannabinoides no se almacenan en vesículas, sino que se producen “a demanda” a partir de fosfolípidos de membrana en respuesta a cambios en la actividad celular, lo que les permite actuar como moduladores dinámicos de múltiples procesos fisiológicos (Di Marzo et al., 1998; Piomelli, 2003).
Este sistema de señalización está compuesto principalmente por tres elementos: los receptores cannabinoides (principalmente CB1 y CB2), los ligandos endógenos como la anandamida (AEA) y el 2-araquidonoilglicerol (2-AG), y las enzimas responsables de su síntesis y degradación, como la NAPE-PLD, DAGL, FAAH y MAGL. La interacción coordinada entre estos componentes permite regular funciones tan diversas como la neurotransmisión, la respuesta inmune, el metabolismo energético o la homeostasis tisular (Lu & Mackie, 2016; Kano et al., 2009).
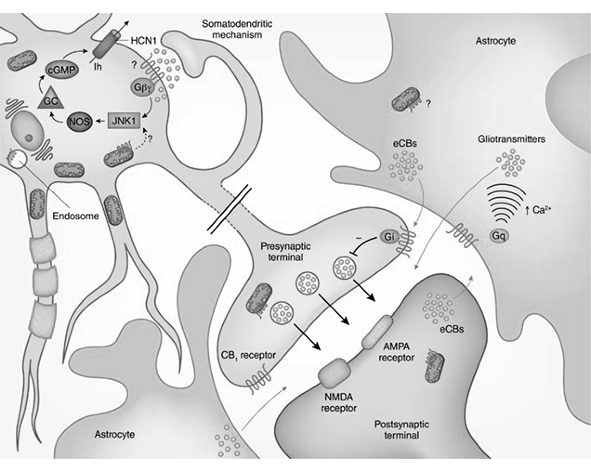
Uno de los aspectos más característicos de la señalización endocannabinoide es su naturaleza retrógrada en el sistema nervioso: los endocannabinoides se liberan desde la neurona postsináptica y actúan sobre receptores presinápticos, modulando la liberación de neurotransmisores como glutamato o GABA. Este mecanismo introduce un nivel adicional de control fino sobre la actividad sináptica, permitiendo al sistema nervioso ajustar su propia excitabilidad en tiempo real (Wilson & Nicoll, 2002; Kano et al., 2009).
Más allá del sistema nervioso, la señalización endocannabinoide opera en múltiples tejidos periféricos, donde participa en la regulación de procesos inflamatorios, la función inmunitaria, la señalización metabólica y la comunicación entre órganos. Esta amplia distribución funcional ha llevado a considerar al sistema endocannabinoide como un modulador global de la homeostasis biológica, actuando como un sistema de ajuste fino frente a perturbaciones internas y externas (Di Marzo & Piscitelli, 2015).
En conjunto, la señalización endocannabinoide no debe entenderse como una vía lineal, sino como una red compleja, adaptable y altamente contextual, cuya actividad depende del estado fisiológico, del tipo celular y de las condiciones del entorno. Su estudio ha transformado la comprensión de la comunicación celular en las últimas décadas y continúa siendo un área clave en la investigación biomédica contemporánea.
COMPONENTES DE LA SEÑALIZACIÓN ENDOCANNABINOIDE
La señalización endocannabinoide se organiza a partir de un conjunto bien definido de componentes moleculares que actúan de forma coordinada: receptores cannabinoides, ligandos endógenos (endocannabinoides) y enzimas encargadas de su síntesis y degradación. A diferencia de otros sistemas de señalización más lineales, este sistema presenta una arquitectura descentralizada y altamente dinámica, donde cada elemento se activa en función del contexto fisiológico y del estado celular (Lu & Mackie, 2016).
Receptores cannabinoides
Los principales mediadores de la señalización endocannabinoide son los receptores cannabinoides tipo 1 (CB1) y tipo 2 (CB2), ambos pertenecientes a la familia de los receptores acoplados a proteína G (GPCR). El receptor CB1 se expresa predominantemente en el sistema nervioso central, especialmente en regiones como la corteza cerebral, el hipocampo, los ganglios basales y el cerebelo, donde modula la liberación de neurotransmisores y la excitabilidad neuronal. Por su parte, el receptor CB2 se localiza principalmente en células del sistema inmunitario y tejidos periféricos, donde participa en la regulación de procesos inflamatorios y de respuesta inmune (Pertwee, 2008; Atwood & Mackie, 2010).
Ambos receptores se acoplan principalmente a proteínas Gi/o, lo que conduce a la inhibición de la adenilato ciclasa, la disminución de los niveles de AMPc y la modulación de canales iónicos, incluyendo la inhibición de canales de calcio tipo N y P/Q y la activación de canales de potasio. Este conjunto de efectos reduce la probabilidad de liberación de neurotransmisores en terminales presinápticas, constituyendo la base de la señalización retrógrada característica del sistema endocannabinoide (Howlett et al., 2002; Kano et al., 2009).
Además de CB1 y CB2, se han identificado otros posibles mediadores de la señalización endocannabinoide, como el receptor TRPV1, ciertos receptores acoplados a proteína G huérfanos (como GPR55) y receptores nucleares como PPARs, lo que sugiere que el sistema endocannabinoide se extiende más allá de sus componentes clásicos y forma parte de una red de señalización lipídica más amplia (Di Marzo & De Petrocellis, 2010).
Endocannabinoides
Los principales ligandos endógenos del sistema son la anandamida (AEA) y el 2-araquidonoilglicerol (2-AG), ambos derivados de ácidos grasos poliinsaturados. Aunque comparten afinidad por los receptores cannabinoides, presentan diferencias relevantes en su concentración, eficacia y funciones fisiológicas. El 2-AG se encuentra en concentraciones más elevadas en el cerebro y actúa como agonista completo de CB1 y CB2, mientras que la anandamida se comporta como un agonista parcial con afinidad más selectiva y funciones más moduladoras (Sugiura et al., 2002; Mechoulam & Parker, 2013).
A diferencia de neurotransmisores clásicos, los endocannabinoides no se almacenan previamente en vesículas, sino que se sintetizan de novo a partir de fosfolípidos de membrana en respuesta a señales intracelulares, como aumentos en el calcio o la activación de receptores acoplados a proteína G. Esta característica permite una regulación temporal muy precisa y localizada de la señalización (Piomelli, 2003).
Enzimas de síntesis y degradación
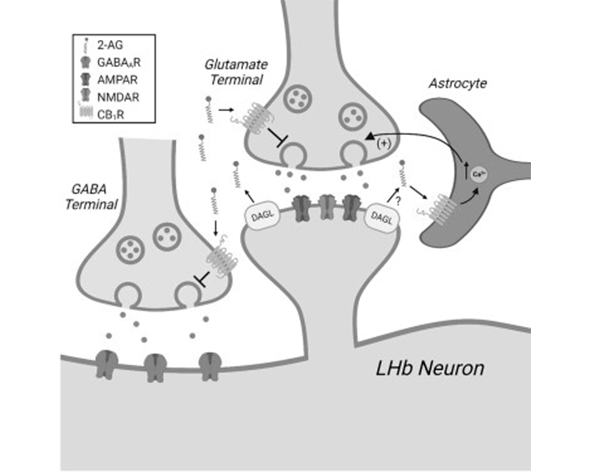
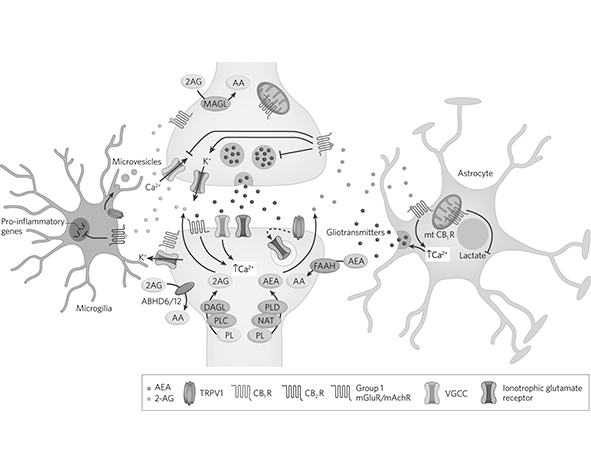
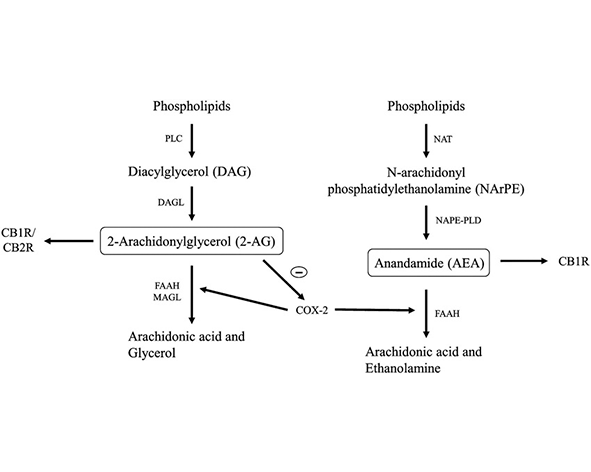
La señalización endocannabinoide está fuertemente regulada por enzimas que controlan la disponibilidad de sus ligandos. La anandamida se sintetiza principalmente a partir de N-acilfosfatidiletanolaminas (NAPE) mediante la enzima NAPE-PLD, mientras que el 2-AG se genera a partir de diacilglicerol (DAG) por acción de la diacilglicerol lipasa (DAGL). Estas rutas permiten la producción rápida de endocannabinoides en respuesta a estímulos celulares (Okamoto et al., 2004; Bisogno et al., 2003).
En cuanto a la degradación, la anandamida es hidrolizada principalmente por la enzima FAAH (Fatty Acid Amide Hydrolase), mientras que el 2-AG es degradado principalmente por la monoacilglicerol lipasa (MAGL). Este control enzimático asegura que la señalización endocannabinoide sea transitoria y espacialmente restringida, evitando una activación prolongada de los receptores (Cravatt et al., 1996; Dinh et al., 2002).
La existencia de estas enzimas no solo limita la duración de la señal, sino que también permite modular el sistema mediante inhibición enzimática, una estrategia ampliamente estudiada en investigación biomédica.
MECANISMOS DE SEÑALIZACIÓN ENDOCANNABINOIDE
La señalización endocannabinoide se caracteriza por un conjunto de mecanismos no convencionales que la diferencian de otros sistemas de neurotransmisión. Su rasgo más distintivo es la señalización retrógrada, aunque también incluye formas de señalización autocrina, paracrina y modulaciones a nivel intracelular, lo que convierte al sistema endocannabinoide en una red de regulación altamente flexible y dependiente del contexto fisiológico (Kano et al., 2009; Castillo et al., 2012).
Señalización retrógrada
En el sistema nervioso central, los endocannabinoides actúan principalmente como mensajeros retrógrados. A diferencia de la neurotransmisión clásica —donde la señal fluye desde la neurona presináptica hacia la postsináptica—, los endocannabinoides se sintetizan en la neurona postsináptica y viajan hacia atrás a través de la hendidura sináptica para unirse a receptores CB1 localizados en la terminal presináptica (Wilson & Nicoll, 2002).
Este proceso se inicia generalmente tras un aumento de calcio intracelular o la activación de receptores acoplados a proteína G en la neurona postsináptica. Como consecuencia, se activan enzimas como DAGL o NAPE-PLD, que generan endocannabinoides de novo. Una vez liberados, estos lípidos difunden a través de la membrana y se unen a los receptores CB1 presinápticos, provocando una inhibición de la liberación de neurotransmisores (Kano et al., 2009).
El resultado funcional es una retroalimentación negativa que permite a la neurona postsináptica regular su propia entrada sináptica, ajustando dinámicamente la intensidad de la señal.
Supresión de la inhibición y de la excitación (DSI y DSE)
Dos de los fenómenos más estudiados en la señalización endocannabinoide son la supresión de la inhibición inducida por despolarización (DSI, Depolarization-Induced Suppression of Inhibition) y la supresión de la excitación inducida por despolarización (DSE, Depolarization-Induced Suppression of Excitation).
En el caso de la DSI, la liberación de endocannabinoides desde la neurona postsináptica inhibe la liberación de GABA en la terminal presináptica, reduciendo la inhibición y aumentando la excitabilidad neuronal. Por el contrario, en la DSE, los endocannabinoides reducen la liberación de glutamato, disminuyendo la excitación (Kreitzer & Regehr, 2001; Ohno-Shosaku et al., 2001).
Ambos mecanismos son transitorios (de segundos a minutos) y dependen de la actividad neuronal, lo que permite un control fino y reversible de la transmisión sináptica.
Plasticidad sináptica mediada por endocannabinoides
Más allá de efectos a corto plazo, los endocannabinoides también participan en formas de plasticidad sináptica a largo plazo, como la depresión a largo plazo (LTD, Long-Term Depression). En este contexto, la activación repetida de receptores CB1 conduce a una reducción sostenida en la liberación de neurotransmisores, modificando la fuerza de la conexión sináptica (Chevaleyre et al., 2006).
Este tipo de plasticidad está implicado en procesos como el aprendizaje, la memoria, la adaptación al entorno y la regulación de circuitos neuronales. La participación del sistema endocannabinoide en estos procesos refuerza su papel como modulador clave de la función cerebral.
Señalización extracerebral y periférica
Aunque gran parte de la investigación se ha centrado en el sistema nervioso, los mecanismos de señalización endocannabinoide también operan en tejidos periféricos mediante interacciones autocrinas y paracrinas. En estos contextos, las células producen endocannabinoides que actúan sobre receptores cercanos o sobre sí mismas, modulando funciones como la respuesta inmune, la inflamación, la señalización metabólica o la comunicación intercelular (Di Marzo & Piscitelli, 2015).
Por ejemplo, en células inmunitarias, la activación de CB2 puede modular la liberación de citoquinas y la migración celular, mientras que en tejidos metabólicos como el tejido adiposo o el hígado, la señalización endocannabinoide influye en procesos relacionados con el balance energético.
Terminación de la señal
La señalización endocannabinoide es inherentemente transitoria y está estrictamente regulada por mecanismos de degradación enzimática. Tras su acción, los endocannabinoides son captados por las células y degradados rápidamente por enzimas como FAAH (para la anandamida) y MAGL (para el 2-AG), lo que limita su difusión y duración (Cravatt et al., 1996; Dinh et al., 2002).
Este control asegura que la señal no se prolongue innecesariamente y permite que el sistema responda con rapidez a nuevos estímulos.
DISTRIBUCIÓN Y CONTEXTO FISIOLÓGICO DE LA SEÑALIZACIÓN ENDOCANNABINOIDE
La señalización endocannabinoide no se limita a un órgano o sistema específico, sino que está ampliamente distribuida en el organismo, donde actúa como un modulador transversal de múltiples funciones fisiológicas. Esta distribución refleja su papel como sistema de ajuste fino, capaz de integrar señales celulares y coordinar respuestas adaptativas en distintos tejidos (Di Marzo & Piscitelli, 2015).
Sistema nervioso central
El sistema nervioso central representa uno de los principales escenarios de la señalización endocannabinoide, especialmente a través del receptor CB1, cuya expresión es particularmente elevada en regiones como la corteza cerebral, el hipocampo, los ganglios basales, el cerebelo y el hipotálamo. En estas áreas, el sistema endocannabinoide modula la liberación de neurotransmisores y participa en procesos como la plasticidad sináptica, el aprendizaje, la memoria y la regulación del comportamiento (Herkenham et al., 1990; Kano et al., 2009).
La localización predominante de CB1 en terminales presinápticas permite que los endocannabinoides actúen como reguladores de la excitabilidad neuronal, ajustando la intensidad de la señal sináptica en función de la actividad. Este control fino contribuye a mantener el equilibrio entre excitación e inhibición en circuitos neuronales complejos.
Sistema nervioso periférico
En el sistema nervioso periférico, la señalización endocannabinoide también desempeña un papel relevante, especialmente en la modulación de la transmisión sensorial y la comunicación entre tejidos. Los receptores cannabinoides se encuentran en neuronas sensoriales, fibras aferentes y estructuras periféricas, donde pueden influir en la señalización nociceptiva y en la respuesta a estímulos externos (Pertwee, 2001).
Además, en tejidos periféricos, los endocannabinoides pueden actuar localmente mediante mecanismos autocrinos y paracrinos, modulando la actividad celular sin necesidad de una transmisión sináptica clásica.
Sistema inmunitario
El sistema inmunitario constituye otro eje fundamental de la señalización endocannabinoide, principalmente a través del receptor CB2. Este receptor se expresa en células como linfocitos, macrófagos y células dendríticas, donde participa en la regulación de la respuesta inmune y en la comunicación entre células del sistema (Atwood & Mackie, 2010).
La activación de CB2 se ha asociado con la modulación de la liberación de citoquinas, la migración celular y la activación inmunitaria, lo que sugiere un papel en la regulación de procesos inflamatorios y en el mantenimiento del equilibrio inmunológico.
Tejidos metabólicos
La señalización endocannabinoide también está presente en órganos implicados en el metabolismo energético, como el hígado, el tejido adiposo, el páncreas y el músculo esquelético. En estos tejidos, el sistema endocannabinoide participa en la regulación del apetito, el almacenamiento de energía, la sensibilidad a la insulina y el metabolismo lipídico (Pagotto et al., 2006).
Por ejemplo, en el hipotálamo, los endocannabinoides están implicados en la regulación del comportamiento alimentario, mientras que en el tejido adiposo pueden influir en la lipogénesis y en la señalización metabólica. Esta integración sugiere que el sistema endocannabinoide actúa como un puente entre la señalización neuronal y el estado metabólico del organismo.
Piel, tracto gastrointestinal y otros tejidos
Más allá de los sistemas clásicos, la señalización endocannabinoide también se ha identificado en la piel, el tracto gastrointestinal, el sistema reproductivo y otros tejidos periféricos. En la piel, por ejemplo, los receptores cannabinoides están implicados en la regulación de la proliferación celular y la función de barrera, mientras que en el tracto gastrointestinal participan en la motilidad y la comunicación neuroinmunitaria (Izzo & Sharkey, 2010).
Esta presencia ubicua refuerza la idea de que el sistema endocannabinoide no actúa como un sistema aislado, sino como una red de señalización distribuida que contribuye a la integración funcional del organismo.
Contexto fisiológico y adaptación
Un aspecto clave de la señalización endocannabinoide es su carácter dependiente del contexto. La actividad del sistema varía en función del estado fisiológico, el tipo celular, el entorno metabólico y las condiciones externas. En situaciones de estrés, desequilibrio o demanda funcional elevada, la señalización endocannabinoide puede ajustarse para contribuir a la restauración del equilibrio interno (homeostasis).
Este comportamiento adaptativo ha llevado a considerar al sistema endocannabinoide como un modulador “on demand”, cuya activación no es constante, sino que responde a necesidades específicas del organismo.
INTEGRACIÓN FUNCIONAL Y PAPEL EN LA HOMEOSTASIS
La señalización endocannabinoide no actúa como un sistema aislado, sino como una red integradora que conecta múltiples niveles de organización biológica, desde la actividad molecular hasta la función de sistemas completos. Su principal característica es su capacidad para modular procesos fisiológicos de forma contextual, contribuyendo al mantenimiento de la homeostasis, entendida como el equilibrio dinámico del organismo frente a cambios internos y externos (Di Marzo & Piscitelli, 2015).
Un sistema modulador “on demand”
A diferencia de otros sistemas de señalización con actividad basal constante, el sistema endocannabinoide se activa principalmente bajo demanda. La síntesis de endocannabinoides ocurre en respuesta a estímulos específicos, como cambios en la actividad neuronal, alteraciones metabólicas o señales inflamatorias. Esta activación localizada y transitoria permite una regulación precisa, evitando una intervención innecesaria en condiciones de equilibrio (Piomelli, 2003).
Este carácter “on demand” convierte al sistema endocannabinoide en un modulador fino más que en un sistema efector primario, ajustando la intensidad y duración de las respuestas celulares sin imponer una dirección única.
Regulación del equilibrio excitación-inhibición
En el sistema nervioso, uno de los papeles clave de la señalización endocannabinoide es mantener el equilibrio entre excitación e inhibición. A través de mecanismos como la DSI y la DSE, los endocannabinoides permiten a las neuronas ajustar la liberación de neurotransmisores en función de la actividad sináptica, evitando tanto la sobreexcitación como la inhibición excesiva (Kano et al., 2009).
Este equilibrio es esencial para la estabilidad de los circuitos neuronales y para la correcta función de procesos como la percepción, la memoria o la coordinación motora.
Coordinación entre sistemas fisiológicos
La amplia distribución de los componentes del sistema endocannabinoide permite la comunicación entre distintos sistemas fisiológicos. Por ejemplo, la interacción entre señalización neuronal, respuesta inmunitaria y metabolismo energético sugiere que el sistema endocannabinoide actúa como un puente funcional que integra información procedente de diferentes tejidos (Di Marzo & Piscitelli, 2015).
Esta capacidad integradora es especialmente relevante en situaciones donde múltiples sistemas deben coordinarse, como en la adaptación al estrés, los cambios en la disponibilidad energética o la respuesta a estímulos ambientales.
Adaptación y resiliencia biológica
La señalización endocannabinoide también se ha relacionado con procesos de adaptación y resiliencia. Al modular la intensidad de las respuestas fisiológicas, el sistema contribuye a limitar desviaciones excesivas del equilibrio interno y a facilitar el retorno a condiciones basales tras una perturbación.
En este sentido, más que iniciar respuestas, el sistema endocannabinoide actúa como un mecanismo de ajuste que amortigua las variaciones y favorece la estabilidad funcional del organismo.
Una red dinámica y contextual
Es importante destacar que la función del sistema endocannabinoide no puede entenderse de forma estática. Su actividad depende del contexto fisiológico, del tipo celular, de la localización tisular y de la interacción con otros sistemas de señalización. Esto implica que sus efectos no son universales ni lineales, sino que varían en función de múltiples factores.
Esta naturaleza dinámica y contextual ha llevado a considerar al sistema endocannabinoide como una red de regulación adaptable, más cercana a un sistema de “afinación” que a un interruptor binario.
IMPORTANCIA EN INVESTIGACIÓN Y PERSPECTIVAS CIENTÍFICAS
El estudio de la señalización endocannabinoide ha transformado de forma significativa la comprensión de la comunicación celular en las últimas décadas, abriendo nuevas líneas de investigación en campos que van desde la neurociencia hasta la biología del sistema inmunitario y el metabolismo. Sin embargo, esta expansión del conocimiento también ha puesto de manifiesto la complejidad del sistema y la necesidad de interpretarlo dentro de un marco científico riguroso, evitando simplificaciones o extrapolaciones no fundamentadas (Lu & Mackie, 2016).
Un sistema clave en biología molecular y fisiología
Desde su caracterización inicial, el sistema endocannabinoide ha pasado de considerarse una curiosidad bioquímica a convertirse en un elemento central en la regulación fisiológica. La identificación de mecanismos como la señalización retrógrada, la síntesis “on demand” de ligandos lipídicos o la modulación sináptica dependiente de contexto ha contribuido a redefinir conceptos clásicos de neurotransmisión y comunicación intercelular (Kano et al., 2009; Castillo et al., 2012).
Además, la implicación del sistema en múltiples tejidos ha impulsado su estudio como una red de regulación transversal, con funciones que abarcan desde la plasticidad neuronal hasta la señalización inmunometabólica.
Complejidad y limitaciones en la interpretación
A pesar del volumen creciente de investigación, la señalización endocannabinoide presenta una elevada complejidad que dificulta su interpretación. La diversidad de receptores implicados, la variabilidad en la expresión tisular, la naturaleza lipídica de los ligandos y su síntesis localizada hacen que los efectos observados dependan en gran medida del contexto experimental.
Asimismo, gran parte de la evidencia procede de modelos preclínicos, lo que requiere cautela a la hora de extrapolar resultados a sistemas humanos complejos. Las diferencias entre especies, las condiciones experimentales y las metodologías empleadas pueden influir significativamente en los resultados (Di Marzo & De Petrocellis, 2010).
Interacción con otros sistemas de señalización
Otro aspecto relevante es la interacción del sistema endocannabinoide con otras vías de señalización celular. Los endocannabinoides pueden modular, y a su vez ser modulados por, sistemas como el dopaminérgico, serotoninérgico, glutamatérgico o el eje hipotalámico-hipofisario, lo que añade una capa adicional de complejidad funcional.
Además, la participación de receptores no clásicos, como TRPV1, PPARs o GPR55, sugiere que la señalización endocannabinoide forma parte de una red más amplia de señalización lipídica, cuyo alcance aún no se comprende completamente (Di Marzo & De Petrocellis, 2010).
Potencial como herramienta de estudio
Más allá de sus implicaciones fisiológicas, el sistema endocannabinoide se ha convertido en una herramienta valiosa para estudiar procesos fundamentales como la plasticidad sináptica, la regulación del metabolismo o la comunicación intercelular. La posibilidad de modular enzimas específicas (como FAAH o MAGL) o receptores cannabinoides permite explorar de forma controlada la función de esta red en distintos contextos experimentales.
Este enfoque ha contribuido a ampliar el conocimiento sobre la organización funcional del organismo y sobre los mecanismos de adaptación a cambios internos y externos.
Perspectivas futuras
El avance en técnicas de biología molecular, genética y neuroimagen está permitiendo una caracterización cada vez más precisa de la señalización endocannabinoide. En los próximos años, es probable que se profundice en aspectos como la especificidad celular, la señalización subcelular y la interacción con otras redes lipídicas.
No obstante, el desarrollo de este campo requerirá mantener un enfoque crítico y basado en evidencia, evitando interpretaciones simplificadas de un sistema que, por su propia naturaleza, es altamente dinámico y dependiente del contexto.
REFERENCIAS
- Atwood BK, Mackie K. (2010). CB2: a cannabinoid receptor with an identity crisis. British Journal of Pharmacology, 160(3), 467–479. - Bisogno T, Howell F, Williams G, et al. (2003). Cloning of the first sn1-DAG lipases points to the spatial and temporal regulation of endocannabinoid signaling in the brain. Journal of Cell Biology, 163(3), 463–468. - Castillo PE, Younts TJ, Chávez AE, Hashimotodani Y. (2012). Endocannabinoid signaling and synaptic function. Neuron, 76(1), 70–81. - Chevaleyre V, Takahashi KA, Castillo PE. (2006). Endocannabinoid-mediated synaptic plasticity in the CNS. Annual Review of Neuroscience, 29, 37–76. - Cravatt BF, Giang DK, Mayfield SP, et al. (1996). Molecular characterization of an enzyme that degrades neuromodulatory fatty-acid amides. Nature, 384(6604), 83–87. - Di Marzo V, Fontana A, Cadas H, et al. (1994). Formation and inactivation of endogenous cannabinoid anandamide in central neurons. Nature, 372(6507), 686–691. - Di Marzo V, Piscitelli F. (2015). The endocannabinoid system and its modulation by phytocannabinoids. Neurotherapeutics, 12(4), 692–698. - Di Marzo V, De Petrocellis L. (2010). Why do cannabinoid receptors have more than one endogenous ligand? Philosophical Transactions of the Royal Society B, 367(1607), 3216–3228. - Dinh TP, Carpenter D, Leslie FM, et al. (2002). Brain monoglyceride lipase participating in endocannabinoid inactivation. Proceedings of the National Academy of Sciences, 99(16), 10819–10824. - Herkenham M, Lynn AB, Little MD, et al. (1990). Cannabinoid receptor localization in brain. Proceedings of the National Academy of Sciences, 87(5), 1932–1936. - Howlett AC, Barth F, Bonner TI, et al. (2002). International Union of Pharmacology. XXVII. Classification of cannabinoid receptors. Pharmacological Reviews, 54(2), 161–202. - Izzo AA, Sharkey KA. (2010). Cannabinoids and the gut: new developments and emerging concepts. Pharmacology & Therapeutics, 126(1), 21–38. - Kano M, Ohno-Shosaku T, Hashimotodani Y, et al. (2009). Endocannabinoid-mediated control of synaptic transmission. Physiological Reviews, 89(1), 309–380. - Kreitzer AC, Regehr WG. (2001). Retrograde inhibition of presynaptic calcium influx by endogenous cannabinoids. Neuron, 29(3), 717–727. - Lu HC, Mackie K. (2016). An introduction to the endogenous cannabinoid system. Biological Psychiatry, 79(7), 516–525. - Mechoulam R, Parker LA. (2013). The endocannabinoid system and the brain. Annual Review of Psychology, 64, 21–47. - Ohno-Shosaku T, Maejima T, Kano M. (2001). Endogenous cannabinoids mediate retrograde signals from depolarized postsynaptic neurons. Neuron, 29(3), 729–738. - Pagotto U, Marsicano G, Cota D, et al. (2006). The emerging role of the endocannabinoid system in endocrine regulation and energy balance. Endocrine Reviews, 27(1), 73–100. - Pertwee RG. (2001). Cannabinoid receptors and pain. Progress in Neurobiology, 63(5), 569–611. - Pertwee RG. (2008). The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids. British Journal of Pharmacology, 153(2), 199–215. - Piomelli D. (2003). The molecular logic of endocannabinoid signalling. Nature Reviews Neuroscience, 4(11), 873–884. - Sugiura T, Kobayashi Y, Oka S, Waku K. (2002). Biosynthesis and degradation of anandamide and 2-arachidonoylglycerol. Prostaglandins, Leukotrienes and Essential Fatty Acids, 66(2-3), 173–192. - Wilson RI, Nicoll RA. (2002). Endocannabinoid signaling in the brain. Science, 296(5568), 678–682.