Introducción
Los receptores clásicos del sistema endocannabinoide, principalmente CB1 y CB2, han sido históricamente considerados los principales mediadores de la señalización endocannabinoide. Sin embargo, a medida que ha avanzado la investigación en farmacología molecular y neurobiología, se ha identificado un conjunto adicional de dianas que participan en esta red de señalización, ampliando significativamente la complejidad funcional del sistema (Di Marzo, 2008; Lu & Mackie, 2016).
Entre estos receptores no clásicos destacan TRPV1 (Transient Receptor Potential Vanilloid 1) y GPR55 (G Protein-Coupled Receptor 55), ambos implicados en procesos fisiológicos que intersectan con la señalización endocannabinoide, aunque no formen parte estricta de la familia canónica de receptores cannabinoides. Estas proteínas actúan como nodos de integración entre sistemas de señalización lipídica, mecanismos sensoriales y respuestas celulares adaptativas, contribuyendo a una visión más amplia del denominado “endocannabinoidome” (Di Marzo & Piscitelli, 2015).
TRPV1, conocido originalmente como el receptor de la capsaicina, es un canal iónico sensible a estímulos térmicos, químicos y mecánicos, cuya activación puede ser modulada por endocannabinoides como la anandamida (AEA). Por su parte, GPR55 es un receptor acoplado a proteína G cuya farmacología aún se encuentra en estudio, pero que ha sido propuesto como un posible “tercer receptor cannabinoide” debido a su capacidad de responder a ciertos ligandos endocannabinoides y fitocannabinoides, incluyendo el CBD en contextos específicos (Caterina et al., 1997; Ryberg et al., 2007).
La interacción entre estos receptores y los endocannabinoides introduce nuevas capas de regulación en procesos como la transmisión sináptica, la percepción sensorial, la inflamación y la homeostasis celular. En este contexto, TRPV1 y GPR55 no deben entenderse como elementos periféricos, sino como componentes funcionales de una red más amplia en la que la señalización endocannabinoide se integra con otros sistemas fisiológicos (Starowicz et al., 2007; Pertwee et al., 2010).
El estudio de estos receptores ha permitido replantear la arquitectura del sistema endocannabinoide clásico, desplazando el foco desde un modelo centrado exclusivamente en CB1/CB2 hacia una red distribuida de receptores, enzimas y mediadores lipídicos interconectados, lo que resulta fundamental para comprender la diversidad de efectos biológicos asociados a los cannabinoides (Iannotti et al., 2016).
TRPV1 – estructura y activación
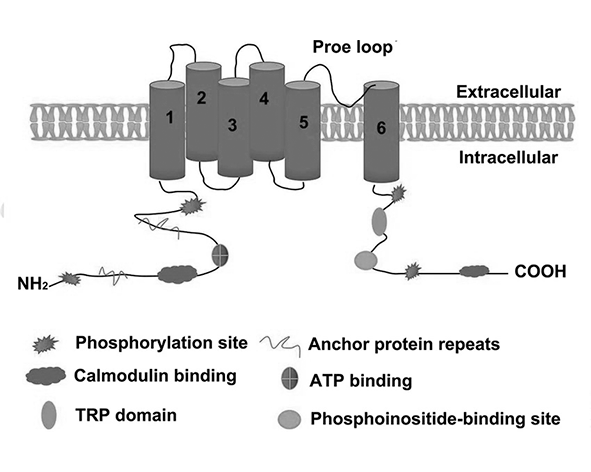
El receptor TRPV1 (Transient Receptor Potential Vanilloid 1) es un canal iónico no selectivo perteneciente a la familia de los canales TRP, caracterizado por su alta permeabilidad a cationes, especialmente calcio (Ca²⁺). Estructuralmente, TRPV1 está formado por cuatro subunidades idénticas que se ensamblan para formar un canal tetramérico, donde cada subunidad contiene seis dominios transmembrana (S1–S6) y un poro central que regula el paso de iones a través de la membrana celular (Caterina et al., 1997; Liao et al., 2013).
El dominio intracelular N-terminal presenta regiones de repetición de anquirina, implicadas en la regulación del canal mediante interacciones proteína-proteína, mientras que el extremo C-terminal participa en procesos de fosforilación y modulación funcional. Esta arquitectura permite que TRPV1 actúe como un sensor polimodal capaz de integrar múltiples estímulos físicos y químicos en una única respuesta iónica (Julius, 2013).
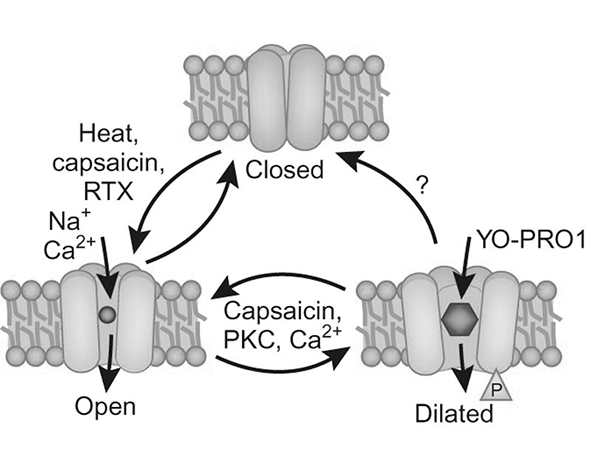
Desde el punto de vista funcional, TRPV1 se activa en respuesta a diversos estímulos, incluyendo temperaturas superiores a ~43 °C, pH ácido (condiciones de acidosis tisular) y compuestos químicos como la capsaicina. Esta capacidad de responder a estímulos nocivos lo convierte en un elemento clave en la transducción de señales nociceptivas, especialmente en neuronas sensoriales periféricas (Caterina et al., 1997; Tominaga et al., 1998).
En el contexto del sistema endocannabinoide, TRPV1 adquiere relevancia al ser activado por endocannabinoides como la anandamida (AEA), lo que establece un puente funcional entre la señalización cannabinoide y los sistemas de percepción sensorial. A diferencia de la activación de receptores CB1, que suele modular la liberación de neurotransmisores de forma inhibitoria, la activación de TRPV1 induce una entrada directa de calcio en la célula, generando respuestas excitatorias (Zygmunt et al., 1999; Smart et al., 2000).
Esta dualidad funcional es especialmente relevante, ya que la anandamida puede actuar tanto sobre CB1 como sobre TRPV1 dependiendo de su concentración, del contexto celular y de la localización subcelular. A bajas concentraciones predomina la señalización mediada por CB1, mientras que a concentraciones más elevadas se favorece la activación de TRPV1, lo que introduce un mecanismo de regulación dependiente de dosis dentro del sistema endocannabinoide (Ross, 2003).
Además, TRPV1 puede ser sensibilizado o desensibilizado mediante fosforilación por quinasas como PKC o PKA, así como por la acción de mediadores inflamatorios. Este fenómeno de sensibilización contribuye a procesos como la hiperalgesia, donde el umbral de activación del receptor disminuye, amplificando la respuesta a estímulos que normalmente no serían percibidos como dolorosos (Bhave et al., 2002; Numazaki et al., 2002).
En conjunto, TRPV1 representa una interfaz crítica entre la señalización endocannabinoide, la percepción del dolor y la respuesta inflamatoria, funcionando como un sensor molecular capaz de traducir cambios en el entorno físico y químico en señales celulares específicas.
TRPV1 – distribución y función fisiológica
El receptor TRPV1 presenta una distribución amplia tanto en el sistema nervioso periférico como en el sistema nervioso central, aunque su expresión es especialmente abundante en neuronas sensoriales primarias localizadas en los ganglios de la raíz dorsal y en los ganglios trigeminales. Estas neuronas están implicadas en la detección de estímulos nocivos, lo que sitúa a TRPV1 como un componente clave en la transducción del dolor y la termorrecepción (Caterina et al., 1997; Tominaga et al., 1998).
En el sistema nervioso central, TRPV1 también se expresa en regiones como el hipocampo, la amígdala, el hipotálamo y la sustancia gris periacueductal, áreas implicadas en la modulación emocional, la memoria y la respuesta al estrés. En estos contextos, su activación no se limita a la percepción sensorial, sino que participa en la modulación de la transmisión sináptica y en procesos de plasticidad neuronal (Mezey et al., 2000; Marsch et al., 2007).
A nivel periférico, TRPV1 se localiza en terminaciones nerviosas libres que inervan tejidos como la piel, las mucosas y órganos internos, donde actúa como sensor de estímulos térmicos, químicos e inflamatorios. Su activación en estos tejidos puede desencadenar la liberación de neuropéptidos como la sustancia P o el péptido relacionado con el gen de la calcitonina (CGRP), contribuyendo a la inflamación neurogénica y a la vasodilatación local (Holzer, 1991; Szallasi et al., 2007).
En el contexto del sistema endocannabinoide, la coexpresión de TRPV1 con receptores CB1 en determinadas poblaciones neuronales permite una interacción funcional compleja. Mientras que CB1 tiende a inhibir la liberación de neurotransmisores, la activación de TRPV1 favorece respuestas excitatorias mediadas por la entrada de calcio, generando un equilibrio dinámico entre señales inhibitorias y excitatorias (Starowicz et al., 2007; Di Marzo et al., 2001).
Además de su papel en el sistema nervioso, TRPV1 también se expresa en células no neuronales, incluyendo queratinocitos, células inmunes y células del sistema digestivo. En estos tejidos, el receptor participa en procesos como la regulación de la inflamación, la respuesta al estrés celular y la percepción visceral, ampliando su función más allá de la nocicepción clásica (Fernandes et al., 2012; Holzer, 2011).
En el tracto gastrointestinal, por ejemplo, TRPV1 interviene en la detección de estímulos químicos y en la modulación de la motilidad intestinal, así como en la respuesta a condiciones inflamatorias. Su activación puede influir en la liberación de mediadores locales y en la comunicación entre el sistema nervioso entérico y el sistema nervioso central (Holzer, 2011).
En conjunto, la distribución de TRPV1 refleja su papel como sensor molecular integrado en múltiples sistemas fisiológicos. Lejos de limitarse a la percepción del dolor, este receptor actúa como un modulador clave en la interacción entre estímulos externos, señalización endógena y respuestas adaptativas del organismo.
TRPV1 y endocannabinoides – interacción con AEA y señalización
La relación entre TRPV1 y el sistema endocannabinoide se establece principalmente a través de la capacidad de ciertos endocannabinoides, especialmente la anandamida (AEA), para actuar como agonistas de este canal iónico. Este fenómeno posiciona a TRPV1 como una diana funcional dentro del denominado endocannabinoidome, ampliando el espectro de acción de los lípidos endógenos más allá de los receptores cannabinoides clásicos CB1 y CB2 (Zygmunt et al., 1999; Di Marzo & De Petrocellis, 2010).
La anandamida presenta una doble afinidad funcional: puede activar receptores CB1 a bajas concentraciones y, en paralelo, activar TRPV1 cuando su concentración local aumenta o cuando las condiciones celulares favorecen esta interacción. Esta dualidad introduce un mecanismo de señalización dependiente del contexto, donde un mismo ligando puede generar efectos opuestos en función de la diana molecular predominante (Ross, 2003; Starowicz et al., 2007).
A nivel celular, la activación de TRPV1 por anandamida induce la apertura del canal y la entrada de Ca²⁺, lo que desencadena una cascada de señalización intracelular asociada a procesos excitatorios. Este mecanismo contrasta con la señalización mediada por CB1, que generalmente implica la inhibición de la adenilato ciclasa, la reducción de AMPc y la modulación negativa de la liberación de neurotransmisores (Smart et al., 2000; Lu & Mackie, 2016).
Esta diferencia funcional permite que la anandamida actúe como un modulador fino de la actividad neuronal. En determinadas sinapsis, la activación inicial de CB1 puede reducir la liberación de neurotransmisores, mientras que una acumulación posterior de AEA puede activar TRPV1, invirtiendo parcialmente el efecto mediante la inducción de señales excitatorias. Este equilibrio dinámico contribuye a la regulación de la plasticidad sináptica y de la señalización retrógrada (Grueter et al., 2010).
Además, existe una interacción funcional entre TRPV1 y las enzimas que regulan los niveles de endocannabinoides. La degradación de anandamida por la FAAH (Fatty Acid Amide Hydrolase) limita tanto su acción sobre CB1 como sobre TRPV1, lo que convierte a esta enzima en un regulador indirecto de la activación de ambos receptores (Cravatt et al., 2001; Di Marzo et al., 2001).
En contextos fisiopatológicos, como la inflamación o el estrés tisular, los niveles de anandamida pueden alterarse, favoreciendo una mayor activación de TRPV1. Este fenómeno ha sido relacionado con cambios en la sensibilidad nociceptiva y con la modulación de respuestas inflamatorias, lo que refuerza el papel de TRPV1 como un punto de convergencia entre señalización endocannabinoide y sistemas de respuesta al daño (Di Marzo & De Petrocellis, 2010).
En conjunto, la interacción entre TRPV1 y los endocannabinoides refleja una arquitectura de señalización compleja en la que los ligandos lipídicos endógenos no actúan sobre una única diana, sino que modulan múltiples receptores en función del contexto celular, la concentración y el estado fisiológico del tejido.
GPR55 – estructura y señalización
El receptor GPR55 (G Protein-Coupled Receptor 55) es un receptor acoplado a proteína G identificado a finales del siglo XX como parte de la familia de receptores huérfanos, es decir, aquellos cuya función y ligandos endógenos no estaban inicialmente bien definidos. Aunque su clasificación dentro del sistema endocannabinoide ha sido objeto de debate, su capacidad para responder a ciertos lípidos endógenos y fitocannabinoides ha llevado a considerarlo una diana relevante dentro del denominado endocannabinoidome (Sawzdargo et al., 1999; Ryberg et al., 2007).
Estructuralmente, GPR55 presenta la arquitectura típica de los receptores acoplados a proteína G (GPCR), caracterizada por siete dominios transmembrana (7TM), un extremo N-terminal extracelular y un extremo C-terminal intracelular. Sin embargo, a diferencia de los receptores cannabinoides clásicos CB1 y CB2, GPR55 muestra una baja homología de secuencia, lo que sugiere una evolución funcional divergente dentro de esta superfamilia de receptores (Pertwee et al., 2010).
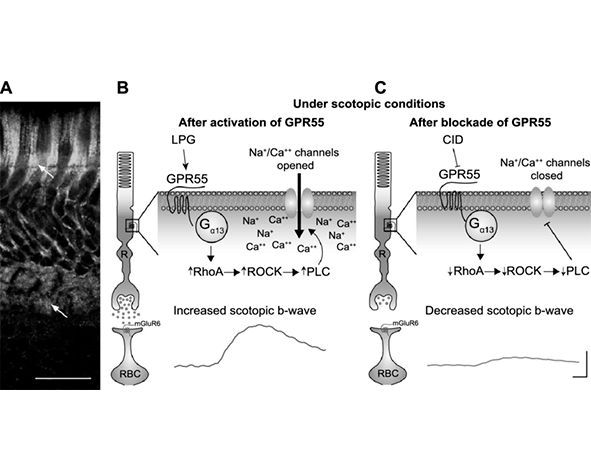
Desde el punto de vista de señalización intracelular, GPR55 se acopla preferentemente a proteínas G de la familia Gα12/13, en lugar de las Gαi/o típicamente asociadas a CB1 y CB2. Esta diferencia tiene implicaciones funcionales importantes, ya que la activación de GPR55 conduce a la activación de RhoA y de cascadas de señalización asociadas a la reorganización del citoesqueleto, la migración celular y la proliferación (Ryberg et al., 2007; Henstridge et al., 2011).
Además, la activación de GPR55 puede inducir aumentos en los niveles intracelulares de calcio mediante mecanismos dependientes de fosfolipasa C (PLC), lo que lo aproxima funcionalmente a receptores que generan respuestas excitatorias. Esta señalización mediada por Ca²⁺ contribuye a la modulación de procesos celulares como la liberación de neurotransmisores y la activación de vías de señalización dependientes de calcio (Lauckner et al., 2008).
Uno de los ligandos endógenos más estudiados para GPR55 es la lisofosfatidilinositol (LPI), un lípido de membrana que parece actuar como agonista funcional en diversos sistemas experimentales. Sin embargo, también se ha observado que ciertos cannabinoides, incluyendo el CBD, pueden modular la actividad de GPR55, actuando en muchos casos como antagonistas o moduladores negativos de su señalización (Oka et al., 2007; Pertwee et al., 2010).
Esta interacción con cannabinoides ha llevado a proponer a GPR55 como un posible “tercer receptor cannabinoide”, aunque esta clasificación sigue siendo controvertida debido a su baja similitud estructural con CB1/CB2 y a la complejidad de su farmacología. En lugar de considerarlo un receptor cannabinoide clásico, muchos autores lo sitúan como un receptor relacionado funcionalmente, integrado dentro de una red más amplia de señalización lipídica (Iannotti et al., 2016).
En conjunto, GPR55 representa un nodo de señalización diferenciado dentro del endocannabinoidome, con mecanismos de activación y efectos celulares distintos a los de los receptores cannabinoides tradicionales. Su estudio ha contribuido a ampliar la comprensión de cómo los lípidos bioactivos modulan procesos celulares complejos más allá de las vías canónicas del sistema endocannabinoide.
GPR55 – distribución y función fisiológica
El receptor GPR55 presenta una distribución amplia en distintos tejidos del organismo, aunque su expresión es particularmente relevante en el sistema nervioso central, el sistema inmunitario y el tejido óseo. En el cerebro, se ha detectado en regiones como el hipocampo, el cerebelo, los ganglios basales y la corteza cerebral, lo que sugiere un papel en la modulación de la actividad neuronal, la coordinación motora y ciertos procesos cognitivos (Ryberg et al., 2007; Lauckner et al., 2008).
En el sistema nervioso, GPR55 se expresa tanto en neuronas como en células gliales, donde su activación puede influir en la liberación de neurotransmisores y en la excitabilidad neuronal. A diferencia de los receptores CB1, cuya activación suele tener un efecto inhibitorio sobre la neurotransmisión, GPR55 tiende a promover respuestas excitatorias mediadas por aumentos en el calcio intracelular, lo que introduce una dimensión funcional distinta dentro de la señalización lipídica en el cerebro (Lauckner et al., 2008; Henstridge et al., 2011).
En el sistema inmunitario, GPR55 se ha identificado en células como linfocitos, monocitos y células dendríticas, donde participa en la regulación de la migración celular, la liberación de mediadores y la respuesta inflamatoria. Su activación a través de ligandos como la lisofosfatidilinositol (LPI) puede modular procesos inmunológicos complejos, aunque su papel exacto continúa siendo objeto de investigación (Oka et al., 2007; Balenga et al., 2011).
Uno de los ámbitos donde GPR55 ha adquirido especial relevancia es el tejido óseo. Se ha observado su expresión en osteoclastos y osteoblastos, células responsables de la resorción y formación ósea, respectivamente. Estudios experimentales sugieren que GPR55 puede participar en la regulación del remodelado óseo, influyendo en el equilibrio entre formación y degradación del tejido, lo que lo convierte en una diana potencial en el estudio de procesos relacionados con la densidad ósea (Whyte et al., 2009).
Además, GPR55 también se expresa en el tracto gastrointestinal, donde podría intervenir en la regulación de la motilidad intestinal y en la respuesta a estímulos inflamatorios. Su presencia en tejidos periféricos refuerza la idea de que este receptor no se limita a funciones neuronales, sino que participa en la integración de señales a nivel sistémico (Schicho et al., 2011).
En el contexto del sistema endocannabinoide ampliado, la distribución de GPR55 sugiere que actúa como un modulador de procesos fisiológicos diversos, incluyendo la excitabilidad neuronal, la respuesta inmune y la homeostasis tisular. Su perfil funcional, en muchos casos opuesto al de CB1, apunta a la existencia de un equilibrio dinámico entre distintas vías de señalización lipídica que contribuyen a la regulación del organismo (Pertwee et al., 2010).
En conjunto, GPR55 se posiciona como un receptor con funciones fisiológicas complejas y aún no completamente definidas, cuya integración dentro del endocannabinoidome refleja la creciente necesidad de entender el sistema endocannabinoide como una red distribuida de señalización más allá de sus componentes clásicos.
Interacción TRPV1, GPR55 y CB1 – una visión integrada de la señalización
La señalización endocannabinoide no puede entenderse como un sistema lineal basado exclusivamente en los receptores CB1 y CB2, sino como una red compleja en la que múltiples receptores interactúan de forma dinámica. En este contexto, TRPV1 y GPR55 introducen capas adicionales de regulación que amplían significativamente el alcance funcional del sistema, dando lugar a una arquitectura distribuida de señalización lipídica conocida como endocannabinoidome (Di Marzo & Piscitelli, 2015; Iannotti et al., 2016).
Uno de los aspectos más relevantes de esta interacción es la coexistencia de efectos opuestos entre los distintos receptores. Mientras que CB1, acoplado a proteínas Gαi/o, tiende a inhibir la liberación de neurotransmisores y reducir la excitabilidad neuronal, TRPV1 y GPR55 pueden inducir respuestas excitatorias mediante la entrada de calcio y la activación de vías intracelulares dependientes de Ca²⁺ y RhoA, respectivamente. Este contraste funcional permite una regulación fina del equilibrio entre inhibición y excitación en distintos contextos fisiológicos (Lu & Mackie, 2016; Lauckner et al., 2008).
La anandamida (AEA) ejemplifica esta complejidad al actuar como un ligando multitarget. A bajas concentraciones, activa preferentemente CB1, generando efectos inhibitorios sobre la neurotransmisión. Sin embargo, cuando su concentración aumenta o su degradación se ve limitada, puede activar TRPV1, desencadenando respuestas excitatorias. Este cambio en la diana molecular introduce un mecanismo de regulación dependiente de dosis y contexto celular (Ross, 2003; Zygmunt et al., 1999).
Por su parte, GPR55 añade una dimensión adicional al actuar en muchos casos como un modulador funcionalmente opuesto a CB1. Mientras CB1 reduce la liberación de neurotransmisores, la activación de GPR55 puede favorecer la excitabilidad neuronal y la liberación de calcio intracelular. Esta relación ha llevado a proponer la existencia de interacciones antagonistas o compensatorias entre ambos receptores, especialmente en tejidos donde coexisten (Pertwee et al., 2010; Henstridge et al., 2011).
El papel del cannabidiol (CBD) en esta red es especialmente relevante, ya que no actúa como un agonista directo de CB1, sino que modula múltiples dianas, incluyendo TRPV1 y GPR55. En el caso de TRPV1, el CBD puede actuar como agonista o modulador, mientras que en GPR55 suele comportarse como antagonista funcional, reduciendo su señalización. Esta acción multitarget refuerza la idea de que los fitocannabinoides no actúan sobre un único receptor, sino que modulan redes completas de señalización (Iannotti et al., 2014; Pertwee et al., 2010).
Además, estos receptores no funcionan de forma aislada, sino que pueden coexistir en las mismas células o microdominios sinápticos, permitiendo interacciones cruzadas que modulan la respuesta celular. La presencia simultánea de CB1, TRPV1 y GPR55 en determinadas neuronas o células inmunes sugiere la existencia de mecanismos de integración que ajustan la respuesta en función del estado fisiológico del tejido (Starowicz et al., 2007).
En conjunto, la interacción entre TRPV1, GPR55 y CB1 refleja una organización compleja en la que la señalización endocannabinoide se distribuye entre múltiples receptores con funciones complementarias y, en ocasiones, opuestas. Este modelo integrado permite entender cómo un mismo ligando puede generar efectos distintos en función del contexto, la concentración y la combinación de receptores presentes en cada sistema biológico.
Importancia en investigación y contexto científico
El estudio de receptores como TRPV1 y GPR55 ha sido clave para ampliar la comprensión del sistema endocannabinoide más allá de su modelo clásico centrado en CB1 y CB2. Estos receptores han permitido identificar nuevas rutas de señalización y mecanismos de interacción que sitúan a los lípidos bioactivos como moduladores versátiles de múltiples sistemas fisiológicos, consolidando el concepto de endocannabinoidome como una red integrada de comunicación celular (Di Marzo & Piscitelli, 2015; Iannotti et al., 2016).
En el ámbito de la investigación básica, TRPV1 ha sido ampliamente estudiado como modelo de canal iónico polimodal, contribuyendo al entendimiento de la transducción sensorial, especialmente en relación con estímulos térmicos y químicos. Su interacción con endocannabinoides ha permitido explorar cómo los sistemas de señalización lipídica pueden modular la percepción sensorial y la plasticidad neuronal, abriendo nuevas líneas de investigación en neurobiología (Julius, 2013; Zygmunt et al., 1999).
Por su parte, GPR55 ha generado un interés creciente debido a su farmacología atípica y a su posible papel en procesos como la migración celular, la señalización intracelular dependiente de calcio y la regulación del citoesqueleto. Aunque su clasificación como receptor cannabinoide sigue siendo debatida, su capacidad de responder a lípidos endógenos y de interactuar con fitocannabinoides lo convierte en una diana relevante en el estudio de la señalización lipídica (Ryberg et al., 2007; Henstridge et al., 2011).
La investigación sobre estos receptores también ha contribuido a replantear la idea de especificidad receptor-ligando dentro del sistema endocannabinoide. En lugar de un modelo unidimensional, los datos actuales apoyan una visión en la que múltiples receptores pueden ser activados o modulados por un mismo ligando, dependiendo del contexto celular, la concentración y la disponibilidad de enzimas metabólicas. Este enfoque ha sido fundamental para entender la diversidad de respuestas observadas en sistemas biológicos complejos (Pertwee et al., 2010; Lu & Mackie, 2016).
En el contexto experimental, TRPV1 y GPR55 se han utilizado como herramientas para estudiar la interacción entre señalización neuronal, inflamación y homeostasis celular. Su implicación en distintos tejidos ha permitido analizar cómo los sistemas de señalización convergen en procesos adaptativos, aportando información clave sobre la integración de estímulos en el organismo (Starowicz et al., 2007; Di Marzo & De Petrocellis, 2010).
Además, estos receptores han puesto de manifiesto la importancia de considerar el sistema endocannabinoide como parte de una red más amplia de mediadores lipídicos, donde la interacción entre diferentes vías de señalización es esencial para mantener el equilibrio fisiológico. Este cambio de paradigma ha impulsado nuevas estrategias de investigación centradas en redes de señalización en lugar de dianas aisladas (Iannotti et al., 2016).
En conjunto, TRPV1 y GPR55 han pasado de ser receptores periféricos a convertirse en elementos clave para comprender la complejidad del endocannabinoidome, aportando una visión más integrada y dinámica de la regulación fisiológica mediada por lípidos bioactivos.
Referencias
- Bhave, G., Zhu, W., Wang, H., Brasier, D. J., Oxford, G. S., & Gereau, R. W. (2002). cAMP-dependent protein kinase regulates desensitization of the capsaicin receptor (VR1) by direct phosphorylation. Neuron, 35(4), 721–731. - Caterina, M. J., Schumacher, M. A., Tominaga, M., Rosen, T. A., Levine, J. D., & Julius, D. (1997). The capsaicin receptor: a heat-activated ion channel in the pain pathway. Nature, 389(6653), 816–824. - Cravatt, B. F., Demarest, K., Patricelli, M. P., Bracey, M. H., Giang, D. K., Martin, B. R., & Lichtman, A. H. (2001). Supersensitivity to anandamide and enhanced endogenous cannabinoid signaling in mice lacking fatty acid amide hydrolase. Proceedings of the National Academy of Sciences, 98(16), 9371–9376. - Di Marzo, V. (2008). Targeting the endocannabinoid system: to enhance or reduce? Nature Reviews Drug Discovery, 7(5), 438–455. - Di Marzo, V., & De Petrocellis, L. (2010). Why do cannabinoid receptors have more than one endogenous ligand? Philosophical Transactions of the Royal Society B, 367(1607), 3216–3228. - Di Marzo, V., & Piscitelli, F. (2015). The endocannabinoid system and its modulation by phytocannabinoids. Neurotherapeutics, 12(4), 692–698. - Di Marzo, V., Bisogno, T., De Petrocellis, L., Melck, D., Orlando, P., Wagner, J. A., & Kunos, G. (2001). Biosynthesis and inactivation of the endocannabinoid 2-arachidonoylglycerol in circulating and tumoral macrophages. European Journal of Biochemistry, 268(12), 3260–3268. - Fernandes, E. S., Fernandes, M. A., & Keeble, J. E. (2012). The functions of TRPA1 and TRPV1: moving away from sensory nerves. British Journal of Pharmacology, 166(2), 510–521. - Grueter, B. A., Brasnjo, G., & Malenka, R. C. (2010). Postsynaptic TRPV1 triggers cell type-specific long-term depression in the nucleus accumbens. Nature Neuroscience, 13(12), 1519–1525. - Henstridge, C. M., Balenga, N. A., Ford, L. A., Ross, R. A., Waldhoer, M., & Irving, A. J. (2011). The GPR55 ligand LPI modulates RhoA-dependent signalling and neuronal morphology. British Journal of Pharmacology, 164(2), 457–470. - Holzer, P. (1991). Capsaicin: cellular targets, mechanisms of action, and selectivity for thin sensory neurons. Pharmacological Reviews, 43(2), 143–201. - Holzer, P. (2011). Transient receptor potential (TRP) channels as drug targets for diseases of the digestive system. Pharmacology & Therapeutics, 131(1), 142–170. - Iannotti, F. A., Di Marzo, V., & Petrosino, S. (2016). Endocannabinoids and endocannabinoid-related mediators: Targets, metabolism and role in neurological disorders. Progress in Lipid Research, 62, 107–128. - Iannotti, F. A., Hill, C. L., Leo, A., Alhusaini, A., Soubrane, C. H., Mazzarella, E., ... & Di Marzo, V. (2014). Nonpsychotropic plant cannabinoids,cannabidivarin (CBDV) and cannabidiol (CBD), activate and desensitize transient receptor potential vanilloid 1 (TRPV1) channels. ACS Chemical Neuroscience, 5(11), 1131–1141. - Julius, D. (2013). TRP channels and pain. Annual Review of Cell and Developmental Biology, 29, 355–384. Lauckner, J. E., Jensen, J. B., Chen, H. Y., Lu, H. C., Hille, B., & Mackie, K. (2008). GPR55 is a cannabinoid receptor that increases intracellular calcium and inhibits M current. Proceedings of the National Academy of Sciences, 105(7), 2699–2704. - Liao, M., Cao, E., Julius, D., & Cheng, Y. (2013). Structure of the TRPV1 ion channel determined by electron cryo-microscopy. Nature, 504(7478), 107–112. Lu, H. C., & Mackie, K. (2016). An introduction to the endogenous cannabinoid system. Biological Psychiatry, 79(7), 516–525. - Marsch, R., Foeller, E., Rammes, G., Bunck, M., Kössl, M., Holsboer, F., ... & Wotjak, C. T. (2007). Reduced anxiety, conditioned fear, and hippocampal long-term potentiation in transient receptor potential vanilloid type 1 receptor-deficient mice. Journal of Neuroscience, 27(4), 832–839. - Mezey, É., Tóth, Z. E., Cortright, D. N., Arzubi, M. K., Krause, J. E., Elde, R., ... & Blumberg, P. M. (2000). Distribution of mRNA for vanilloid receptor subtype 1 (VR1), and VR1-like receptor, in the central nervous system of the rat and human. Proceedings of the National Academy of Sciences, 97(7), 3655–3660. - Numazaki, M., Tominaga, T., Toyooka, H., & Tominaga, M. (2002). Direct phosphorylation of capsaicin receptor VR1 by protein kinase Cε and identification of two target serine residues. Journal of Biological Chemistry, 277(16), 13375–13378. - Oka, S., Kimura, S., Toshida, T., Ota, R., Yamashita, A., Sugiura, T., & Waku, K. (2007). Lysophosphatidylinositol induces rapid phosphorylation of p38 MAP kinase and activating transcription factor-2 in HEK293 cells expressing GPR55. Journal of Biochemistry, 142(1), 65–71. - Pertwee, R. G., Howlett, A. C., Abood, M. E., Alexander, S. P., Di Marzo, V., Elphick, M. R., ... & Ross, R. A. (2010). International Union of Basic and Clinical Pharmacology. LXXIX. Cannabinoid receptors and their ligands. Pharmacological Reviews, 62(4), 588–631. - Ross, R. A. (2003). Anandamide and vanilloid TRPV1 receptors. British Journal of Pharmacology, 140(5), 790–801. Ryberg, E., Larsson, N., Sjögren, S., Hjorth, S., Hermansson, N. O., Leonova, J., ... & Greasley, P. J. (2007). The orphan receptor GPR55 is a novel cannabinoid receptor. British Journal of Pharmacology, 152(7), 1092–1101. - Sawzdargo, M., Nguyen, T., Lee, D. K., Lynch, K. R., Cheng, R., Heng, H. H., ... & George, S. R. (1999). Identification and cloning of three novel human G protein-coupled receptor genes GPR52, ψGPR53 and GPR55. Genomics, 64(2), 193–200. - Schicho, R., Bashashati, M., Bawa, M., McHugh, D., Saur, D., Hu, H. M., ... & Storr, M. (2011). The atypical cannabinoid O-1602 protects against experimental colitis and inhibits neutrophil recruitment. Inflammatory Bowel Diseases, 17(8), 1651–1664. - Smart, D., Gunthorpe, M. J., Jerman, J. C., Nasir, S., Gray, J., Muir, A. I., ... & Davis, J. B. (2000). The endogenous lipid anandamide is a full agonist at the human vanilloid receptor (hVR1). British Journal of Pharmacology, 129(2), 227–230. - Starowicz, K., Nigam, S., & Di Marzo, V. (2007). Biochemistry and pharmacology of endovanilloids. Pharmacology & Therapeutics, 114(1), 13–33. - Szallasi, A., Cortright, D. N., Blum, C. A., & Eid, S. R. (2007). The vanilloid receptor TRPV1: 10 years from channel cloning to antagonist proof-of-concept. Nature Reviews Drug Discovery, 6(5), 357–372. - Tominaga, M., Caterina, M. J., Malmberg, A. B., Rosen, T. A., Gilbert, H., Skinner, K., ... & Julius, D. (1998). The cloned capsaicin receptor integrates multiple pain-producing stimuli. Neuron, 21(3), 531–543. - Whyte, L. S., Ryberg, E., Sims, N. A., Ridge, S. A., Mackie, K., Greasley, P. J., & Ross, R. A. (2009). The putative cannabinoid receptor GPR55 affects osteoclast function in vitro and bone mass in vivo. Proceedings of the National Academy of Sciences, 106(38), 16511–16516. - Zygmunt, P. M., Petersson, J., Andersson, D. A., Chuang, H. H., Sørgård, M., Di Marzo, V., ... & Högestätt, E. D. (1999). Vanilloid receptors on sensory nerves mediate the vasodilator action of anandamide. Nature, 400(6743), 452–457.