Introducción
El receptor nuclear PPARγ es un factor de transcripción perteneciente a la superfamilia de receptores nucleares, proteínas especializadas en traducir señales químicas en cambios en la expresión génica. A diferencia de los receptores de membrana, que actúan en escalas temporales rápidas, PPARγ modula procesos más lentos pero profundamente estructurales, como la diferenciación celular, el metabolismo lipídico y la regulación de la respuesta inflamatoria (Evans et al., 2004; Lehrke & Lazar, 2005).
Se expresa de forma predominante en tejido adiposo, donde desempeña un papel central en la formación y mantenimiento de los adipocitos, pero también está presente en otros tejidos como el colon, el sistema inmunitario y determinadas regiones del sistema nervioso central. Esta distribución sugiere que su función no se limita al almacenamiento energético, sino que participa en redes fisiológicas más amplias relacionadas con la homeostasis metabólica y el equilibrio inflamatorio (Tontonoz & Spiegelman, 2008).
Desde un punto de vista funcional, PPARγ actúa como un sensor de lípidos, activándose mediante la unión de moléculas lipofílicas —muchas de ellas derivadas de ácidos grasos— que reflejan el estado metabólico del organismo. Tras su activación, forma un heterodímero con el receptor RXR (Retinoid X Receptor) y se une a secuencias específicas del ADN denominadas PPRE (Peroxisome Proliferator Response Elements), modulando la transcripción de genes implicados en almacenamiento de lípidos, sensibilidad a la insulina y control de procesos inflamatorios (Chawla et al., 2001; Glass & Ogawa, 2006).
En el contexto del sistema endocannabinoide ampliado, PPARγ adquiere un interés particular como punto de convergencia entre señalización lipídica y regulación génica, dado que diversos lípidos bioactivos relacionados con esta red —incluyendo endocannabinoides y compuestos afines— pueden interactuar directa o indirectamente con este receptor. Esta interacción amplía la comprensión clásica del sistema, integrando mecanismos nucleares en la respuesta fisiológica a señales lipídicas (O’Sullivan, 2007; Pistis & Melis, 2010).
Más allá de su función como regulador metabólico, PPARγ forma parte de una familia evolutivamente conservada de receptores nucleares que incluyen otros sensores lipídicos como PPARα y PPARβ/δ, así como receptores de hormonas esteroideas, tiroideas y retinoides. Esta familia comparte una arquitectura modular y un mecanismo de acción basado en la regulación directa de la transcripción génica, lo que permite a las células adaptar su programa funcional a cambios en el entorno químico. En este marco, PPARγ puede entenderse no solo como un regulador específico del metabolismo adiposo, sino como un componente de un sistema más amplio de control transcripcional que coordina respuestas metabólicas, inmunológicas y celulares a nivel sistémico (Evans & Mangelsdorf, 2014).
Historia del descubrimiento
El receptor PPARγ fue identificado a principios de la década de 1990 como parte de una nueva subfamilia de receptores nucleares activados por ligandos lipídicos. Su descubrimiento se produjo en el contexto del estudio de los llamados “peroxisome proliferators”, compuestos capaces de inducir la proliferación de peroxisomas en hepatocitos de roedores, lo que llevó a la caracterización inicial de los receptores PPAR como sensores metabólicos nucleares (Issemann & Green, 1990).
La isoforma PPARγ fue posteriormente diferenciada de otros miembros de la familia, como PPARα y PPARβ/δ, al observarse su patrón de expresión altamente enriquecido en tejido adiposo. Este hallazgo fue clave, ya que estudios funcionales demostraron que su activación inducía la diferenciación de preadipocitos en adipocitos maduros, posicionándolo como un regulador central de la adipogénesis y del almacenamiento lipídico (Tontonoz et al., 1994).
Un avance relevante en la caracterización de PPARγ fue la identificación de sus isoformas principales, PPARγ1 y PPARγ2, generadas a partir de un mismo gen mediante el uso de promotores alternativos y splicing diferencial. Mientras que PPARγ1 presenta una distribución más amplia en distintos tejidos, PPARγ2 se expresa de forma predominante en tejido adiposo y contiene una extensión adicional en el extremo N-terminal que potencia su actividad transcripcional. Esta diferencia estructural contribuye a su papel específico en la diferenciación adipocitaria y en la regulación del metabolismo lipídico (Zhu et al., 1995; Tontonoz & Spiegelman, 2008).
Durante la segunda mitad de los años 90, la investigación sobre PPARγ se intensificó al descubrirse su implicación directa en la regulación de la sensibilidad a la insulina. Este avance estuvo estrechamente ligado al desarrollo de las tiazolidinedionas (TZDs), una clase de fármacos antidiabéticos que actúan como agonistas de PPARγ, lo que permitió validar experimentalmente su papel en la homeostasis glucídica y en el metabolismo energético sistémico (Lehmann et al., 1995).
Con el avance de la investigación, el papel de PPARγ se expandió más allá del metabolismo lipídico, incorporándose a procesos relacionados con la inflamación, la inmunomodulación y la regulación del microambiente tisular. Este cambio de paradigma permitió entender que su actividad no es exclusivamente metabólica, sino que forma parte de redes fisiológicas complejas donde interactúan múltiples vías de señalización (Ricote et al., 1998).
En años más recientes, la integración de PPARγ dentro del concepto de endocannabinoidome ha aportado una nueva dimensión funcional, al demostrarse que diversos lípidos bioactivos —incluyendo algunos endocannabinoides y compuestos afines— pueden modular su actividad. Esta convergencia ha reforzado su papel como nodo de integración entre señalización lipídica y control transcripcional (O’Sullivan, 2007; Pistis & Melis, 2010).
Estructura y mecanismo de acción
El receptor PPARγ presenta la arquitectura clásica de los receptores nucleares, organizada en varios dominios funcionales altamente conservados que determinan su capacidad de unión a ligandos, interacción con el ADN y regulación transcripcional. Esta organización modular permite una integración precisa entre reconocimiento de señales químicas y respuesta génica (Evans & Mangelsdorf, 2014).
A nivel estructural, PPARγ se compone de cuatro regiones principales: un dominio N-terminal con función reguladora (AF-1), un dominio de unión al ADN (DBD, DNA-binding domain), una región bisagra flexible y un dominio de unión a ligando (LBD, ligand-binding domain) en el extremo C-terminal. El DBD contiene motivos tipo “dedo de zinc” que permiten el reconocimiento específico de secuencias en el ADN, mientras que el LBD presenta una cavidad hidrofóbica capaz de acomodar una amplia variedad de ligandos lipídicos (Chandra et al., 2008).
El dominio LBD de PPARγ es especialmente relevante desde el punto de vista estructural y farmacológico, ya que presenta un bolsillo de unión amplio y flexible, con una arquitectura en forma de “Y” que permite la interacción con ligandos de distinta naturaleza química. Este bolsillo está formado por varias hélices α que delimitan una cavidad interna donde los ligandos establecen interacciones hidrofóbicas y enlaces de hidrógeno con residuos clave. Esta plasticidad estructural explica la capacidad del receptor para reconocer tanto ligandos endógenos como compuestos sintéticos con diferentes afinidades y perfiles de activación (Nolte et al., 1998).
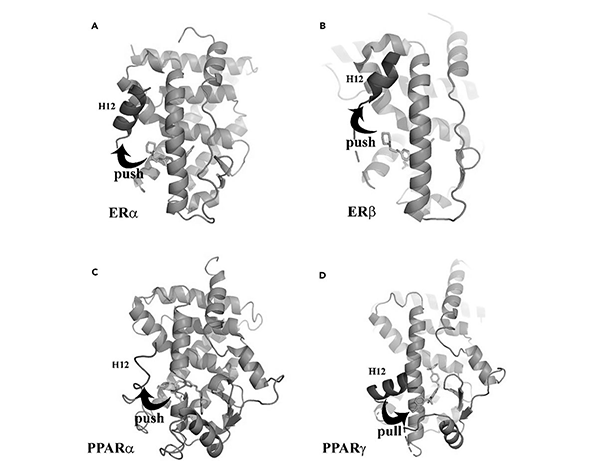
La unión del ligando induce un cambio conformacional en el LBD, particularmente en la hélice 12 (H12), que actúa como un interruptor estructural crítico. En presencia de agonistas, esta hélice se posiciona de manera que favorece la interacción con coactivadores que contienen motivos LXXLL, facilitando la activación transcripcional. En ausencia de ligando o en presencia de antagonistas, esta conformación se altera, promoviendo la asociación con correpresores y reduciendo la actividad del receptor (Glass & Ogawa, 2006).
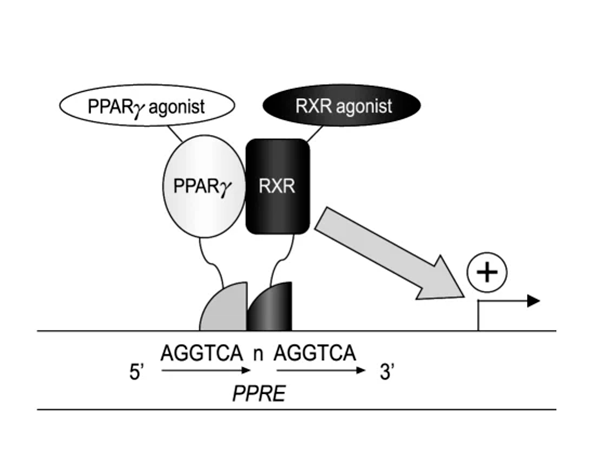
Una vez activado, PPARγ forma un heterodímero funcional con el receptor RXR (Retinoid X Receptor). Este complejo se une a secuencias específicas del ADN denominadas PPRE (Peroxisome Proliferator Response Elements), localizadas en las regiones promotoras de genes diana. La unión al ADN, junto con la interacción con cofactores, modula la maquinaria transcripcional y altera la expresión génica de forma coordinada (Chawla et al., 2001).
Este proceso no actúa como un simple interruptor binario, sino como un sistema de regulación fina. Diferentes ligandos pueden inducir conformaciones ligeramente distintas del receptor, lo que se traduce en perfiles de activación génica específicos. Este fenómeno, conocido como modulación selectiva del receptor, es clave para entender por qué distintos compuestos que activan PPARγ pueden generar efectos fisiológicos divergentes (Choi et al., 2010).
Además, la estructura de PPARγ permite interacciones dinámicas con múltiples cofactores y complejos proteicos, lo que añade una capa adicional de regulación. Estas interacciones no dependen únicamente del ligando, sino también del contexto celular, del estado metabólico y de modificaciones postraduccionales del propio receptor, configurando una respuesta altamente adaptable y específica (Feige et al., 2006).
Distribución y expresión tisular
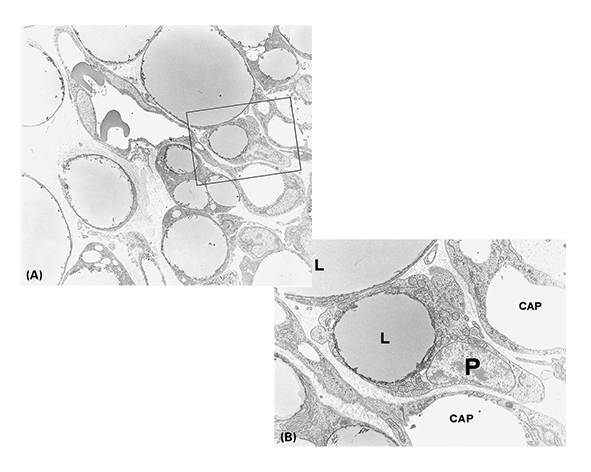
El receptor PPARγ presenta un patrón de expresión característico, con predominio en tejidos directamente implicados en el metabolismo energético, especialmente en el tejido adiposo. En adipocitos maduros, PPARγ se expresa de forma abundante y constituye un regulador esencial de la diferenciación adipocitaria, la captación de ácidos grasos y el almacenamiento de triglicéridos, actuando como un eje central en la homeostasis lipídica (Tontonoz et al., 1994; Rosen & Spiegelman, 2001).
Dentro del tejido adiposo, su expresión y función difieren entre el tejido adiposo blanco (WAT) y el tejido adiposo marrón (BAT). En el WAT, PPARγ está estrechamente asociado con el almacenamiento energético y la expansión del tejido adiposo, mientras que en el BAT participa en la regulación de procesos relacionados con la termogénesis y el metabolismo oxidativo. Además, en adipocitos beige o “brite”, PPARγ contribuye a la plasticidad metabólica del tejido adiposo, facilitando la transición entre fenotipos de almacenamiento y gasto energético en función de las condiciones fisiológicas (Seale et al., 2011).
Además del tejido adiposo, PPARγ también se expresa en células del sistema inmunitario, incluyendo macrófagos y linfocitos. En estos contextos, su activación se asocia con la modulación de la respuesta inflamatoria, favoreciendo perfiles antiinflamatorios y regulando la producción de citocinas. Esta función ha sido clave para ampliar su papel más allá del metabolismo, integrándolo en procesos de inmunorregulación y resolución de la inflamación (Ricote et al., 1998; Bouhlel et al., 2007).
En el tracto gastrointestinal, particularmente en el colon, PPARγ muestra una expresión significativa en células epiteliales. Aquí participa en la regulación de la diferenciación celular, la integridad de la barrera intestinal y la respuesta a estímulos inflamatorios locales, lo que ha motivado su estudio en modelos de enfermedades inflamatorias intestinales (Su et al., 1999).
En el sistema nervioso central, aunque su expresión es más moderada en comparación con el tejido adiposo, PPARγ está presente en neuronas y células gliales, incluyendo astrocitos y microglía. En este entorno, se ha relacionado con procesos de neuroinflamación, metabolismo energético cerebral y protección frente a estrés celular, sugiriendo una función moduladora en el equilibrio neuroinmunológico (Moreno et al., 2004; Bernardo & Minghetti, 2008).
Finalmente, PPARγ también se expresa en otros tejidos como el hígado, el músculo esquelético y el endotelio vascular, aunque en niveles variables. En estos contextos, su función se relaciona con la regulación del metabolismo lipídico local, la señalización inflamatoria y la adaptación a cambios en el entorno metabólico. Esta distribución amplia refuerza la idea de que su actividad es sistémica, actuando como un integrador de señales metabólicas e inmunológicas en distintos niveles del organismo (Lehrke & Lazar, 2005).
Rol fisiológico
El receptor PPARγ desempeña un papel central en la regulación de la homeostasis energética, actuando como un modulador clave del metabolismo lipídico y glucídico. Su activación en tejido adiposo promueve la diferenciación de preadipocitos en adipocitos maduros y facilita la captación y almacenamiento de ácidos grasos en forma de triglicéridos, contribuyendo a la regulación del balance energético sistémico (Rosen & Spiegelman, 2001).
Más allá del almacenamiento lipídico, PPARγ participa de forma directa en la regulación de la sensibilidad a la insulina. Su activación mejora la captación de glucosa en tejidos periféricos y modula la liberación de adipocinas, estableciendo un vínculo funcional entre el tejido adiposo y el metabolismo glucídico global. Este papel es clave para entender su implicación en estados fisiológicos y patológicos relacionados con la resistencia a la insulina (Lehrke & Lazar, 2005).
En este contexto, PPARγ regula la expresión y secreción de adipocinas clave como la adiponectina y la leptina, moléculas que actúan como mediadores endocrinos del tejido adiposo. La adiponectina se asocia con una mejora en la sensibilidad a la insulina y efectos antiinflamatorios, mientras que la leptina participa en la regulación del apetito y el equilibrio energético. A través de estas señales, PPARγ no solo controla el almacenamiento de energía, sino que coordina la comunicación entre tejido adiposo, hígado, músculo y sistema nervioso central (Kadowaki et al., 2006).
En el sistema inmunitario, PPARγ actúa como un regulador de la respuesta inflamatoria. Su activación en macrófagos favorece la transición hacia fenotipos antiinflamatorios y limita la producción de mediadores proinflamatorios. Este efecto no solo contribuye a la resolución de la inflamación, sino que también modula la interacción entre metabolismo e inmunidad, un aspecto fundamental en la fisiología contemporánea (Ricote et al., 1998; Bouhlel et al., 2007).
En el contexto del sistema nervioso central, PPARγ interviene en la regulación de la neuroinflamación y en la protección frente a estrés celular. Su actividad en células gliales y neuronas sugiere un papel modulador en la respuesta a daño tisular y en el mantenimiento del equilibrio homeostático cerebral, integrando señales metabólicas e inflamatorias en el entorno neuronal (Bernardo & Minghetti, 2008).
Además, PPARγ contribuye al mantenimiento de la integridad de barreras epiteliales, como la intestinal, donde regula procesos de diferenciación celular y respuesta a estímulos locales. Esta función refuerza su papel como modulador del entorno tisular, participando en la interacción entre metabolismo, microbiota y sistema inmunitario (Su et al., 1999).
En conjunto, el rol fisiológico de PPARγ no puede entenderse como una función aislada, sino como parte de una red integrada en la que señales lipídicas, metabólicas e inmunológicas convergen para mantener la homeostasis del organismo. Esta capacidad de integración es la que explica su relevancia en múltiples sistemas fisiológicos y su interés como diana en investigación biomédica (Evans et al., 2004).
Farmacología
El receptor PPARγ constituye una diana farmacológica relevante debido a su papel central en la regulación del metabolismo energético y la respuesta inflamatoria. Su actividad puede ser modulada por una amplia variedad de ligandos, tanto endógenos como exógenos, lo que ha permitido explorar diferentes estrategias de intervención a nivel molecular (Lehrke & Lazar, 2005).
Entre los ligandos endógenos, destacan diversos ácidos grasos y sus derivados oxigenados, como eicosanoides y prostaglandinas. Estos compuestos actúan como moduladores fisiológicos del receptor, reflejando el estado metabólico del organismo. En particular, algunas prostaglandinas como la 15-deoxi-Δ12,14-prostaglandina J2 han sido descritas como agonistas naturales de PPARγ, aunque su relevancia fisiológica en condiciones normales sigue siendo objeto de debate (Forman et al., 1995).
En el ámbito farmacológico, los agonistas sintéticos más conocidos son las tiazolidinedionas (TZDs), una clase de compuestos desarrollados para el tratamiento de la diabetes tipo 2. Fármacos como pioglitazona o rosiglitazona actúan como agonistas de PPARγ, mejorando la sensibilidad a la insulina mediante la regulación de genes implicados en el metabolismo glucídico y lipídico. Estos compuestos permitieron validar clínicamente el papel del receptor, aunque su uso ha estado condicionado por efectos adversos asociados a su activación sistémica (Nesto et al., 2004).
Más recientemente, se ha puesto el foco en el desarrollo de moduladores selectivos de PPARγ (SPPARMs), diseñados para inducir perfiles de activación más específicos y reducir efectos secundarios. Este enfoque se basa en la idea de que diferentes ligandos pueden estabilizar conformaciones distintas del receptor, modulando selectivamente la expresión génica en lugar de activarla de forma global (Choi et al., 2010).
En paralelo, diversos compuestos lipídicos relacionados con el sistema endocannabinoide han mostrado capacidad para interactuar con PPARγ, ya sea como agonistas directos o mediante mecanismos indirectos. Entre ellos se incluyen algunos endocannabinoides y fitocannabinoides, lo que ha ampliado el interés farmacológico del receptor más allá del metabolismo clásico, integrándolo en el estudio de redes lipídicas complejas (O’Sullivan, 2007).
Desde una perspectiva farmacodinámica, la activación de PPARγ no se traduce en un efecto único, sino en un conjunto de respuestas dependientes del contexto tisular, del tipo de ligando y del entorno molecular. Esta complejidad es clave para entender tanto su potencial terapéutico como las limitaciones observadas en intervenciones farmacológicas dirigidas a este receptor (Evans et al., 2004).
Mecanismos moleculares
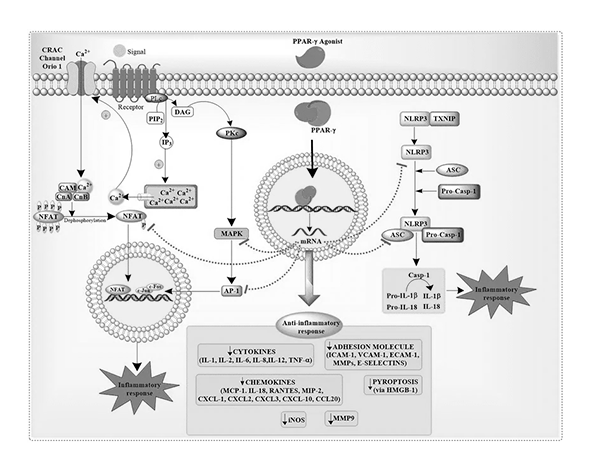
El receptor PPARγ ejerce su función a través de mecanismos moleculares que combinan activación transcripcional directa y modulación indirecta de otras vías de señalización. Esta dualidad es clave para entender su papel como integrador de señales metabólicas e inflamatorias en distintos contextos celulares (Glass & Ogawa, 2006).
El mecanismo clásico de acción implica la unión de un ligando al dominio LBD, lo que induce un cambio conformacional que favorece la liberación de correpresores (como NCoR o SMRT) y el reclutamiento de coactivadores transcripcionales, incluyendo proteínas como PGC-1α o CBP/p300. Este proceso permite la formación de un complejo activo que, tras heterodimerizar con RXR, se une a secuencias PPRE en el ADN, promoviendo la transcripción de genes diana relacionados con el metabolismo lipídico y la homeostasis energética (Chawla et al., 2001; Feige et al., 2006).
Más allá de esta activación directa, PPARγ también ejerce efectos mediante mecanismos de transrepresión, interfiriendo con factores de transcripción proinflamatorios como NF-κB, AP-1 o STAT. Este efecto no depende necesariamente de la unión directa al ADN, sino de interacciones proteína-proteína que limitan la capacidad de estos factores para activar genes inflamatorios. Como resultado, la activación de PPARγ puede reducir la expresión de citocinas, quimioquinas y otras moléculas implicadas en la respuesta inflamatoria (Ricote et al., 1998; Pascual et al., 2005).
Un aspecto especialmente relevante es que distintos ligandos pueden inducir conformaciones estructurales específicas del receptor, modulando selectivamente la interacción con cofactores. Este fenómeno, conocido como modulación conformacional o “biased agonism” en receptores nucleares, explica por qué diferentes agonistas de PPARγ pueden generar perfiles de expresión génica divergentes, incluso dentro del mismo tipo celular (Choi et al., 2010).
En el contexto del sistema endocannabinoide ampliado, algunos lípidos bioactivos pueden activar PPARγ de forma directa o indirecta, integrando señales metabólicas con regulación génica. Esta interacción no sigue necesariamente los patrones clásicos de agonismo farmacológico, sino que puede implicar rutas metabólicas intermedias, cambios en la disponibilidad de ligandos o modulación de cofactores celulares, lo que añade una capa adicional de complejidad a su regulación (O’Sullivan, 2007).
Finalmente, la actividad de PPARγ está sujeta a regulación postraduccional mediante fosforilación, sumoilación o ubiquitinación, modificaciones que pueden alterar su estabilidad, localización o capacidad transcripcional. Estas capas adicionales de control permiten una regulación dinámica del receptor en función del estado celular y del entorno fisiológico (Feige & Auwerx, 2007).
Interacción con el sistema endocannabinoide
El receptor PPARγ forma parte del conjunto ampliado de dianas moleculares que interactúan con lípidos bioactivos relacionados con el sistema endocannabinoide, también denominado endocannabinoidome. A diferencia de los receptores clásicos como CB1 o CB2, que son receptores de membrana acoplados a proteínas G, PPARγ actúa a nivel nuclear como regulador transcripcional, ampliando el espectro funcional de estas señales lipídicas (O’Sullivan, 2007).
Diversos endocannabinoides y lípidos estructuralmente relacionados han mostrado capacidad para modular la actividad de PPARγ. Entre ellos destacan compuestos como la anandamida (AEA) y el 2-araquidonoilglicerol (2-AG), así como otros mediadores lipídicos como la oleoiletanolamida (OEA) o la palmitoiletanolamida (PEA). Estos compuestos pueden actuar como ligandos directos o influir indirectamente en la activación del receptor a través de rutas metabólicas interconectadas (Pistis & Melis, 2010).
En el caso de los fitocannabinoides, se ha descrito que algunos compuestos derivados de la planta de cannabis, como el cannabidiol (CBD), pueden interactuar con PPARγ, ya sea mediante activación directa o modulando su actividad de forma indirecta. Esta interacción no sigue necesariamente los patrones clásicos de agonismo, sino que puede implicar efectos moduladores dependientes del contexto celular y de la disponibilidad de cofactores (O’Sullivan, 2007).
Desde una perspectiva funcional, la activación de PPARγ por lípidos relacionados con el sistema endocannabinoide permite conectar señales metabólicas con respuestas génicas a largo plazo. Mientras que la activación de receptores de membrana genera respuestas rápidas, la activación de PPARγ introduce una capa adicional de regulación más sostenida, modulando la expresión de genes implicados en metabolismo, inflamación y diferenciación celular (Pistis & Melis, 2010).
Esta convergencia sitúa a PPARγ como un nodo clave en la integración de señales lipídicas dentro del organismo, ampliando la comprensión del sistema endocannabinoide más allá de sus receptores clásicos y reforzando el concepto de una red funcional compleja en la que múltiples dianas moleculares cooperan en la regulación de la homeostasis (O’Sullivan, 2007).
Importancia en investigación científica
El receptor PPARγ se ha consolidado como una de las dianas moleculares más estudiadas en biología metabólica e inflamatoria, debido a su capacidad para integrar señales lipídicas y traducirlas en cambios coordinados en la expresión génica. Esta característica lo sitúa en el centro de múltiples líneas de investigación que abarcan desde el metabolismo energético hasta la inmunología y la biología celular (Lehrke & Lazar, 2005).
En el ámbito metabólico, PPARγ ha sido fundamental para comprender los mecanismos que regulan la adipogénesis, la sensibilidad a la insulina y la distribución del tejido adiposo. Su estudio ha permitido redefinir el papel del tejido adiposo, pasando de ser considerado un simple depósito energético a entenderse como un órgano endocrino activo, capaz de modular procesos sistémicos mediante la secreción de adipocinas (Rosen & Spiegelman, 2001).
Desde una perspectiva inmunológica, la investigación sobre PPARγ ha contribuido a esclarecer cómo los procesos metabólicos y la respuesta inflamatoria están profundamente interconectados. Su capacidad para modular la actividad de células inmunitarias ha abierto nuevas vías para explorar la regulación de la inflamación en distintos contextos fisiológicos y patológicos, consolidando el concepto de inmunometabolismo (Ricote et al., 1998; Bouhlel et al., 2007).
En neurociencia, el interés por PPARγ ha crecido en relación con su papel en la regulación de la neuroinflamación y el metabolismo cerebral. Aunque su función en el sistema nervioso central es más compleja y menos definida que en otros tejidos, su estudio ha aportado información relevante sobre la interacción entre metabolismo energético, inflamación y función neuronal (Bernardo & Minghetti, 2008).
Además, la conexión de PPARγ con el sistema endocannabinoide ampliado ha ampliado su relevancia en investigación básica, al situarlo como un punto de convergencia entre lípidos bioactivos y regulación transcripcional. Esta perspectiva ha favorecido el desarrollo de enfoques más integradores, en los que diferentes sistemas de señalización se estudian como redes interconectadas en lugar de vías aisladas (O’Sullivan, 2007).
En conjunto, la investigación sobre PPARγ ha contribuido a cambiar la forma en que se entienden procesos fundamentales como el metabolismo, la inflamación y la regulación génica, consolidando su papel como un nodo central en la fisiología molecular contemporánea y como una diana de interés continuo en biomedicina.
Referencias
- Issemann, I., & Green, S. (1990). Activation of a member of the steroid hormone receptor superfamily by peroxisome proliferators. Nature, 347(6294), 645–650. - Tontonoz, P., Hu, E., & Spiegelman, B. M. (1994). Stimulation of adipogenesis in fibroblasts by PPARγ, a lipid-activated transcription factor. Cell, 79(7), 1147–1156. - Zhu, Y., Qi, C., Jain, S., Rao, M. S., & Reddy, J. K. (1995). Isolation and characterization of PPARγ cDNA and its tissue distribution. Biochemical and Biophysical Research Communications, 209(3), 1018–1025. - Lehmann, J. M., Moore, L. B., Smith-Oliver, T. A., et al. (1995). An antidiabetic thiazolidinedione is a high affinity ligand for PPARγ. Journal of Biological Chemistry, 270(22), 12953–12956. - Forman, B. M., Tontonoz, P., Chen, J., et al. (1995). 15-deoxy-Δ12,14-prostaglandin J2 is a ligand for the adipocyte determination factor PPARγ. Cell, 83(5), 803–812. - Nolte, R. T., Wisely, G. B., Westin, S., et al. (1998). Ligand binding and co-activator assembly of the PPARγ ligand-binding domain. Nature, 395(6698), 137–143. - Ricote, M., Li, A. C., Willson, T. M., et al. (1998). The peroxisome proliferator-activated receptor-γ is a negative regulator of macrophage activation. Nature, 391(6662), 79–82. - Chawla, A., Repa, J. J., Evans, R. M., & Mangelsdorf, D. J. (2001). Nuclear receptors and lipid physiology: opening the X-files. Science, 294(5548), 1866–1870. - Rosen, E. D., & Spiegelman, B. M. (2001). PPARγ: a nuclear regulator of metabolism, differentiation, and cell growth. Journal of Biological Chemistry, 276(41), 37731–37734. - Evans, R. M., Barish, G. D., & Wang, Y. X. (2004). PPARs and the complex journey to obesity. Nature Medicine, 10(4), 355–361. - Lehrke, M., & Lazar, M. A. (2005). The many faces of PPARγ. Cell, 123(6), 993–999. - Glass, C. K., & Ogawa, S. (2006). Combinatorial roles of nuclear receptors in inflammation and immunity. Nature Reviews Immunology, 6(1), 44–55. - Feige, J. N., Gelman, L., Michalik, L., et al. (2006). From molecular action to physiological outputs: PPARγ regulation of energy metabolism. Progress in Lipid Research, 45(2), 120–159. - O’Sullivan, S. E. (2007). Cannabinoids go nuclear: evidence for activation of PPARs. British Journal of Pharmacology, 152(5), 576–582. - Bernardo, A., & Minghetti, L. (2008). PPAR-γ agonists as regulators of microglial activation and brain inflammation. Current Pharmaceutical Design, 14(16), 1606–1615. - Bouhlel, M. A., Derudas, B., Rigamonti, E., et al. (2007). PPARγ activation primes human monocytes into alternative M2 macrophages. Cell Metabolism, 6(2), 137–143. - Chandra, V., Huang, P., Hamuro, Y., et al. (2008). Structure of the intact PPARγ–RXR nuclear receptor complex on DNA. Nature, 456(7220), 350–356. - Pistis, M., & Melis, M. (2010). From surface to nuclear receptors: the endocannabinoid family extends its assets. Current Medicinal Chemistry, 17(14), 1450–1467. - Choi, J. H., Banks, A. S., Estall, J. L., et al. (2010). Anti-diabetic drugs inhibit obesity-linked phosphorylation of PPARγ. Nature, 466(7305), 451–456. - Kadowaki, T., Yamauchi, T., Kubota, N., et al. (2006). Adiponectin and adiponectin receptors in insulin resistance. Journal of Clinical Investigation, 116(7), 1784–1792. - Seale, P., Bjork, B., Yang, W., et al. (2011). PRDM16 controls a brown fat/skeletal muscle switch. Nature, 454(7207), 961–967. - Su, C. G., Wen, X., Bailey, S. T., et al. (1999). A novel therapy for colitis utilizing PPARγ ligands to inhibit the epithelial inflammatory response. Journal of Clinical Investigation, 104(4), 383–389. - Moreno, S., Farioli-Vecchioli, S., & Cerù, M. P. (2004). Immunolocalization of PPARs in the rat CNS. Journal of Comparative Neurology, 472(4), 464–474. - Feige, J. N., & Auwerx, J. (2007). Transcriptional targets of PPARγ: from lipid metabolism to inflammation. Trends in Endocrinology & Metabolism, 18(9), 366–373.