Introducción
La N-acyl phosphatidylethanolamine phospholipase D (NAPE-PLD) es una enzima clave en el sistema endocannabinoide responsable de la biosíntesis de N-aciletanolaminas (NAEs), entre las que destaca la anandamida (AEA), uno de los principales endocannabinoides implicados en la regulación de múltiples procesos fisiológicos. Esta enzima cataliza la hidrólisis de los fosfolípidos de membrana tipo NAPE (N-acil-fosfatidiletanolamina), liberando directamente NAEs en respuesta a estímulos celulares específicos, especialmente en contextos de señalización neuronal y estrés fisiológico (Okamoto et al., 2004; Ueda et al., 2013).
A diferencia de otras rutas metabólicas más complejas, la NAPE-PLD representa una vía relativamente directa para la producción de anandamida, lo que la sitúa como un nodo central dentro de la regulación fina del tono endocannabinoide. Su actividad está estrechamente ligada a la dinámica de membrana y a la disponibilidad de precursores lipídicos, lo que sugiere que la síntesis de endocannabinoides no es un proceso constitutivo, sino altamente dependiente del estado celular y del contexto fisiológico (Di Marzo et al., 1994; Simon & Cravatt, 2006).
Desde un punto de vista funcional, la NAPE-PLD no solo participa en la generación de anandamida, sino también en la producción de otras NAEs bioactivas como la palmitoiletanolamida (PEA) y la oleoiletanolamida (OEA), moléculas implicadas en la modulación de la inflamación, el metabolismo energético y la señalización periférica. Este hecho amplía su relevancia más allá del sistema endocannabinoide clásico, integrándola dentro de lo que actualmente se denomina endocannabinoidoma (Piomelli et al., 2014; Tsuboi et al., 2018).
En conjunto, la NAPE-PLD actúa como una enzima reguladora clave en la generación de señales lipídicas con función neuromoduladora, participando en procesos como la homeostasis, la percepción del dolor, la respuesta al estrés y la regulación del apetito. Su estudio ha permitido comprender mejor cómo se generan los endocannabinoides “a demanda” y cómo se integran en redes de señalización más amplias dentro del organismo (Lu & Mackie, 2016; Ueda et al., 2013).
Historia del descubrimiento
El estudio de la NAPE-PLD está directamente ligado a la búsqueda de las rutas biosintéticas responsables de la formación de la anandamida (AEA) tras su descubrimiento en 1992. Durante los primeros años, se sabía que la anandamida derivaba de fosfolípidos de membrana, pero los mecanismos enzimáticos exactos que permitían su liberación permanecían poco claros. Las primeras hipótesis apuntaban a rutas multietapa que implicaban varias enzimas intermedias, lo que dificultaba la comprensión global del proceso (Devane et al., 1992; Di Marzo et al., 1994).
El avance clave se produjo a principios de los años 2000, cuando el grupo de Okamoto y colaboradores (2004) identificó y caracterizó por primera vez una enzima capaz de hidrolizar directamente las N-acil-fosfatidiletanolaminas (NAPE)para generar N-aciletanolaminas, incluida la anandamida. Esta enzima fue denominada NAPE-PLD, estableciendo una vía biosintética más directa y eficiente en comparación con los modelos previos. Este descubrimiento supuso un punto de inflexión en la comprensión de la síntesis de endocannabinoides, al demostrar que podían generarse mediante mecanismos enzimáticos específicos y regulados.
Posteriormente, estudios estructurales y bioquímicos confirmaron que la NAPE-PLD pertenece a la familia de las fosfolipasas tipo D y que presenta características únicas en comparación con otras enzimas lipídicas, incluyendo una dependencia de iones metálicos como el zinc para su actividad catalítica. Estas investigaciones también revelaron que la enzima está altamente conservada entre especies, lo que sugiere un papel fisiológico fundamental en la regulación de señales lipídicas (Okamoto et al., 2004; Wang et al., 2006).
A medida que avanzó la investigación, se observó que la NAPE-PLD no es la única vía para la producción de anandamida. Se identificaron rutas alternativas que pueden generar NAEs en ausencia o baja actividad de esta enzima, lo que introdujo el concepto de redundancia metabólica dentro del sistema endocannabinoide. Este hallazgo reforzó la idea de que la síntesis de endocannabinoides es un proceso flexible y adaptativo, capaz de responder a diferentes condiciones fisiológicas y celulares (Simon & Cravatt, 2006; Ueda et al., 2013).
En conjunto, el descubrimiento de la NAPE-PLD marcó un hito en la biología del sistema endocannabinoide, al proporcionar una base molecular clara para la síntesis de anandamida y abrir nuevas líneas de investigación sobre la regulación de los lípidos bioactivos en el organismo.
Estructura y características moleculares
La NAPE-PLD es una enzima perteneciente a la superfamilia de las metaloenzimas tipo fosfolipasa D, caracterizada por presentar un dominio catalítico dependiente de iones metálicos, principalmente zinc (Zn²⁺), que resulta esencial para su actividad hidrolítica. A nivel estructural, la NAPE-PLD muestra un plegamiento típico de las enzimas tipo metalo-β-lactamasa, lo que la diferencia de otras fosfolipasas D clásicas y sugiere un origen evolutivo distinto dentro del metabolismo lipídico (Wang et al., 2006; Okamoto et al., 2004).
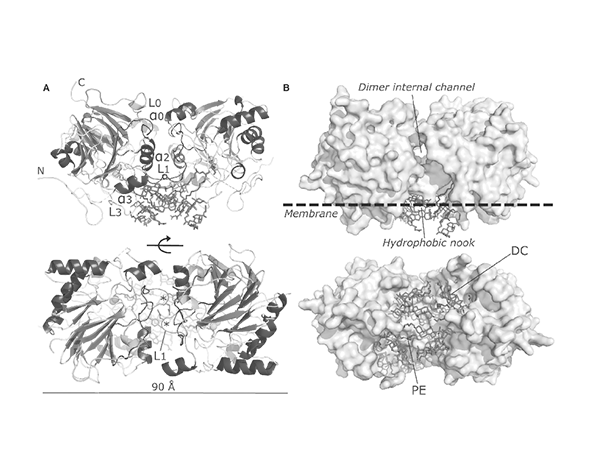
La estructura tridimensional de la NAPE-PLD, resuelta mediante cristalografía de rayos X, revela la presencia de un sitio activo binuclear en el que dos iones de zinc coordinan la activación de una molécula de agua, facilitando el ataque nucleofílico sobre el enlace fosfodiéster del sustrato NAPE. Este mecanismo catalítico permite la liberación directa de N-aciletanolaminas (NAEs) sin necesidad de intermediarios complejos, lo que confiere a la enzima una alta eficiencia en condiciones fisiológicas (Wang et al., 2006).
Además, la NAPE-PLD presenta una organización dimérica funcional, donde dos subunidades idénticas interactúan formando una estructura estable que contribuye a la regulación de su actividad. Esta dimerización no solo estabiliza la enzima, sino que también parece estar implicada en la correcta orientación de los sustratos lipídicos dentro de la membrana, facilitando su acceso al sitio activo (Okamoto et al., 2004).
Desde el punto de vista de su localización celular, la NAPE-PLD se asocia principalmente a membranas intracelulares, especialmente en compartimentos como el retículo endoplásmico y la membrana plasmática. Esta localización es coherente con la naturaleza lipídica de sus sustratos, ya que los NAPE se encuentran integrados en la bicapa lipídica, lo que implica que la actividad enzimática ocurre en un entorno de interfaz membrana-agua altamente dinámico (Ueda et al., 2013).
Otro aspecto relevante es la modulación alostérica de la enzima por lípidos de membrana, como los ácidos biliares y otros fosfolípidos, que pueden influir en su actividad catalítica. Este tipo de regulación sugiere que la NAPE-PLD no actúa de forma aislada, sino integrada en el contexto físico-químico de la membrana celular, donde cambios en la composición lipídica pueden alterar la producción de NAEs (Tsuboi et al., 2018).
En conjunto, la estructura de la NAPE-PLD refleja una adaptación específica para la generación de mediadores lipídicos en entornos de membrana, combinando un mecanismo catalítico eficiente con una regulación dependiente del contexto celular.
Mecanismo molecular de síntesis de anandamida
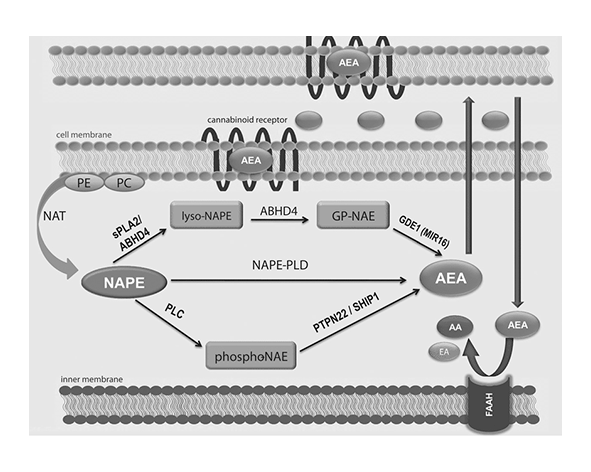
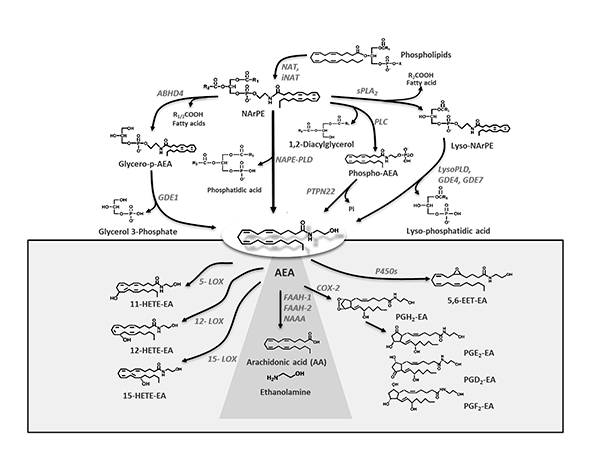
La NAPE-PLD cataliza la formación de anandamida (AEA) mediante la hidrólisis directa de N-acil-fosfatidiletanolaminas (NAPE), fosfolípidos presentes en la membrana celular que actúan como precursores inmediatos de las N-aciletanolaminas. Este proceso constituye una de las vías más directas y eficientes para la generación de endocannabinoides “a demanda”, en respuesta a estímulos fisiológicos específicos (Okamoto et al., 2004; Ueda et al., 2013).
El mecanismo catalítico comienza con la interacción de la NAPE-PLD con su sustrato dentro de la bicapa lipídica. La enzima reconoce la estructura del NAPE y lo posiciona adecuadamente en el sitio activo, donde los iones de zinc (Zn²⁺)desempeñan un papel clave. Estos iones coordinan la activación de una molécula de agua, generando un nucleófilo altamente reactivo que ataca el enlace fosfodiéster del sustrato, produciendo la escisión de la molécula y liberando anandamida (AEA) junto con un fosfolípido residual (Wang et al., 2006).
A diferencia de otras rutas biosintéticas más complejas, este mecanismo permite la generación de anandamida en un solo paso enzimático, lo que favorece una respuesta rápida y localizada. Este carácter “on demand” es fundamental en la señalización endocannabinoide, ya que la anandamida no se almacena en vesículas como los neurotransmisores clásicos, sino que se sintetiza en el momento en que es necesaria, generalmente en la neurona postsináptica (Di Marzo et al., 1994; Lu & Mackie, 2016).
Una vez liberada, la anandamida puede difundir a través de la membrana y activar receptores como CB1, CB2 u otras dianas moleculares como TRPV1, modulando la actividad neuronal y otros procesos celulares. Tras ejercer su función, es rápidamente degradada por enzimas como la FAAH (fatty acid amide hydrolase), lo que contribuye a la naturaleza transitoria de la señal endocannabinoide (Cravatt et al., 1996; Ueda et al., 2013).
Es importante destacar que la NAPE-PLD no es la única vía capaz de generar anandamida. Existen rutas alternativas que implican múltiples pasos enzimáticos, como la vía dependiente de fosfolipasas C y fosfatasas, lo que introduce redundancia en el sistema. Esta diversidad de mecanismos sugiere que la síntesis de anandamida puede adaptarse a diferentes condiciones fisiológicas, tipos celulares y estados metabólicos (Simon & Cravatt, 2006).
En conjunto, el mecanismo molecular mediado por la NAPE-PLD representa una estrategia eficiente y regulada para la producción de anandamida, integrando señales celulares, composición lipídica de membrana y control enzimático dentro de la dinámica del sistema endocannabinoide.
Distribución y contexto fisiológico
La NAPE-PLD presenta una distribución amplia en el organismo, aunque su expresión es especialmente relevante en tejidos con alta actividad de señalización lipídica, como el sistema nervioso central, el sistema digestivo, el tejido adiposo y diversos componentes del sistema inmunitario. Esta distribución refleja su papel fundamental en la generación de mediadores bioactivos implicados en la regulación de la homeostasis (Ueda et al., 2013; Tsuboi et al., 2018).
En el cerebro, la NAPE-PLD se expresa en neuronas y, en menor medida, en células gliales. Su actividad está estrechamente relacionada con la síntesis de anandamida en regiones implicadas en funciones como la memoria, la emoción, la percepción del dolor y el control del apetito. En este contexto, la producción “a demanda” de anandamida permite modular la neurotransmisión de forma retrógrada, actuando como un sistema de ajuste fino de la actividad sináptica (Lu & Mackie, 2016).
A nivel periférico, la NAPE-PLD desempeña un papel relevante en el intestino, donde participa en la producción de moléculas como la oleoiletanolamida (OEA), implicada en la regulación de la saciedad y el metabolismo energético. Esta función conecta directamente la actividad de la enzima con la señalización entre el sistema digestivo y el sistema nervioso, integrándose en lo que se conoce como eje intestino-cerebro (Piomelli et al., 2014).
En el tejido adiposo y en el hígado, la NAPE-PLD contribuye a la regulación del metabolismo lipídico mediante la generación de NAEs que modulan procesos como la lipólisis, la inflamación y la sensibilidad a la insulina. Estos efectos no se limitan a la anandamida, sino que incluyen otras NAEs con funciones específicas en la homeostasis energética (Tsuboi et al., 2018).
En el ámbito del sistema inmunitario, la actividad de la NAPE-PLD se ha relacionado con la producción de mediadores que pueden modular la respuesta inflamatoria. Aunque estos mecanismos son complejos y dependen del contexto celular, la presencia de la enzima en células inmunes sugiere un papel en la regulación de la comunicación entre el sistema endocannabinoide y las vías inflamatorias clásicas (Ueda et al., 2013).
Además, la expresión de la NAPE-PLD puede variar en función de condiciones fisiológicas y patológicas, como el estrés, la inflamación o alteraciones metabólicas. Esta regulación dinámica refuerza la idea de que la enzima forma parte de un sistema adaptativo que responde a cambios en el entorno interno del organismo (Lu & Mackie, 2016).
En conjunto, la distribución de la NAPE-PLD pone de manifiesto su papel integrador en múltiples sistemas fisiológicos, actuando como un punto de conexión entre la señalización lipídica, el metabolismo y la regulación de la homeostasis.
Interacción con fitocannabinoides y endocannabinoidoma
La NAPE-PLD no actúa de forma aislada dentro del sistema endocannabinoide, sino que se integra en una red más amplia conocida como endocannabinoidoma, que engloba no solo a los endocannabinoides clásicos como la anandamida (AEA), sino también a múltiples lípidos bioactivos relacionados, sus enzimas de síntesis y degradación, y una amplia variedad de receptores diana (Piomelli et al., 2014).
En este contexto, la NAPE-PLD desempeña un papel central al generar no solo anandamida, sino también otras N-aciletanolaminas (NAEs) como la palmitoiletanolamida (PEA) y la oleoiletanolamida (OEA). Estas moléculas no activan directamente los receptores cannabinoides clásicos CB1 y CB2, pero sí interactúan con otras dianas como PPAR-α, TRPV1 o GPRs huérfanos, ampliando significativamente el alcance funcional del sistema (Tsuboi et al., 2018; Piomelli et al., 2014).
La relación entre la NAPE-PLD y los fitocannabinoides, como el cannabidiol (CBD), es principalmente indirecta. El CBD no actúa como sustrato de la NAPE-PLD ni estimula directamente su actividad enzimática, pero puede modular el sistema endocannabinoide alterando el equilibrio entre síntesis y degradación de endocannabinoides. Uno de los mecanismos más estudiados es la inhibición funcional de la FAAH, lo que puede aumentar los niveles de anandamida al reducir su degradación, potenciando así el efecto de la vía biosintética en la que participa la NAPE-PLD (Bisogno et al., 2001; Ibeas Bih et al., 2015).
Además, algunos estudios sugieren que cambios en la composición lipídica de la membrana inducidos por fitocannabinoides podrían influir indirectamente en la actividad de la NAPE-PLD, dado que esta enzima depende del entorno de membrana para acceder a sus sustratos. Este tipo de interacción refuerza la idea de que los fitocannabinoides pueden modular el sistema no solo a nivel receptor, sino también en etapas previas de la señalización, como la síntesis de mediadores (Di Marzo, 2018).
Otro aspecto relevante es la sinergia funcional entre NAEs, donde moléculas como PEA y OEA pueden potenciar o modular los efectos de la anandamida a través de mecanismos como el llamado “entourage effect”. Aunque este concepto sigue siendo objeto de debate científico, refleja la complejidad del sistema y la dificultad de atribuir efectos biológicos a una única molécula o vía metabólica (Piomelli et al., 2014).
En este marco, la NAPE-PLD se posiciona como un nodo estratégico dentro del endocannabinoidoma, al controlar la disponibilidad de múltiples mediadores lipídicos que actúan sobre distintas dianas moleculares. Su actividad contribuye a la generación de una señalización integrada, donde los efectos finales dependen de la interacción entre múltiples rutas, enzimas y receptores.
En conjunto, la relación entre la NAPE-PLD, los endocannabinoides y los fitocannabinoides ilustra cómo el sistema endocannabinoide funciona como una red compleja y adaptativa, más allá de un modelo lineal basado únicamente en los receptores CB1 y CB2.
Importancia en investigación y relevancia biomédica
La NAPE-PLD ha adquirido un papel relevante en la investigación biomédica como enzima clave en la regulación de lípidos bioactivos implicados en múltiples procesos fisiológicos. Su capacidad para controlar la síntesis de anandamida (AEA) y otras N-aciletanolaminas (NAEs) la convierte en un punto estratégico para comprender cómo se modulan funciones como la señalización neuronal, el metabolismo energético y la respuesta inflamatoria (Ueda et al., 2013; Tsuboi et al., 2018).
En el ámbito de la neurociencia, la NAPE-PLD ha sido estudiada por su implicación en la regulación de la neurotransmisión y la plasticidad sináptica. Alteraciones en la producción de anandamida pueden influir en procesos como la percepción del dolor, la respuesta al estrés o la modulación emocional. Aunque estos mecanismos son complejos y aún están en investigación, la enzima se considera una pieza relevante dentro de las redes que regulan la homeostasis neuronal (Lu & Mackie, 2016).
En relación con el metabolismo, la NAPE-PLD participa indirectamente en la regulación del apetito y del equilibrio energético a través de la producción de moléculas como la oleoiletanolamida (OEA). Estudios experimentales han mostrado que cambios en la actividad de esta vía pueden asociarse a alteraciones en el peso corporal, la ingesta de alimentos y la señalización metabólica, lo que ha despertado interés en su estudio dentro del contexto de trastornos metabólicos (Piomelli et al., 2014).
Asimismo, la enzima ha sido investigada en el contexto de la inflamación y la respuesta inmune. Las NAEs generadas por la NAPE-PLD pueden interactuar con diferentes dianas moleculares implicadas en la modulación de procesos inflamatorios, lo que sugiere un posible papel en la regulación de la respuesta del organismo ante distintos estímulos. Sin embargo, estos efectos dependen del contexto celular y del equilibrio global del sistema endocannabinoide (Ueda et al., 2013).
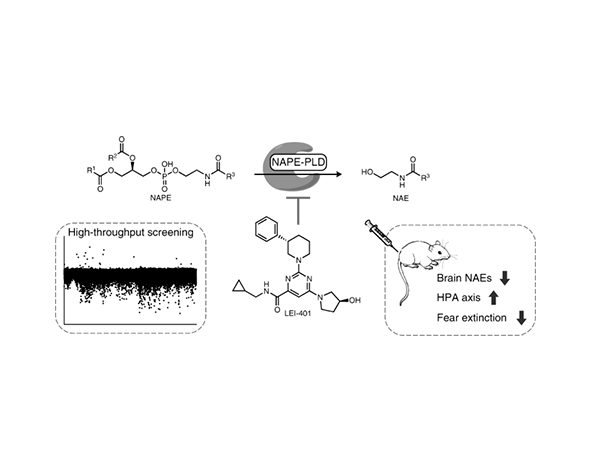
Desde el punto de vista farmacológico, la NAPE-PLD se ha considerado una posible diana para modular los niveles de endocannabinoides. A diferencia de las estrategias centradas en receptores, el enfoque sobre enzimas de síntesis permite intervenir en etapas más tempranas de la señalización. No obstante, el desarrollo de moduladores selectivos de la NAPE-PLD presenta desafíos importantes, debido a la complejidad del sistema y a la existencia de vías biosintéticas alternativas que pueden compensar su inhibición (Simon & Cravatt, 2006).
Además, estudios recientes han explorado la relación entre la NAPE-PLD y la microbiota intestinal, sugiriendo que ciertos metabolitos bacterianos podrían influir en la actividad de esta enzima y, por tanto, en la producción de NAEs. Este campo emergente abre nuevas perspectivas sobre la interacción entre el metabolismo lipídico, el sistema endocannabinoide y el ecosistema microbiano del organismo (Di Marzo, 2018).
En conjunto, la NAPE-PLD representa una pieza clave en la investigación del sistema endocannabinoide y del endocannabinoidoma, no solo por su papel en la síntesis de mediadores lipídicos, sino también por su integración en redes fisiológicas complejas. Su estudio continúa aportando información relevante sobre los mecanismos que regulan el equilibrio interno del organismo.
Referencias
- Bisogno, T., Hanus, L., De Petrocellis, L., Tchilibon, S., Ponde, D. E., Brandi, I., Moriello, A. S., Davis, J. B., Mechoulam, R., & Di Marzo, V. (2001). Molecular targets for cannabidiol and its synthetic analogues: Effect on vanilloid VR1 receptors and on the cellular uptake and enzymatic hydrolysis of anandamide. British Journal of Pharmacology, 134(4), 845–852. - Cravatt, B. F., Giang, D. K., Mayfield, S. P., Boger, D. L., Lerner, R. A., & Gilula, N. B. (1996). Molecular characterization of an enzyme that degrades neuromodulatory fatty-acid amides. Nature, 384(6604), 83–87. - Devane, W. A., Hanus, L., Breuer, A., Pertwee, R. G., Stevenson, L. A., Griffin, G., Gibson, D., Mandelbaum, A., Etinger, A., & Mechoulam, R. (1992). Isolation and structure of a brain constituent that binds to the cannabinoid receptor. Science, 258(5090), 1946–1949. - Di Marzo, V., Fontana, A., Cadas, H., Schinelli, S., Cimino, G., Schwartz, J. C., & Piomelli, D. (1994). Formation and inactivation of endogenous cannabinoid anandamide in central neurons. Nature, 372(6507), 686–691. - Di Marzo, V. (2018). New approaches and challenges to targeting the endocannabinoid system. Nature Reviews Drug Discovery, 17(9), 623–639. - Ibeas Bih, C., Chen, T., Nunn, A. V., Bazelot, M., Dallas, M., & Whalley, B. J. (2015). Molecular targets of cannabidiol in neurological disorders. Neurotherapeutics, 12(4), 699–730. - Lu, H. C., & Mackie, K. (2016). An introduction to the endogenous cannabinoid system. Biological Psychiatry, 79(7), 516–525. - Okamoto, Y., Morishita, J., Tsuboi, K., Tonai, T., & Ueda, N. (2004). Molecular characterization of a phospholipase D generating anandamide and its congeners. Journal of Biological Chemistry, 279(7), 5298–5305. - Piomelli, D., Astarita, G., & Rapaka, R. (2014). A neuroscientist’s guide to lipidomics. Nature Reviews Neuroscience, 8(10), 743–754. - Simon, G. M., & Cravatt, B. F. (2006). Endocannabinoid biosynthesis proceeding through glycerophospho-N-acyl ethanolamine and a role for α/β-hydrolase 4 in this pathway. Journal of Biological Chemistry, 281(36), 26465–26472. - Tsuboi, K., Uyama, T., Okamoto, Y., & Ueda, N. (2018). Endocannabinoids and related N-acylethanolamines: Biological activities and metabolism. Inflammation and Regeneration, 38(1), 28. - Ueda, N., Tsuboi, K., & Uyama, T. (2013). N-acylethanolamine metabolism with special reference to N-acylethanolamine-hydrolyzing acid amidase (NAAA). Progress in Lipid Research, 52(4), 563–584. - Wang, J., Okamoto, Y., Morishita, J., Tsuboi, K., Miyatake, A., Ueda, N., & Yamamoto, M. (2006). Crystal structure of the phospholipase D-like domain of NAPE-PLD reveals a metallo-β-lactamase fold involved in lipid metabolism. Proceedings of the National Academy of Sciences, 103(47), 17670–17675.