Introducción
La inflamación es un proceso biológico esencial para la supervivencia del organismo, mediante el cual se detectan, contienen y eliminan estímulos potencialmente dañinos, incluyendo patógenos, daño tisular, toxinas o alteraciones internas. Lejos de ser un fenómeno patológico en sí mismo, constituye un mecanismo adaptativo altamente conservado evolutivamente cuyo objetivo principal es restaurar la homeostasis tras una agresión. (Medzhitov, 2008; Nathan, 2002).
Este proceso implica una respuesta coordinada entre el sistema inmunitario, el sistema vascular y múltiples sistemas de señalización celular. A nivel local, se caracteriza por cambios en la permeabilidad vascular, reclutamiento de células inmunes y liberación de mediadores inflamatorios como citocinas, quimiocinas y eicosanoides. Estos eventos permiten aislar el daño, eliminar el agente causal y activar mecanismos de reparación tisular. (Nathan & Ding, 2010; Libby, 2007).
Sin embargo, la inflamación no es un proceso binario, sino un continuo dinámico que puede evolucionar desde una respuesta aguda y resolutiva hacia estados crónicos cuando los mecanismos de regulación fallan o el estímulo persiste. La inflamación crónica de bajo grado se ha asociado con numerosas enfermedades complejas, incluyendo patologías cardiovasculares, metabólicas, neurodegenerativas y autoinmunes. (Hotamisligil, 2006; Furman et al., 2019).
En este contexto, el sistema endocannabinoide (SEC) ha emergido como un sistema modulador clave en la regulación de la inflamación. A través de la señalización mediada por receptores cannabinoides, ligandos endógenos y enzimas específicas, el SEC participa en el control de la intensidad, duración y resolución de la respuesta inflamatoria, actuando como un mecanismo homeostático que limita respuestas excesivas y contribuye al equilibrio fisiológico. (Klein, 2005; Turcotte et al., 2016).
Historia
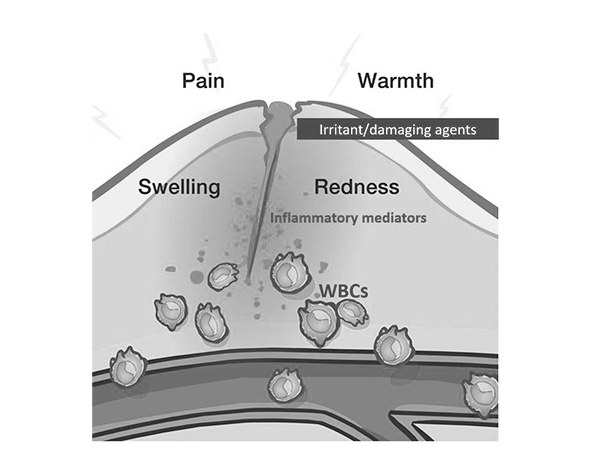
El concepto de inflamación tiene sus raíces en la medicina clásica, donde ya en el siglo I d.C., Aulo Cornelio Celso describió los cuatro signos cardinales: rubor (enrojecimiento), calor, tumor (hinchazón) y dolor. Esta caracterización macroscópica reflejaba una observación clínica directa de los cambios tisulares visibles durante procesos inflamatorios, constituyendo una de las primeras aproximaciones sistemáticas al fenómeno. (Majno & Joris, 2004).
Siglos más tarde, en el siglo XIX, Rudolf Virchow amplió esta descripción añadiendo el concepto de functio laesa(pérdida de función), consolidando así los cinco signos clásicos de la inflamación. Este avance coincidió con el desarrollo de la teoría celular, que permitió comenzar a interpretar la inflamación no solo como un fenómeno visible, sino como un proceso biológico que ocurre a nivel tisular y celular. (Virchow, 1858; Majno & Joris, 2004).
A finales del siglo XIX y principios del XX, los trabajos de Elie Metchnikoff marcaron un punto de inflexión en la comprensión de la inflamación al introducir el concepto de fagocitosis. Metchnikoff identificó el papel de células especializadas en la ingestión y eliminación de patógenos, estableciendo las bases de la inmunidad innata y posicionando la inflamación como un mecanismo activo de defensa biológica. (Gordon, 2008).
Durante el siglo XX, el avance de la bioquímica y la biología molecular permitió identificar los mediadores químicos implicados en la inflamación, incluyendo histamina, prostaglandinas, leucotrienos y citocinas. Este periodo transformó la visión de la inflamación, pasando de ser considerada una respuesta inespecífica a entenderse como un proceso altamente regulado, mediado por redes complejas de señalización celular. (Serhan et al., 2007; Nathan, 2002).
En las últimas décadas, la investigación ha profundizado en los mecanismos de resolución de la inflamación, destacando que este proceso no es pasivo, sino activamente regulado por mediadores específicos como las resolvinas, protectinas y maresinas. Este cambio conceptual ha sido clave para comprender cómo el organismo no solo inicia la inflamación, sino que también controla su finalización. (Serhan et al., 2007).
La implicación del sistema endocannabinoide en la regulación de la inflamación comenzó a explorarse a finales del siglo XX, tras la identificación de los receptores CB1 y CB2 y de los endocannabinoides como la anandamida y el 2-AG. Desde entonces, numerosos estudios han demostrado que el SEC actúa como un modulador de la respuesta inmune, integrándose en las redes de señalización que controlan tanto la activación como la resolución de la inflamación. (Klein, 2005; Turcotte et al., 2016).
Organización + distribución del SEC
El sistema endocannabinoide (SEC) presenta una amplia distribución en los tejidos implicados en la respuesta inflamatoria, configurando una red de señalización que conecta el sistema inmunitario, el sistema nervioso y los órganos periféricos. Sus componentes principales —receptores cannabinoides, endocannabinoides y enzimas metabólicas— permiten una regulación localizada y dinámica de los procesos inflamatorios en función del contexto fisiológico. (Di Marzo, 1998; Pertwee, 2008).
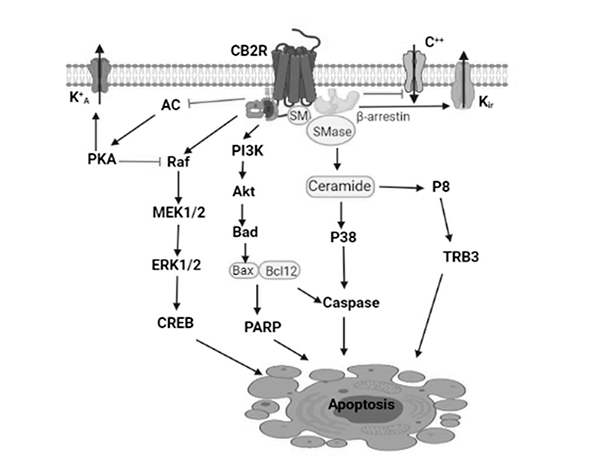
El receptor CB2 constituye uno de los elementos clave del SEC en el contexto de la inflamación. Se expresa predominantemente en células del sistema inmunitario, incluyendo macrófagos, linfocitos B y T, células dendríticas y neutrófilos. Su distribución no es estática, ya que puede aumentar en condiciones inflamatorias, lo que sugiere un papel adaptativo en la modulación de la respuesta inmune. (Klein, 2005; Cabral & Griffin-Thomas, 2009).
En tejidos periféricos, el receptor CB2 también se encuentra en órganos como el bazo, el hígado, el tracto gastrointestinal y la piel, todos ellos implicados en procesos inflamatorios locales o sistémicos. Esta distribución permite que el SEC actúe directamente sobre la respuesta inflamatoria en diferentes compartimentos del organismo, ajustando la intensidad de la señalización inmune. (Cabral & Griffin-Thomas, 2009; Turcotte et al., 2016).
El receptor CB1, aunque se asocia principalmente con el sistema nervioso central, también está presente en neuronas periféricas y en ciertos tipos celulares no neuronales. En el contexto de la inflamación, su papel se relaciona especialmente con la modulación neuroinmune y con la regulación de la percepción del dolor inflamatorio, integrando señales entre el sistema nervioso y el sistema inmunitario. (Pertwee, 2008; Lu & Mackie, 2016).
Los endocannabinoides, como la anandamida (AEA) y el 2-araquidonoilglicerol (2-AG), se sintetizan “a demanda” a partir de lípidos de membrana en respuesta a estímulos celulares. A diferencia de otros mediadores, no se almacenan en vesículas, lo que permite una señalización rápida y localizada en los sitios donde se produce la inflamación. Esta característica resulta clave para la regulación fina de la respuesta inflamatoria. (Di Marzo, 1998; Piomelli, 2003).
Las enzimas responsables de la síntesis y degradación de los endocannabinoides, como NAPE-PLD, DAGL, FAAH y MAGL, están igualmente distribuidas en células inmunes y tejidos periféricos. Su actividad determina la duración y la intensidad de la señal endocannabinoide, permitiendo un control temporal preciso de la modulación inflamatoria. (Blankman et al., 2007; Cravatt et al., 2001).
En conjunto, la organización del SEC en tejidos inflamatorios refleja su papel como sistema regulador distribuido, capaz de integrar señales locales y sistémicas para modular la respuesta inflamatoria y contribuir al mantenimiento de la homeostasis. (Turcotte et al., 2016).
Mecanismos
El sistema endocannabinoide (SEC) modula la inflamación a través de una red compleja de mecanismos celulares y moleculares que afectan tanto a la fase de activación como a la resolución del proceso inflamatorio. Esta modulación no actúa como un interruptor binario, sino como un sistema de ajuste fino que regula la intensidad, duración y localización de la respuesta inmune en función del contexto fisiológico. (Turcotte et al., 2016; Nagarkatti et al., 2009).
Uno de los mecanismos principales implica la regulación de la producción de citocinas. La activación del receptor CB2 en células inmunes se asocia con una disminución en la liberación de citocinas proinflamatorias como TNF-α, IL-1β e IL-6, así como con un aumento relativo de mediadores con perfil antiinflamatorio. Este efecto contribuye a limitar la amplificación de la respuesta inflamatoria y a prevenir daño tisular excesivo. (Klein, 2005; Cabral & Griffin-Thomas, 2009).
El SEC también modula la migración y el reclutamiento de células inmunes hacia los sitios de inflamación. A través de la señalización cannabinoide, se regulan procesos como la quimiotaxis, la adhesión celular y la extravasación leucocitaria, lo que permite controlar la magnitud de la infiltración celular en el tejido afectado. Este control resulta clave para evitar respuestas inflamatorias desproporcionadas. (Turcotte et al., 2016).
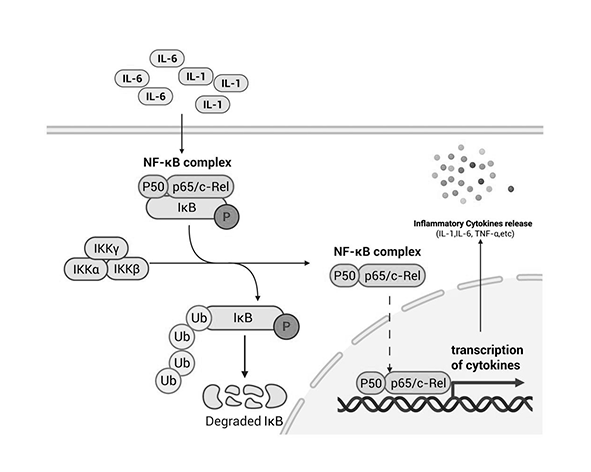
A nivel intracelular, los cannabinoides interfieren con vías de señalización fundamentales en la inflamación, como NF-κB y MAPK. Estas rutas regulan la expresión de genes implicados en la producción de mediadores inflamatorios, por lo que su modulación por el SEC tiene un impacto directo en la respuesta celular frente a estímulos inflamatorios. (Nagarkatti et al., 2009; Pertwee, 2008).
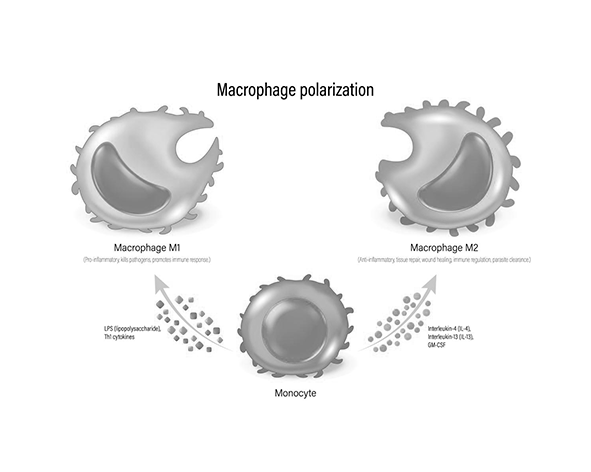
Además, el SEC influye en la polarización de macrófagos, favoreciendo en determinados contextos la transición desde fenotipos proinflamatorios (M1) hacia estados más asociados a la resolución y reparación tisular (M2). Este cambio funcional contribuye a la terminación del proceso inflamatorio y al restablecimiento del equilibrio tisular. (Nagarkatti et al., 2009).
Otro aspecto relevante es la interacción del SEC con otros sistemas de señalización lipídica, como la vía de los eicosanoides. Dado que los endocannabinoides y los eicosanoides comparten precursores metabólicos, existe una interconexión funcional que influye en la producción de mediadores inflamatorios derivados del ácido araquidónico. (Di Marzo, 1998; Pacher et al., 2006).
Finalmente, el SEC participa en los mecanismos de resolución activa de la inflamación, promoviendo la limitación de la respuesta inmune y facilitando procesos de reparación tisular. Este papel integrador refuerza su función como sistema homeostático que no solo modula la activación inflamatoria, sino también su correcta finalización. (Serhan et al., 2007; Turcotte et al., 2016).
Funciones fisiológicas
La inflamación cumple funciones fisiológicas esenciales para la supervivencia del organismo, actuando como un mecanismo de defensa, adaptación y reparación frente a agresiones internas y externas. Lejos de ser un proceso exclusivamente patológico, su correcta activación y resolución son fundamentales para mantener la integridad tisular y la homeostasis sistémica. (Medzhitov, 2008; Nathan, 2002).
Una de sus funciones principales es la eliminación de agentes nocivos, como patógenos o toxinas. A través de la activación de células del sistema inmunitario, especialmente neutrófilos y macrófagos, la inflamación permite identificar, contener y destruir microorganismos invasores mediante procesos como la fagocitosis y la liberación de mediadores antimicrobianos. (Nathan, 2002; Gordon, 2008).
La inflamación también desempeña un papel clave en la limpieza de tejidos dañados. Tras una lesión, se activan mecanismos que permiten la eliminación de células muertas, restos celulares y componentes extracelulares alterados, preparando el entorno para la regeneración y reparación tisular. Este proceso es esencial para evitar la acumulación de material dañado y mantener la funcionalidad del tejido. (Serhan et al., 2007).
Otra función fundamental es la activación de la reparación tisular. La inflamación coordina la liberación de factores de crecimiento y la activación de células implicadas en la regeneración, como fibroblastos y células endoteliales. Estos procesos favorecen la angiogénesis, la síntesis de matriz extracelular y la restauración de la estructura del tejido. (Eming et al., 2014).
Además, la inflamación actúa como un sistema de señalización que alerta al organismo sobre la presencia de daño o infección. A través de la liberación de citocinas y otros mediadores, se generan respuestas sistémicas como la fiebre o la activación del eje neuroendocrino, lo que permite una respuesta coordinada a nivel del organismo completo. (Medzhitov, 2008).
En condiciones fisiológicas, la inflamación está estrechamente regulada para evitar respuestas excesivas o prolongadas. El sistema endocannabinoide participa en esta regulación modulando la intensidad de la respuesta inmune y facilitando su resolución. Este control es esencial para mantener el equilibrio entre defensa y daño, evitando la progresión hacia estados inflamatorios crónicos. (Klein, 2005; Turcotte et al., 2016).
Por tanto, la inflamación no debe entenderse únicamente como un proceso negativo, sino como una función fisiológica crítica cuya correcta regulación determina en gran medida la salud y el equilibrio del organismo. (Nathan & Ding, 2010).
Implicaciones
La inflamación, cuando se encuentra correctamente regulada, constituye un mecanismo protector esencial. Sin embargo, su desregulación —ya sea por activación excesiva, persistencia del estímulo o fallos en los mecanismos de resolución— puede contribuir de manera significativa al desarrollo y progresión de múltiples enfermedades. En este sentido, la inflamación crónica de bajo grado se ha consolidado como un denominador común en numerosas patologías complejas. (Hotamisligil, 2006; Furman et al., 2019).
En el ámbito cardiovascular, la inflamación desempeña un papel central en la aterosclerosis, donde la acumulación de lípidos y células inmunes en la pared arterial genera placas que pueden comprometer el flujo sanguíneo. Este proceso inflamatorio sostenido contribuye a la inestabilidad de las placas y al riesgo de eventos como infarto de miocardio o accidente cerebrovascular. (Libby, 2007).
En enfermedades metabólicas, como la obesidad y la diabetes tipo 2, la inflamación crónica de bajo grado en tejidos como el adiposo y el hígado altera la señalización de la insulina y favorece la disfunción metabólica. Este estado inflamatorio persistente se asocia con resistencia a la insulina y con el desarrollo de complicaciones sistémicas. (Hotamisligil, 2006).
A nivel del sistema nervioso, la neuroinflamación se ha relacionado con enfermedades neurodegenerativas como el Alzheimer o el Parkinson. La activación sostenida de células gliales y la liberación de mediadores inflamatorios pueden contribuir al daño neuronal progresivo y a la alteración de la función cognitiva. (Glass et al., 2010).
Asimismo, la inflamación juega un papel relevante en enfermedades autoinmunes, donde el sistema inmunitario responde de forma inapropiada contra tejidos propios. En estos casos, la inflamación no solo no resuelve un daño, sino que se convierte en el principal mecanismo de lesión tisular. (Davidson & Diamond, 2001).
En este contexto, el sistema endocannabinoide adquiere relevancia como modulador de estos procesos. Su capacidad para regular la respuesta inmune, limitar la producción de mediadores proinflamatorios y favorecer la resolución de la inflamación ha sido objeto de investigación en múltiples modelos experimentales. Sin embargo, estos efectos deben interpretarse dentro de un marco fisiológico y regulatorio, evitando simplificaciones o extrapolaciones clínicas directas. (Klein, 2005; Turcotte et al., 2016).
Por tanto, comprender la inflamación no solo como un proceso aislado, sino como un eje central en la fisiopatología de múltiples enfermedades, resulta clave para el desarrollo de estrategias de investigación y aproximaciones terapéuticas más precisas. (Nathan & Ding, 2010).
Véase también
Referencias
- Cabral GA, Griffin-Thomas L. (2009). Emerging role of the cannabinoid receptor CB2 in immune regulation: therapeutic prospects for neuroinflammation. Expert Reviews in Molecular Medicine. - Cravatt BF, Giang DK, Mayfield SP, et al. (2001). Molecular characterization of an enzyme that degrades neuromodulatory fatty-acid amides. Nature. - Davidson A, Diamond B. (2001). Autoimmune diseases. New England Journal of Medicine. - Di Marzo V. (1998). ‘Endocannabinoids’ and other fatty acid derivatives with cannabimimetic properties: biochemistry and possible physiopathological relevance. Biochimica et Biophysica Acta. - Eming SA, Wynn TA, Martin P. (2014). Inflammation and metabolism in tissue repair and regeneration. Science. - Furman D, Campisi J, Verdin E, et al. (2019). Chronic inflammation in the etiology of disease across the life span. Nature Medicine. - Glass CK, Saijo K, Winner B, et al. (2010). Mechanisms underlying inflammation in neurodegeneration. Cell. - Gordon S. (2008). Elie Metchnikoff: father of natural immunity. Nature Reviews Immunology. - Hotamisligil GS. (2006). Inflammation and metabolic disorders. Nature. - Klein TW. (2005). Cannabinoid-based drugs as anti-inflammatory therapeutics. Nature Reviews Immunology. - Libby P. (2007). Inflammatory mechanisms: the molecular basis of inflammation and disease. Nutrition Reviews. - Majno G, Joris I. (2004). Cells, tissues, and disease: principles of general pathology. Oxford University Press. - Medzhitov R. (2008). Origin and physiological roles of inflammation. Nature. - Nagarkatti P, Pandey R, Rieder SA, et al. (2009). Cannabinoids as novel anti-inflammatory drugs. Future Medicinal Chemistry. - Nathan C. (2002). Points of control in inflammation. Nature. - Nathan C, Ding A. (2010). Nonresolving inflammation. Cell. - Pacher P, Batkai S, Kunos G. (2006). The endocannabinoid system as an emerging target of pharmacotherapy. Pharmacological Reviews. - Pertwee RG. (2008). The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids. British Journal of Pharmacology. - Serhan CN, Chiang N, Van Dyke TE. (2007). Resolving inflammation: dual anti-inflammatory and pro-resolution lipid mediators. Nature Reviews Immunology. - Turcotte C, Blanchet MR, Laviolette M, Flamand N. (2016). The CB2 receptor and its role as a regulator of inflammation. Cellular and Molecular Life Sciences.