Introducción
El denominado efecto séquito (entourage effect) describe un fenómeno farmacológico en el que múltiples compuestos presentes en la planta de Cannabis sativa —incluyendo fitocannabinoides, terpenos y flavonoides— interactúan entre sí generando respuestas biológicas que no pueden explicarse únicamente por la acción de un solo compuesto aislado. Este concepto plantea un modelo de actividad basado en la complejidad química y funcional de la planta, alejándose del enfoque reduccionista clásico de “una molécula, una diana” (Russo, 2011; Di Marzo, 2018).
El término fue introducido inicialmente en el contexto del sistema endocannabinoide para describir cómo ciertos lípidos endógenos estructuralmente relacionados, considerados en un principio inactivos, podían modular la actividad de endocannabinoides principales como el 2-araquidonoilglicerol (2-AG). Este hallazgo supuso un cambio conceptual relevante, al demostrar que la actividad biológica dentro del sistema endocannabinoide podía depender de interacciones cooperativas entre múltiples mediadores lipídicos (Ben-Shabat et al., 1998; Di Marzo, 2018).
Posteriormente, el concepto de efecto séquito fue extrapolado al ámbito del cannabis vegetal, donde se ha propuesto que la combinación de fitocannabinoides como el cannabidiol (CBD) y el Δ9-tetrahidrocannabinol (THC), junto con terpenos y otros metabolitos secundarios, puede dar lugar a perfiles farmacológicos diferenciados respecto a los compuestos aislados. Estas interacciones pueden influir en la afinidad por receptores cannabinoides, la activación de dianas moleculares no cannabinoides y la farmacocinética global de los compuestos (Russo, 2011; Pertwee, 2008).
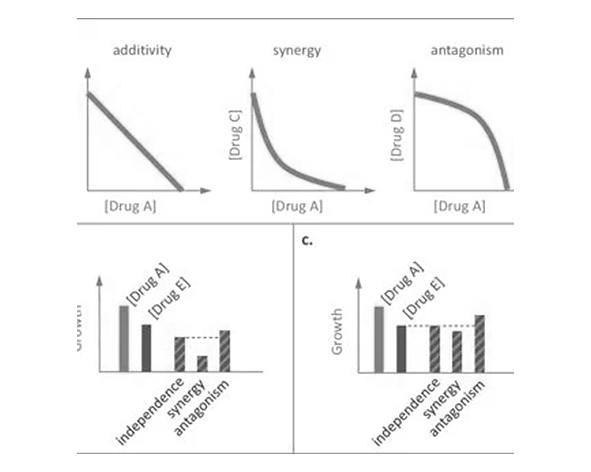
Desde una perspectiva mecanística, el efecto séquito no implica necesariamente una potenciación uniforme, sino una modulación compleja y dependiente del contexto, que puede incluir sinergias, antagonismos parciales o efectos aditivos. En este sentido, el fenómeno se integra dentro del marco del denominado endocannabinoidome, una red ampliada de señalización que incluye múltiples ligandos, receptores y enzimas interconectadas, reflejando la naturaleza sistémica de la regulación endocannabinoide (Di Marzo, 2018).
A pesar de su creciente popularidad en la literatura científica y divulgativa, el efecto séquito continúa siendo objeto de debate. La evidencia experimental disponible es heterogénea y depende en gran medida del modelo de estudio, la composición específica de los extractos y las condiciones farmacocinéticas. Por ello, su interpretación requiere un enfoque crítico, evitando simplificaciones y extrapolaciones no sustentadas por datos robustos (Russo, 2019; Bonn-Miller et al., 2018).
Historia del descubrimiento
El concepto de efecto séquito fue descrito por primera vez en 1998 en un estudio liderado por Shimon Ben-Shabat, en el que se investigaba la actividad de lípidos endógenos relacionados con el sistema endocannabinoide. En este trabajo, los autores observaron que ciertos ésteres de glicerol estructuralmente similares al 2-araquidonoilglicerol (2-AG), pero sin actividad significativa por sí mismos, eran capaces de potenciar la acción de este endocannabinoide al administrarse conjuntamente. Este fenómeno fue interpretado como una forma de modulación cooperativa entre mediadores lipídicos, dando origen al término “entourage effect” (Ben-Shabat et al., 1998).
En su contexto original, el efecto séquito no hacía referencia a la planta de Cannabis sativa ni a combinaciones de fitocannabinoides, sino a interacciones dentro del propio sistema endocannabinoide endógeno. Este matiz es fundamental, ya que el concepto surge en un entorno bioquímico específico donde múltiples lípidos comparten rutas metabólicas, enzimas y dianas moleculares, influyendo de manera conjunta en la señalización celular (Di Marzo, 2018).
Años más tarde, el término fue retomado y ampliado por Ethan B. Russo, quien propuso que un fenómeno similar podría ocurrir en el contexto del cannabis vegetal. En su revisión de 2011, Russo planteó que los fitocannabinoides y los terpenos presentes en la planta podrían interactuar entre sí generando efectos farmacológicos modulados, lo que contribuiría a explicar diferencias observadas entre extractos completos y compuestos aislados como el THC o el CBD. Esta reinterpretación marcó un punto de inflexión en la forma en que se entendía la complejidad farmacológica del cannabis (Russo, 2011).
Sin embargo, la extrapolación del efecto séquito desde el sistema endocannabinoide endógeno al fitocomplejo del cannabis no está exenta de limitaciones. Mientras que en el entorno endógeno las concentraciones, localización y metabolismo de los lípidos están altamente regulados, en los extractos vegetales la composición puede variar significativamente en función de factores como la genética de la planta, el método de extracción o la formulación final. Esta diferencia introduce una variabilidad considerable que dificulta la generalización del concepto en contextos aplicados (Bonn-Miller et al., 2018).
En las últimas décadas, el término “efecto séquito” ha ganado una notable popularidad tanto en la literatura científica como en el ámbito comercial del cannabis. No obstante, su uso se ha ampliado en ocasiones más allá de la evidencia experimental disponible, siendo frecuentemente empleado como argumento simplificado para justificar la superioridad de extractos complejos frente a compuestos aislados. Este uso extensivo ha contribuido a generar cierta ambigüedad conceptual, haciendo necesario un enfoque más riguroso y crítico en su definición y aplicación (Russo, 2019; Di Marzo, 2018).
Base molecular del efecto séquito
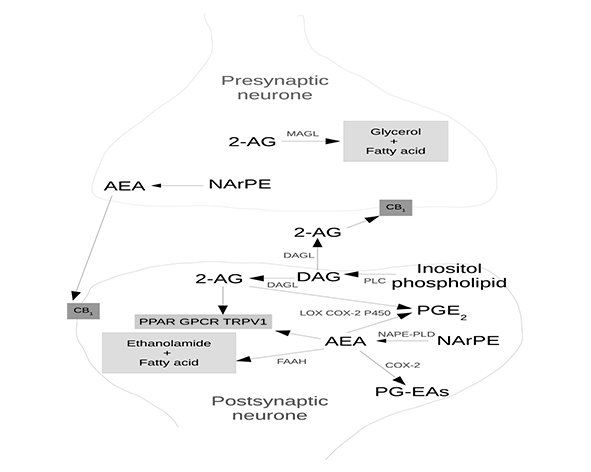
El denominado efecto séquito puede entenderse como un fenómeno emergente derivado de la interacción simultánea de múltiples compuestos bioactivos sobre distintas dianas moleculares dentro del organismo. En el contexto del sistema endocannabinoide y del endocannabinoidome, esta interacción no se limita a los receptores cannabinoides clásicos (CB1 y CB2), sino que involucra una red compleja de receptores, canales iónicos, enzimas y transportadores que responden de forma integrada a diferentes ligandos (Di Marzo, 2018).
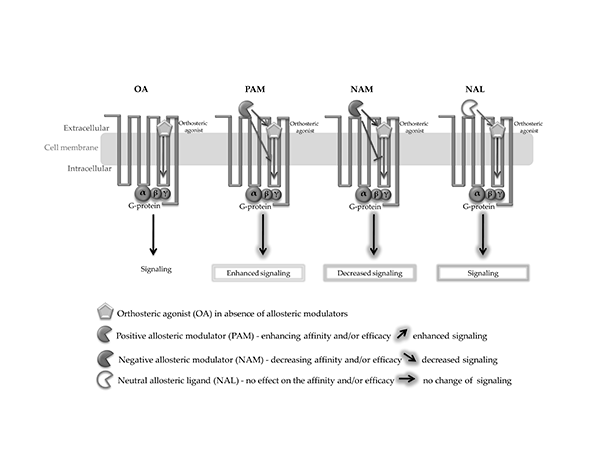
Uno de los mecanismos propuestos para explicar el efecto séquito es la modulación directa de receptores cannabinoides. Algunos fitocannabinoides pueden actuar como agonistas parciales, antagonistas o moduladores alostéricos de CB1 y CB2, alterando la afinidad o la eficacia de otros ligandos presentes en el mismo entorno. Por ejemplo, el cannabidiol (CBD) ha sido descrito como un modulador alostérico negativo del receptor CB1, lo que puede modificar la respuesta inducida por el Δ9-tetrahidrocannabinol (THC) en determinados contextos (Laprairie et al., 2015; Pertwee, 2008).
Además de la interacción directa con receptores cannabinoides, diversos compuestos presentes en el cannabis pueden actuar sobre dianas no cannabinoides, ampliando el espectro de efectos biológicos. Entre estas dianas se incluyen canales iónicos como TRPV1, receptores nucleares como PPARγ y otros sistemas de señalización intracelular. Esta diversidad de interacciones contribuye a generar respuestas fisiológicas complejas que no pueden atribuirse a un único mecanismo de acción (Russo, 2011; Di Marzo, 2018).
Otro nivel relevante es la modulación enzimática y metabólica. Algunos compuestos pueden influir en la actividad de enzimas responsables de la síntesis o degradación de endocannabinoides, como FAAH o MAGL, alterando así la disponibilidad de ligandos endógenos. Este tipo de interacción puede modificar indirectamente la señalización endocannabinoide, amplificando o atenuando respuestas fisiológicas sin necesidad de una activación directa de los receptores (Di Marzo, 2018).
En el ámbito farmacocinético, también se han propuesto mecanismos relacionados con la absorción, distribución y estabilidad de los compuestos. La presencia de ciertos terpenos o lípidos podría influir en la permeabilidad de membranas biológicas, la solubilidad de los cannabinoides o su metabolismo hepático, afectando así su biodisponibilidad. No obstante, la evidencia en este campo es aún limitada y en muchos casos procede de modelos experimentales preliminares (Russo, 2011; Bonn-Miller et al., 2018).
Desde una perspectiva integradora, el efecto séquito no debe interpretarse como una sinergia universal o predecible, sino como una red de interacciones dinámicas y contextuales, donde múltiples variables —incluyendo la concentración relativa de los compuestos, el tejido diana y el estado fisiológico del organismo— determinan el resultado final. Este enfoque sitúa el fenómeno dentro de la biología de sistemas, donde la respuesta emerge de la interacción global y no de la suma lineal de efectos individuales (Di Marzo, 2018).
Interpretación científica vs uso comercial del término
El concepto de efecto séquito ha sido ampliamente adoptado en el ámbito del cannabis, tanto en la literatura científica como en el discurso comercial. Sin embargo, existe una diferencia significativa entre su formulación original —basada en interacciones específicas dentro del sistema endocannabinoide— y su uso actual, que en muchos casos lo presenta como una propiedad generalizada y prácticamente garantizada de cualquier extracto complejo (Ben-Shabat et al., 1998; Russo, 2011).
Desde el punto de vista científico, el efecto séquito describe un conjunto de interacciones potenciales entre compuestos que pueden dar lugar a modulaciones farmacológicas dependientes del contexto. Estas interacciones no son universales ni necesariamente sinérgicas, y su resultado puede variar en función de múltiples factores, como la concentración relativa de los compuestos, la diana molecular implicada o el entorno fisiológico. En este sentido, la evidencia disponible no permite afirmar de forma general que los extractos complejos sean sistemáticamente superiores a los compuestos aislados en todos los escenarios (Bonn-Miller et al., 2018; Di Marzo, 2018).
En contraste, en el ámbito comercial el término “efecto séquito” se utiliza frecuentemente como argumento simplificado para justificar la supuesta superioridad de productos denominados full spectrum o de espectro completo. Esta interpretación tiende a presentar el fenómeno como una sinergia automática entre todos los compuestos presentes, sin considerar las limitaciones experimentales ni la variabilidad inherente a los extractos vegetales.
Desde una perspectiva más rigurosa, la relevancia de los extractos complejos no radica en una supuesta sinergia universal, sino en su composición multicomponente, que incluye una amplia gama de fitocannabinoides, terpenos, ceras y flavonoides. Esta diversidad química permite reproducir, en mayor medida, el perfil natural de la planta, incorporando múltiples compuestos que pueden interactuar con diferentes dianas biológicas o vías metabólicas. En este sentido, el interés científico reside en la posibilidad de que esta matriz compleja contribuya a generar respuestas biológicas más amplias o moduladas, sin que ello implique necesariamente un efecto superior en todos los casos (Russo, 2019; Di Marzo, 2018).
Cabe señalar que, en la práctica, no todos los productos etiquetados como full spectrum presentan una composición verdaderamente multicomponente al ser analizados. La variabilidad en los procesos de extracción, refinado y formulación puede dar lugar a perfiles químicos significativamente más simples de lo que su denominación sugiere, lo que refuerza la necesidad de evaluar estos productos desde una perspectiva analítica y no únicamente descriptiva.
Otro aspecto relevante es la falta de estandarización en la composición de los extractos comerciales. A diferencia de los sistemas biológicos endógenos, donde las concentraciones y proporciones de los mediadores están finamente reguladas, los productos derivados del cannabis pueden presentar perfiles químicos muy variables en función de la genética, el proceso de extracción y la formulación final. Esta variabilidad dificulta la reproducibilidad de los efectos y limita la extrapolación de resultados entre distintos productos (Bonn-Miller et al., 2018).
Asimismo, el uso indiscriminado del término puede generar expectativas poco realistas, al sugerir que la complejidad química por sí misma garantiza un efecto superior o más “equilibrado”. Desde una perspectiva científica, la complejidad no implica necesariamente eficacia, y en algunos casos puede introducir interacciones no deseadas o efectos difíciles de predecir. Por ello, la evaluación de estos sistemas requiere un enfoque basado en evidencia, evitando generalizaciones simplificadas (Di Marzo, 2018).
En este contexto, resulta fundamental diferenciar entre el efecto séquito como hipótesis científica —aún en desarrollo y sujeta a validación experimental— y su uso como concepto divulgativo o comercial. Esta distinción permite mantener un discurso riguroso y alineado con la evidencia disponible, evitando tanto la negación del fenómeno como su sobredimensión. En última instancia, el valor del concepto reside en su capacidad para abrir nuevas líneas de investigación, no en su utilización como argumento absoluto (Russo, 2019).
Importancia en investigación científica
El concepto de efecto séquito ha adquirido relevancia en la investigación contemporánea como marco teórico para explorar interacciones complejas entre compuestos bioactivos dentro del sistema endocannabinoide y del denominado endocannabinoidome. Su principal aportación reside en cuestionar el modelo farmacológico clásico centrado en compuestos aislados, promoviendo enfoques más integradores basados en redes de señalización y múltiples dianas moleculares (Di Marzo, 2018).
En el ámbito de la farmacología, el efecto séquito ha impulsado el interés por el estudio de combinaciones de compuestos en lugar de moléculas individuales. Este enfoque ha llevado al desarrollo de modelos experimentales que evalúan interacciones entre fitocannabinoides, terpenos y otros metabolitos, con el objetivo de identificar posibles efectos sinérgicos o moduladores. No obstante, estos estudios requieren diseños rigurosos y condiciones controladas, ya que la variabilidad en las proporciones y concentraciones puede influir de forma significativa en los resultados (Russo, 2011; Bonn-Miller et al., 2018).
Asimismo, el concepto ha contribuido al avance de la biología de sistemas aplicada al sistema endocannabinoide, favoreciendo una comprensión más amplia de cómo diferentes mediadores lipídicos, receptores y enzimas interactúan en conjunto para regular procesos fisiológicos. Esta perspectiva resulta especialmente relevante en contextos donde múltiples vías de señalización convergen, y donde las respuestas biológicas no pueden explicarse mediante mecanismos lineales simples (Di Marzo, 2018).
Desde el punto de vista translacional, el efecto séquito ha estimulado el desarrollo de formulaciones complejas y extractos estandarizados, aunque su validación clínica sigue siendo limitada. La investigación en este campo se enfrenta al reto de demostrar de manera consistente que determinadas combinaciones ofrecen ventajas frente a compuestos aislados, lo que implica la necesidad de ensayos clínicos bien diseñados y comparativos. Hasta la fecha, la evidencia disponible es aún insuficiente para establecer conclusiones generalizables en humanos (Bonn-Miller et al., 2018; Russo, 2019).
Además, el estudio del efecto séquito ha puesto de relieve la importancia de factores como la farmacocinética, la biodisponibilidad y la interacción entre compuestos, aspectos que pueden modificar significativamente la respuesta biológica. Este enfoque ha ampliado el interés hacia la influencia de los excipientes, los sistemas de administración y la matriz lipídica en la que se presentan los cannabinoides, integrando variables que tradicionalmente recibían menor atención en estudios centrados en moléculas puras (Di Marzo, 2018).
En conjunto, el efecto séquito representa una herramienta conceptual útil para guiar nuevas líneas de investigación en farmacología y biomedicina, siempre que se interprete dentro de sus límites y con base en evidencia experimental sólida. Su valor no reside en ofrecer respuestas definitivas, sino en plantear preguntas relevantes sobre la complejidad de las interacciones biológicas y la necesidad de enfoques más integradores en el estudio de sistemas fisiológicos complejos (Russo, 2019).
Referencias
- Ben-Shabat, S., Fride, E., Sheskin, T., Tamiri, T., Rhee, M. H., Vogel, Z., Bisogno, T., De Petrocellis, L., Di Marzo, V., & Mechoulam, R. (1998). An entourage effect: inactive endogenous fatty acid glycerol esters enhance 2-arachidonoyl-glycerol cannabinoid activity. European Journal of Pharmacology, 353(1), 23–31. - Russo, E. B. (2011). Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. British Journal of Pharmacology, 163(7), 1344–1364. - Russo, E. B. (2019). The case for the entourage effect and conventional breeding of clinical cannabis: no “strain,” no gain. Frontiers in Plant Science, 9, 1969. - Di Marzo, V. (2018). New approaches and challenges to targeting the endocannabinoid system. Nature Reviews Drug Discovery, 17(9), 623–639. - Pertwee, R. G. (2008). The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids: Δ9-tetrahydrocannabinol, cannabidiol and Δ9-tetrahydrocannabivarin. British Journal of Pharmacology, 153(2), 199–215. - Laprairie, R. B., Bagher, A. M., Kelly, M. E. M., & Denovan-Wright, E. M. (2015). Cannabidiol is a negative allosteric modulator of the cannabinoid CB1 receptor. British Journal of Pharmacology, 172(20), 4790–4805. - Bonn-Miller, M. O., Loflin, M. J. E., Thomas, B. F., Marcu, J. P., Hyke, T., & Vandrey, R. (2018). Labeling accuracy of cannabidiol extracts sold online. JAMA, 318(17), 1708–1709. - McPartland, J. M., Duncan, M., Di Marzo, V., & Pertwee, R. G. (2015). Are cannabidiol and Δ9-tetrahydrocannabivarin negative modulators of the endocannabinoid system? A systematic review. British Journal of Pharmacology, 172(3), 737–753. - Morales, P., Hurst, D. P., & Reggio, P. H. (2017). Molecular targets of the phytocannabinoids: a complex picture. Progress in the Chemistry of Organic Natural Products, 103, 103–131. Pamplona, F. A., da Silva, L. R., & Coan, A. C. (2018). Potential clinical benefits of CBD-rich cannabis extracts over purified CBD in treatment-resistant epilepsy: observational data meta-analysis. Frontiers in Neurology, 9, 759.