Introducción
El dolor constituye una experiencia multidimensional que integra componentes sensoriales, emocionales y cognitivos, resultado de la interacción entre señales periféricas de daño potencial o real y procesos de modulación central. Desde el punto de vista fisiológico, la nocicepción implica la detección de estímulos nocivos mediante nociceptores periféricos, su transmisión a través de fibras aferentes hacia la médula espinal y su posterior procesamiento en centros superiores del sistema nervioso central, incluyendo tálamo, corteza somatosensorial y estructuras límbicas. Sin embargo, esta señal no es lineal ni estática, sino que está sujeta a mecanismos de amplificación o inhibición que determinan la experiencia final del dolor. (Fields, 2018)
En este contexto, el sistema endocannabinoide (SEC) emerge como un modulador clave de la nocicepción, actuando en múltiples niveles del eje periférico-central. Su función principal no es generar la señal de dolor, sino regular su intensidad, duración y cualidad mediante la modulación de la excitabilidad neuronal y la liberación de neurotransmisores. Este sistema actúa como un regulador homeostático que responde a cambios en el entorno fisiológico, activándose en situaciones de estrés, inflamación o daño tisular para limitar la hiperexcitabilidad neuronal y restaurar el equilibrio funcional. (Di Marzo, 2018)
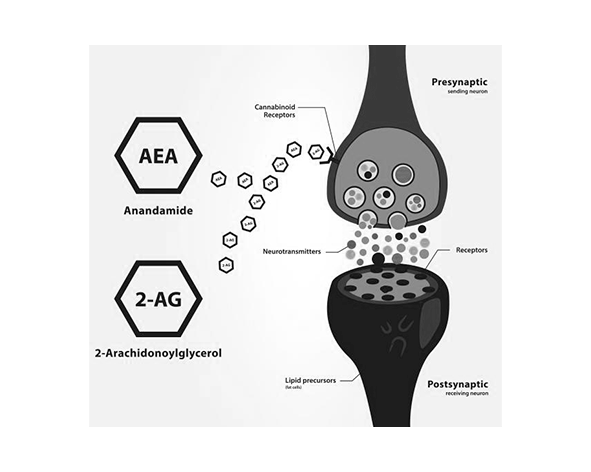
El SEC está compuesto por receptores cannabinoides, principalmente CB1 y CB2, ligandos endógenos como la anandamida (AEA) y el 2-araquidonoilglicerol (2-AG), y enzimas responsables de su síntesis y degradación, como FAAH y MAGL. En el contexto del dolor, estos componentes interactúan de forma coordinada para modular tanto la transmisión ascendente de la señal nociceptiva como los sistemas descendentes de control del dolor, que incluyen circuitos inhibitorios desde el tronco encefálico hacia la médula espinal. (Lu & Mackie, 2016; Zou & Kumar, 2018)
Además, el SEC no actúa de manera aislada, sino que se integra en una red más amplia de sistemas de señalización, incluyendo receptores TRP, sistemas opioides endógenos, serotonina y noradrenalina. Esta interacción sugiere que la modulación del dolor por el SEC es un proceso complejo y distribuido, que afecta tanto a la percepción sensorial como a los componentes afectivos del dolor. (Finn et al., 2021)
Desde una perspectiva fisiológica, el estudio del SEC en el dolor permite entender cómo el organismo regula la respuesta frente a estímulos nocivos y cómo se desarrollan estados de dolor crónico cuando estos mecanismos de regulación fallan o se desajustan. En este sentido, el SEC se considera un elemento central en la transición entre dolor agudo adaptativo y dolor crónico maladaptativo, caracterizado por sensibilización periférica y central. (Ossipov et al., 2010)
Historia
El interés por la relación entre el sistema endocannabinoide y el dolor tiene raíces que preceden al descubrimiento formal del propio sistema. Diversas culturas documentaron el uso de preparaciones de Cannabis sativa en contextos relacionados con el alivio del dolor, aunque durante siglos estos usos se mantuvieron en el ámbito empírico, sin una comprensión mecanística de sus efectos. No fue hasta finales del siglo XX cuando el avance en neurociencia permitió identificar las bases biológicas de esta interacción. (Pertwee, 2006)
El punto de inflexión se produjo en la década de 1990 con la identificación del receptor CB1 en el sistema nervioso central, seguido poco después por el descubrimiento del receptor CB2, inicialmente asociado al sistema inmunológico. Estos hallazgos, junto con la caracterización de los primeros endocannabinoides —anandamida (AEA) en 1992 y 2-AG en 1995—, establecieron las bases del sistema endocannabinoide como un sistema de señalización endógeno implicado en múltiples funciones fisiológicas, incluida la modulación del dolor. (Devane et al., 1992; Mechoulam et al., 1995)
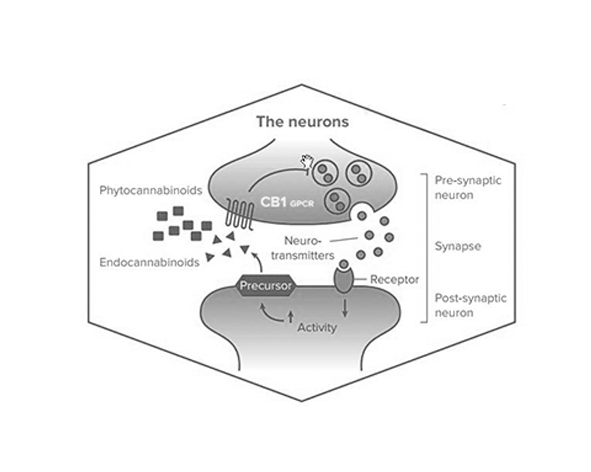
Durante los primeros años de investigación, el foco se centró en los efectos de la activación de CB1 en el sistema nervioso central. Estudios en modelos animales mostraron que la activación de estos receptores podía reducir la liberación de neurotransmisores excitatorios como el glutamato en sinapsis clave del procesamiento nociceptivo, lo que se traducía en una disminución de la transmisión del dolor. Este mecanismo se relacionó con la localización de CB1 en neuronas presinápticas en regiones como la médula espinal dorsal, el tálamo y la corteza. (Iversen, 2003)
Posteriormente, la atención se amplió hacia el papel de CB2, especialmente en contextos de inflamación y dolor persistente. A diferencia de CB1, cuya expresión es predominante en el sistema nervioso central, CB2 se identificó principalmente en células del sistema inmunológico, como macrófagos y microglía. Su activación se asoció con la modulación de la liberación de citocinas y mediadores inflamatorios, sugiriendo un papel indirecto en la regulación del dolor a través del control de procesos inflamatorios. (Guindon & Hohmann, 2009)
A medida que avanzó la investigación, se hizo evidente que el SEC no opera como un sistema aislado, sino como parte de una red compleja de señalización. Se identificaron interacciones funcionales con sistemas como el opioide endógeno, lo que abrió nuevas líneas de investigación sobre mecanismos sinérgicos en la modulación del dolor. Asimismo, la implicación de canales iónicos como TRPV1 en la señalización de la anandamida añadió una capa adicional de complejidad al sistema. (Zygmunt et al., 1999; Finn et al., 2021)
En las últimas décadas, el estudio del SEC en el contexto del dolor ha evolucionado desde una visión centrada en receptores individuales hacia un enfoque sistémico que considera la dinámica de síntesis y degradación de endocannabinoides, la distribución tisular de sus componentes y su papel en distintos tipos de dolor, incluyendo dolor neuropático, inflamatorio y nociplástico. Este cambio de paradigma ha permitido entender el SEC como un sistema modulador clave en la fisiología del dolor, con implicaciones relevantes en investigación biomédica. (Di Marzo, 2018)
Organización y distribución del SEC
El sistema endocannabinoide (SEC) presenta una distribución amplia y estratégicamente localizada en estructuras clave implicadas en la detección, transmisión y modulación del dolor. Esta organización no es uniforme, sino que refleja la necesidad de regular la señal nociceptiva en múltiples niveles, desde los tejidos periféricos hasta los circuitos centrales que integran la experiencia del dolor. (Lu & Mackie, 2016)
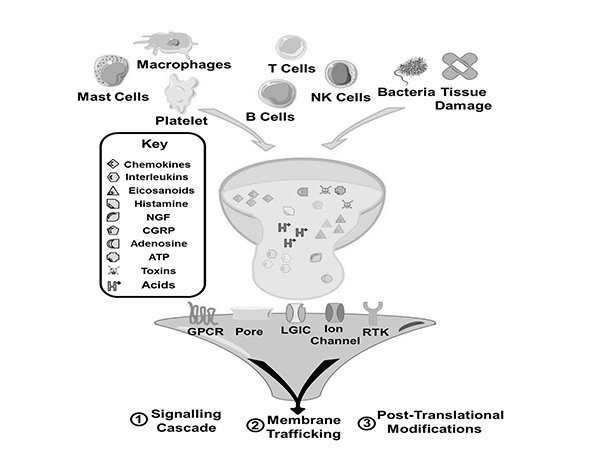
En el sistema nervioso periférico, los receptores cannabinoides se expresan en terminaciones nerviosas de nociceptores primarios, particularmente en fibras C y Aδ responsables de la detección de estímulos nocivos térmicos, mecánicos y químicos. La presencia de CB1 en estas terminaciones permite una modulación directa de la excitabilidad neuronal, reduciendo la generación de potenciales de acción ante estímulos nocivos. Además, en condiciones de inflamación o daño tisular, se ha observado un aumento en la expresión de CB2 en células inmunes infiltradas, como macrófagos y mastocitos, lo que sugiere un papel adaptativo del SEC en el control del dolor periférico asociado a procesos inflamatorios. (Guindon & Hohmann, 2009)
A nivel de la médula espinal, el SEC desempeña un papel crítico en la modulación de la transmisión nociceptiva en el asta dorsal, donde las neuronas de segundo orden reciben la información proveniente de los nociceptores periféricos. Los receptores CB1 se localizan predominantemente en terminales presinápticas de neuronas aferentes primarias y en interneuronas, regulando la liberación de neurotransmisores excitatorios como glutamato y sustancia P. Esta modulación presináptica contribuye a reducir la señal ascendente hacia estructuras superiores. (Zou & Kumar, 2018)
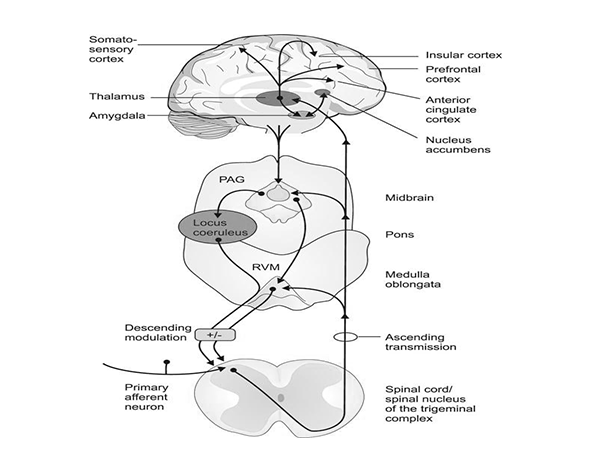
En el sistema nervioso central, la distribución de CB1 es particularmente densa en regiones implicadas en el procesamiento y la modulación del dolor, incluyendo el tálamo, la corteza somatosensorial, la amígdala, el hipocampo y el periacueducto gris (PAG). Estas estructuras no solo participan en la discriminación sensorial del dolor, sino también en sus componentes emocionales y cognitivos. La activación del SEC en estas áreas puede influir tanto en la intensidad percibida del dolor como en su carga afectiva. (Herkenham et al., 1991; Fields, 2018)
El sistema descendente de modulación del dolor, que incluye estructuras como el periacueducto gris, el núcleo del rafe y el locus coeruleus, también está fuertemente influenciado por el SEC. En estos circuitos, la activación de CB1 puede facilitar mecanismos inhibitorios descendentes que reducen la transmisión nociceptiva en la médula espinal, actuando como un sistema de control “top-down” que modula la experiencia del dolor en función del contexto. (Ossipov et al., 2010)
En cuanto a los endocannabinoides, su síntesis y liberación se produce de forma “on demand”, es decir, en respuesta a cambios en la actividad neuronal o en el estado fisiológico. A diferencia de los neurotransmisores clásicos, no se almacenan en vesículas, sino que se generan a partir de lípidos de membrana y actúan localmente antes de ser rápidamente degradados por enzimas como FAAH (para AEA) y MAGL (para 2-AG). Esta característica permite una regulación fina y temporalmente precisa de la señalización endocannabinoide. (Di Marzo, 2018)
Además, el SEC interactúa con otras dianas moleculares relevantes en la fisiología del dolor, como los canales TRPV1, implicados en la detección de estímulos térmicos y químicos. La anandamida, por ejemplo, puede actuar tanto sobre receptores CB1 como sobre TRPV1, lo que introduce una dualidad funcional en su efecto sobre la nocicepción dependiendo del contexto y la concentración local. (Zygmunt et al., 1999)
En conjunto, la organización del SEC en el sistema del dolor refleja un sistema distribuido y altamente integrado, capaz de modular la señal nociceptiva en múltiples niveles y de adaptarse a diferentes estados fisiológicos y patológicos. Esta distribución explica su implicación tanto en la regulación del dolor agudo como en procesos de sensibilización asociados al dolor crónico. (Finn et al., 2021)
Mecanismos
La modulación del dolor por el sistema endocannabinoide (SEC) se basa en una serie de mecanismos celulares y moleculares que actúan de forma coordinada para regular la transmisión nociceptiva. Estos mecanismos no operan en un único punto del sistema, sino que se distribuyen a lo largo de todo el eje periférico-central, afectando tanto a la generación de la señal de dolor como a su propagación y procesamiento. (Lu & Mackie, 2016)
Uno de los mecanismos fundamentales del SEC es la modulación presináptica de la liberación de neurotransmisores. Los receptores CB1, localizados principalmente en terminales presinápticas, están acoplados a proteínas G (Gi/o), cuya activación inhibe la adenilato ciclasa, reduce los niveles de AMPc y modula la actividad de canales iónicos. En concreto, la activación de CB1 disminuye la entrada de calcio a través de canales tipo N y P/Q y aumenta la salida de potasio, lo que reduce la probabilidad de liberación de neurotransmisores excitatorios como glutamato. Este efecto contribuye a disminuir la transmisión de la señal nociceptiva en sinapsis clave, especialmente en la médula espinal y en circuitos centrales. (Zou & Kumar, 2018)
Un segundo mecanismo clave es la señalización retrógrada de los endocannabinoides. A diferencia de los neurotransmisores clásicos, los endocannabinoides como la anandamida (AEA) y el 2-AG se sintetizan en la neurona postsináptica en respuesta a un aumento de la actividad neuronal o a la elevación de calcio intracelular. Una vez liberados, difunden hacia la neurona presináptica y activan receptores CB1, inhibiendo la liberación de neurotransmisores. Este mecanismo permite una regulación local y dinámica de la actividad sináptica, actuando como un sistema de “feedback negativo” que limita la hiperexcitabilidad neuronal asociada al dolor. (Ohno-Shosaku et al., 2001; Kano et al., 2009)
En el contexto del dolor periférico, el SEC también modula la actividad de nociceptores directamente. La activación de CB1 en terminaciones nerviosas periféricas puede reducir la excitabilidad de estas neuronas, mientras que la activación de CB2 en células inmunes regula la liberación de mediadores inflamatorios como prostaglandinas, citocinas y quimiocinas. Este control de la respuesta inflamatoria contribuye a disminuir la sensibilización periférica, un proceso clave en el desarrollo del dolor persistente. (Guindon & Hohmann, 2009)
Además, el SEC interactúa con canales iónicos implicados en la transducción del dolor, especialmente los pertenecientes a la familia TRP (Transient Receptor Potential). La anandamida, por ejemplo, puede activar el canal TRPV1, conocido por su papel en la detección de estímulos térmicos y químicos nocivos. Esta interacción introduce una complejidad funcional, ya que dependiendo del contexto fisiológico, la activación de TRPV1 puede contribuir tanto a la facilitación como a la modulación del dolor. (Zygmunt et al., 1999)
Otro mecanismo relevante es la interacción del SEC con los sistemas descendentes de control del dolor. En estructuras como el periacueducto gris (PAG) y el bulbo rostral ventromedial, la activación de CB1 puede influir en la liberación de neurotransmisores como serotonina y noradrenalina, facilitando la activación de vías inhibitorias descendentes que reducen la transmisión nociceptiva en la médula espinal. Este mecanismo es fundamental para entender cómo el cerebro puede modular activamente la percepción del dolor en función del contexto emocional o cognitivo. (Ossipov et al., 2010)
Asimismo, existe una interacción funcional entre el SEC y el sistema opioide endógeno. Estudios han demostrado que ambos sistemas pueden actuar de forma sinérgica en la modulación del dolor, compartiendo vías de señalización y localización anatómica en regiones clave. Esta relación sugiere que el SEC forma parte de una red más amplia de sistemas moduladores del dolor, en la que múltiples mecanismos convergen para regular la experiencia nociceptiva. (Finn et al., 2021)
En conjunto, los mecanismos del SEC en el dolor reflejan un sistema altamente adaptable, capaz de responder a cambios en la actividad neuronal y en el estado fisiológico del organismo. Esta capacidad de modulación dinámica es esencial para mantener el equilibrio entre la detección de estímulos nocivos y la prevención de respuestas excesivas que puedan derivar en dolor crónico. (Di Marzo, 2018)
Funciones fisiológicas
El sistema endocannabinoide (SEC) desempeña funciones fisiológicas clave en la regulación del dolor, actuando como un sistema modulador que ajusta la intensidad, duración y cualidad de la experiencia nociceptiva. Su papel no es eliminar la señal de dolor —que cumple una función protectora esencial—, sino mantenerla dentro de un rango funcional que permita la respuesta adaptativa sin generar una activación excesiva o persistente. (Fields, 2018)
Una de las funciones principales del SEC es la limitación de la sensibilización periférica. Tras un daño tisular o un proceso inflamatorio, los nociceptores pueden volverse más sensibles a estímulos, reduciendo su umbral de activación. El SEC interviene en este contexto modulando la excitabilidad de estas neuronas y regulando la liberación de mediadores inflamatorios por parte de células inmunes. Este mecanismo contribuye a evitar que la señal nociceptiva se amplifique de forma desproporcionada. (Guindon & Hohmann, 2009)
A nivel central, el SEC participa en la regulación de la sensibilización central, un proceso en el que las neuronas del sistema nervioso central muestran una respuesta aumentada ante estímulos nociceptivos o incluso no nociceptivos. A través de la modulación de la liberación de neurotransmisores excitatorios e inhibitorios en la médula espinal y en regiones cerebrales superiores, el SEC contribuye a mantener el equilibrio entre excitación e inhibición sináptica, evitando la hiperexcitabilidad neuronal característica del dolor crónico. (Zou & Kumar, 2018)
Otra función relevante del SEC es la integración de los componentes emocionales y cognitivos del dolor. Estructuras como la amígdala, el hipocampo y la corteza prefrontal, que participan en la evaluación emocional y contextual del dolor, presentan una alta densidad de receptores CB1. La actividad del SEC en estas regiones puede influir en cómo se percibe y se interpreta el dolor, modulando aspectos como la aversividad, la memoria asociada al dolor y la respuesta al estrés. (Finn et al., 2021)
El SEC también forma parte de los sistemas descendentes de control del dolor, facilitando la activación de vías inhibitorias que proyectan desde el cerebro hacia la médula espinal. Este control “top-down” permite ajustar la percepción del dolor en función del contexto, por ejemplo, reduciendo su intensidad en situaciones de alta demanda adaptativa. La participación del SEC en estos circuitos refuerza su papel como regulador dinámico de la experiencia nociceptiva. (Ossipov et al., 2010)
Además, el SEC contribuye a la resolución de procesos inflamatorios, lo que tiene implicaciones indirectas en la modulación del dolor. La activación de receptores CB2 en células inmunes regula la liberación de citocinas y otros mediadores, favoreciendo un entorno menos proinflamatorio. Esta función es especialmente relevante en el contexto del dolor inflamatorio, donde la interacción entre sistema inmune y sistema nervioso es clave. (Di Marzo, 2018)
En conjunto, las funciones fisiológicas del SEC en el dolor reflejan su papel como sistema de regulación homeostática, capaz de actuar en múltiples niveles para mantener el equilibrio entre la detección de estímulos nocivos y la prevención de respuestas excesivas o persistentes. Este equilibrio es fundamental para evitar la transición hacia estados de dolor crónico, en los que los mecanismos de control se encuentran alterados o desregulados. (Fields, 2018)
Implicaciones
La implicación del sistema endocannabinoide (SEC) en la fisiología del dolor trasciende su papel como modulador puntual de la nocicepción, situándolo como un componente central en la regulación del equilibrio entre dolor adaptativo y dolor maladaptativo. Desde una perspectiva fisiológica, el SEC actúa como un sistema de control que limita la amplificación excesiva de la señal nociceptiva, pero cuando este sistema se desregula, pueden aparecer estados persistentes de dolor caracterizados por sensibilización periférica y central. (Ossipov et al., 2010)
Uno de los aspectos más relevantes es su papel en la transición del dolor agudo al dolor crónico. En condiciones normales, el SEC contribuye a resolver la respuesta al daño tisular mediante la modulación de la inflamación y la excitabilidad neuronal. Sin embargo, alteraciones en la señalización endocannabinoide —ya sea por cambios en la expresión de receptores, en la síntesis de endocannabinoides o en su degradación— pueden favorecer la persistencia de la señal nociceptiva más allá de su función protectora inicial. Este fenómeno se ha observado en distintos modelos de dolor neuropático e inflamatorio. (Di Marzo, 2018)
Asimismo, el SEC se encuentra estrechamente vinculado con la interacción entre sistema nervioso e inmune, lo que tiene implicaciones en procesos donde el dolor está asociado a inflamación crónica. La activación de receptores CB2 en células inmunes modula la liberación de citocinas y otros mediadores, influyendo en el microentorno inflamatorio que rodea a las terminaciones nerviosas. Esta interacción sugiere que el SEC participa no solo en la transmisión del dolor, sino también en los procesos que lo perpetúan. (Guindon & Hohmann, 2009)
Otra implicación importante es su papel en la dimensión afectiva del dolor. El SEC, a través de su acción en estructuras como la amígdala y la corteza prefrontal, influye en la evaluación emocional del dolor, en la memoria asociada a experiencias dolorosas y en la respuesta al estrés. Esto conecta el dolor con estados emocionales como ansiedad o estrés, que a su vez pueden retroalimentar la percepción nociceptiva. Este componente es especialmente relevante en condiciones de dolor crónico, donde la experiencia del dolor no puede explicarse únicamente por factores periféricos. (Finn et al., 2021)
Además, la interacción del SEC con otros sistemas moduladores, como el sistema opioide endógeno, sugiere la existencia de redes de regulación convergentes. Estas interacciones permiten una modulación más compleja y adaptable del dolor, pero también implican que alteraciones en uno de estos sistemas pueden afectar al equilibrio global. Este enfoque sistémico ha llevado a considerar el SEC como parte de una red integradora que regula múltiples aspectos de la homeostasis. (Zou & Kumar, 2018)
Desde una perspectiva de investigación, el SEC se ha convertido en una diana de interés para comprender mejor los mecanismos del dolor y su regulación. El estudio de enzimas como FAAH y MAGL, responsables de la degradación de endocannabinoides, ha permitido explorar cómo la modulación de la disponibilidad de estos ligandos afecta a la señalización nociceptiva. Asimismo, la variabilidad individual en componentes del SEC podría explicar diferencias en la percepción del dolor entre individuos. (Lu & Mackie, 2016)
En conjunto, las implicaciones del SEC en el dolor reflejan su papel como sistema regulador central en la fisiología nociceptiva. Su capacidad para integrar señales neuronales, inmunes y emocionales lo sitúa como un elemento clave en la comprensión de cómo el organismo gestiona el dolor en condiciones normales y patológicas, así como en la transición hacia estados de disfunción persistente. (Di Marzo, 2018)
Véase también
- Sistema endocannabinoide (SEC)
- Señalización endocannabinoide
- Anandamida (AEA)
- 2-araquidonoilglicerol (2-AG)
- Receptor CB1
Referencias
- Di Marzo, V. (2018). New approaches and challenges to targeting the endocannabinoid system. Nature Reviews Drug Discovery. - Fields, H. L. (2018). Pain: An unpleasant topic. Pain. - Finn, D. P., Haroutounian, S., Hohmann, A. G., Krane, E., Soliman, N., Rice, A. S. C. (2021). Cannabinoids, the endocannabinoid system, and pain: A review of preclinical studies. Pain. - Guindon, J., Hohmann, A. G. (2009). The endocannabinoid system and pain. CNS & Neurological Disorders - Drug Targets. - Herkenham, M. et al. (1991). Cannabinoid receptor localization in brain. Proceedings of the National Academy of Sciences. - Iversen, L. (2003). Cannabis and the brain. Brain. - Kano, M., Ohno-Shosaku, T., Hashimotodani, Y., Uchigashima, M., Watanabe, M. (2009). Endocannabinoid-mediated control of synaptic transmission. Physiological Reviews. - Lu, H. C., Mackie, K. (2016). An introduction to the endogenous cannabinoid system. Biological Psychiatry. - Mechoulam, R., Ben-Shabat, S., Hanus, L. et al. (1995). Identification of an endogenous 2-monoglyceride, present in canine gut, that binds to cannabinoid receptors. Biochemical Pharmacology. - Ossipov, M. H., Dussor, G. O., Porreca, F. (2010). Central modulation of pain. Journal of Clinical Investigation. - Pertwee, R. G. (2006). Cannabinoid pharmacology: the first 66 years. British Journal of Pharmacology. - Zygmunt, P. M. et al. (1999). Vanilloid receptors on sensory nerves mediate the vasodilator action of anandamide. Nature. - Zou, S., Kumar, U. (2018). Cannabinoid receptors and the endocannabinoid system: signaling and function in the central nervous system. International Journal of Molecular Sciences.
{
«@context»: «https://schema.org»,
«@type»: «ScholarlyArticle»,
«headline»: «Dolor y sistema endocannabinoide»,
«name»: «Dolor y sistema endocannabinoide»,
«description»: «Revisión fisiológica del papel del sistema endocannabinoide en la modulación del dolor, incluyendo mecanismos, distribución y funciones en la nocicepción.»,
«image»: «https://tantrumcbd.es/wp-content/uploads/2026/04/Fig1-25.png»,
«inLanguage»: «es»,
«datePublished»: «2026-04-20»,
«dateModified»: «2026-04-20»,
«author»: {
«@type»: «Person»,
«name»: «Mario Gonzalez»
},
«publisher»: {
«@type»: «Organization»,
«name»: «Tantrum Knowledge»
},
«isPartOf»: {
«@type»: «CreativeWorkSeries»,
«name»: «Tantrum Knowledge»
},
«about»: [
«Sistema endocannabinoide»,
«Dolor»,
«Nocicepción»,
«CB1»,
«CB2»,
«Endocannabinoides»
],
«citation»: [
«Di Marzo V. (2018)»,
«Fields HL. (2018)»,
«Finn DP et al. (2021)»,
«Guindon J., Hohmann AG. (2009)»,
«Lu HC., Mackie K. (2016)»
]
}