Introducción
El cannabigerol (CBG) es un fitocannabinoide no psicotrópico presente en Cannabis sativa L. que ocupa una posición central en la biosíntesis de los principales cannabinoides de la planta. Aunque su concentración en la planta madura suele ser baja en comparación con compuestos como el cannabidiol (CBD) o el Δ9-tetrahidrocannabinol (THC), su relevancia bioquímica es desproporcionadamente alta debido a su papel como precursor directo de múltiples metabolitos cannabinoides (Taura et al., 2007; Gülck & Møller, 2020).
Desde una perspectiva biosintética, el CBG deriva de la descarboxilación del ácido cannabigerólico (CBGA), considerado el punto de partida de la ruta metabólica cannabinoide. El CBGA se forma a partir de la condensación del geranil difosfato (GPP) y el ácido olivetólico, catalizada por una preniltransferasa específica. A partir de este intermediario clave, diferentes sintasas —como la THCA sintasa, la CBDA sintasa y la CBCA sintasa— transforman el CBGA en los ácidos precursores de los cannabinoides más abundantes, lo que sitúa al CBG en una posición jerárquica dentro del metabolismo secundario del cannabis (Fellermeier & Zenk, 1998; Taura et al., 2007).
Esta función como intermediario metabólico explica por qué el contenido de CBG en la planta suele ser bajo en estadios avanzados de maduración: a medida que progresa el desarrollo floral, el CBGA es progresivamente convertido en otros cannabinoides, reduciendo la fracción de CBG libre disponible. Sin embargo, determinadas variedades seleccionadas o manipulaciones agronómicas pueden aumentar su contenido, lo que ha despertado interés tanto desde el punto de vista botánico como industrial (García et al., 2021).
En el ámbito farmacológico, el CBG presenta un perfil de interacción complejo y no restringido a los receptores cannabinoides clásicos. Aunque muestra afinidad moderada por los receptores CB1 y CB2, también interactúa con múltiples dianas moleculares, incluyendo canales TRP (como TRPV1 y TRPA1), receptores serotoninérgicos (5-HT1A), receptores adrenérgicos α2 y otros sistemas implicados en la modulación neuroquímica y celular. Esta diversidad funcional lo integra dentro del denominado “endocannabinoidome”, una red ampliada de señalización lipídica que trasciende el sistema endocannabinoide clásico (Pertwee, 2008; Cascio et al., 2010; Di Marzo, 2018).
Además de su interacción molecular, el CBG ha sido objeto de creciente interés en investigación preclínica debido a su posible implicación en procesos fisiológicos relacionados con la regulación neuronal, la señalización inflamatoria, la homeostasis metabólica y la función gastrointestinal. No obstante, la mayor parte de la evidencia disponible procede de modelos experimentales in vitro o animales, por lo que su interpretación en contextos humanos requiere cautela y un análisis crítico de la literatura (Borrelli et al., 2013; Rock et al., 2012).
En conjunto, el cannabigerol representa un elemento clave tanto en la biología del cannabis como en la investigación del sistema endocannabinoide y sus extensiones funcionales. Su papel como precursor biosintético, su perfil farmacológico diverso y su creciente presencia en estudios científicos lo convierten en una molécula de interés dentro del estudio de los fitocannabinoides, especialmente en el contexto de aproximaciones no centradas exclusivamente en el CBD o el THC.
Historia del descubrimiento
El cannabigerol (CBG) fue identificado por primera vez en la década de 1960, en el contexto de los primeros estudios sistemáticos sobre la composición química de Cannabis sativa. Durante este periodo, el desarrollo de técnicas analíticas como la cromatografía permitió aislar y caracterizar diversos fitocannabinoides, sentando las bases de la química del cannabis moderna (Gaoni & Mechoulam, 1964).
Aunque los primeros trabajos se centraron principalmente en el Δ9-tetrahidrocannabinol (THC) debido a su actividad psicotrópica, investigaciones posteriores comenzaron a identificar otros compuestos estructuralmente relacionados. Entre ellos, el CBG emergió como una molécula de interés no tanto por su abundancia, sino por su posición dentro de la ruta biosintética del cannabis. Fue en décadas posteriores, especialmente a partir de los años 80 y 90, cuando se empezó a comprender que el ácido cannabigerólico (CBGA) actuaba como precursor común de los principales cannabinoides, redefiniendo el papel del CBG dentro de la planta (Shoyama et al., 1975; Fellermeier & Zenk, 1998).
Este cambio de perspectiva marcó un punto de inflexión en la investigación, desplazando el enfoque desde el estudio aislado de compuestos individuales hacia una comprensión más integrada del metabolismo cannabinoide. En este contexto, el CBG dejó de considerarse un cannabinoide menor para ser reconocido como una molécula clave en la arquitectura biosintética del cannabis.
En las últimas décadas, el interés por el CBG ha aumentado de forma progresiva, impulsado tanto por avances en biotecnología vegetal como por la selección genética de variedades ricas en este compuesto. Paralelamente, el desarrollo del concepto de sistema endocannabinoide en los años 90, tras el descubrimiento de receptores como CB1 y CB2, abrió nuevas líneas de investigación que posteriormente se expandieron hacia el estudio de fitocannabinoides menos abundantes como el CBG (Matsuda et al., 1990; Munro et al., 1993).
Más recientemente, el surgimiento del concepto de “endocannabinoidome” ha ampliado aún más el marco teórico en el que se estudia el CBG, integrándolo en una red compleja de señalización que incluye múltiples receptores, enzimas y lípidos bioactivos. Este enfoque ha contribuido a revalorizar su estudio, no solo desde la química del cannabis, sino también desde la biología molecular y la farmacología (Di Marzo, 2018).
En conjunto, la evolución del conocimiento sobre el cannabigerol refleja el desarrollo progresivo de la ciencia del cannabis: desde la identificación de compuestos individuales hasta la comprensión de sistemas biológicos complejos, donde moléculas como el CBG ocupan un papel estructural y funcional clave.
Estructura química y propiedades del CBG
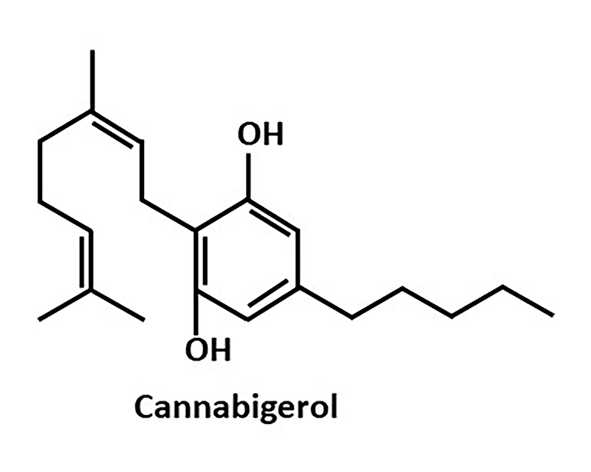
El cannabigerol (CBG) es un fitocannabinoide de naturaleza lipofílica perteneciente a la familia de los compuestos terpenofenólicos. Su estructura química deriva de la unión entre un núcleo fenólico (procedente del ácido olivetólico) y una cadena prenilada (derivada del geranil difosfato), lo que le confiere características híbridas entre compuestos fenólicos y terpenoides (Fellermeier & Zenk, 1998).
A nivel molecular, el CBG presenta una estructura acíclica en comparación con otros fitocannabinoides como el THC, que posee un sistema tricíclico. Esta diferencia estructural es consecuencia directa de su papel biosintético: el CBG no ha sufrido ciclación enzimática, lo que lo convierte en una molécula más flexible desde el punto de vista conformacional. Esta flexibilidad puede influir en su capacidad de interacción con diferentes dianas moleculares, al permitir múltiples configuraciones espaciales (Mechoulam & Gaoni, 1965).
La fórmula molecular del CBG es C₂₁H₃₂O₂, con un peso molecular aproximado de 316,48 g/mol. Su estructura incluye un grupo hidroxilo fenólico, responsable en parte de su reactividad química y de su capacidad para formar interacciones de tipo puente de hidrógeno. Además, la cadena alquílica lateral contribuye significativamente a su lipofilia, favoreciendo su afinidad por entornos biológicos ricos en lípidos, como las membranas celulares (Pertwee, 2008).
Desde el punto de vista fisicoquímico, el CBG es una molécula altamente hidrofóbica, prácticamente insoluble en agua y soluble en disolventes orgánicos como etanol o aceites vegetales. Esta propiedad condiciona su comportamiento farmacocinético, especialmente en lo relativo a su absorción y distribución en sistemas biológicos. Su estabilidad también está influida por factores como la luz, el oxígeno y la temperatura, pudiendo sufrir procesos de degradación o transformación química en determinadas condiciones (Gülck & Møller, 2020).
En su forma natural, el CBG se encuentra principalmente en la planta como ácido cannabigerólico (CBGA), su forma carboxilada. La conversión de CBGA a CBG se produce mediante un proceso de descarboxilación, generalmente inducido por calor, en el que se libera dióxido de carbono (CO₂). Este proceso es común a otros fitocannabinoides y constituye un paso clave en la obtención de sus formas neutras activas desde el punto de vista químico (Taura et al., 2007).
Desde una perspectiva estructural comparativa, la ausencia de ciclación en el CBG lo diferencia significativamente de otros cannabinoides como el CBD y el THC, cuyas estructuras presentan anillos adicionales formados por reacciones enzimáticas específicas. Esta característica posiciona al CBG como un intermediario estructural dentro de la diversidad química del cannabis, reflejando su papel como precursor en la biosíntesis de compuestos más complejos.
En conjunto, la estructura química del CBG no solo define sus propiedades fisicoquímicas, sino que también condiciona su papel biológico y su capacidad de interacción con múltiples sistemas moleculares, situándolo como una molécula clave tanto en la química del cannabis como en la investigación farmacológica contemporánea.
Biosíntesis del CBG y papel del CBGA como precursor universal
El cannabigerol (CBG) no se sintetiza directamente como tal en la planta de Cannabis sativa, sino que deriva de su forma ácida precursora, el ácido cannabigerólico (CBGA), una molécula central en la biosíntesis de los fitocannabinoides. El CBGA es considerado el principal intermediario metabólico del que se originan la mayoría de los cannabinoides conocidos, lo que lo sitúa como un nodo fundamental en la red biosintética del cannabis (Fellermeier & Zenk, 1998; Taura et al., 2007).
Formación del CBGA: condensación de GPP y ácido olivetólico
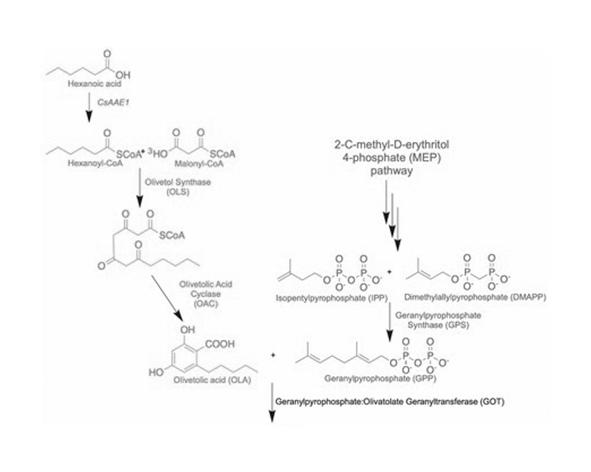
La biosíntesis del CBGA comienza con la convergencia de dos rutas metabólicas distintas: la vía del mevalonato (o MEP/DOXP en plastidios), responsable de la producción de precursores terpenoides, y la vía de los poliquétidos, que genera compuestos fenólicos.
Por un lado, el geranil difosfato (GPP), un intermediario clave en la biosíntesis de monoterpenos, aporta la cadena prenilada. Por otro, el ácido olivetólico, sintetizado a partir de unidades de malonil-CoA mediante una poliquétido sintasa (PKS), proporciona el núcleo fenólico. La unión de ambos compuestos está catalizada por una preniltransferasa específica (geraniltransferasa), dando lugar al CBGA (Fellermeier & Zenk, 1998; Gagne et al., 2012).
Este paso representa un punto de control crítico en la biosíntesis cannabinoide, ya que determina la disponibilidad del precursor común para la generación de otros fitocannabinoides.
Conversión del CBGA en otros cannabinoides
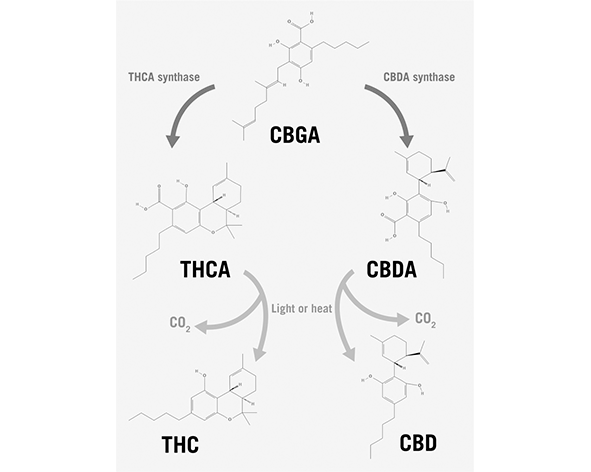
Una vez formado, el CBGA puede ser transformado en distintos ácidos cannabinoides mediante la acción de enzimas oxidasas específicas:
- THCA sintasa → convierte CBGA en ácido tetrahidrocannabinólico (THCA)
- CBDA sintasa → convierte CBGA en ácido cannabidiólico (CBDA)
- CBCA sintasa → convierte CBGA en ácido cannabicroménico (CBCA)
Estas reacciones implican procesos de ciclación oxidativa que generan las estructuras características de cada cannabinoide. La expresión diferencial de estas enzimas en la planta determina el quimiotipo (chemovar) del cannabis, es decir, el perfil final de cannabinoides presentes (Taura et al., 2007; Sirikantaramas et al., 2004).
En este contexto, el CBG aparece como producto final únicamente cuando el CBGA no es transformado por estas enzimas o cuando su actividad es limitada, lo que explica su baja concentración en la mayoría de las variedades convencionales.
Descarboxilación: de CBGA a CBG
El paso final para la obtención de CBG es la descarboxilación del CBGA, un proceso no enzimático que implica la pérdida de un grupo carboxilo en forma de dióxido de carbono (CO₂). Esta transformación puede ocurrir de manera natural con el tiempo o acelerarse mediante la exposición al calor (Taura et al., 2007).
CBGA → CBG + CO₂
Este mismo mecanismo es común a otros cannabinoides ácidos, como el THCA o el CBDA, y constituye un proceso clave tanto en contextos naturales como en aplicaciones industriales.
Regulación biosintética y acumulación de CBG
La concentración final de CBG en la planta depende de varios factores, incluyendo la actividad enzimática, la genética de la variedad y el estado de desarrollo de la planta. En variedades convencionales, la alta eficiencia de las sintasas cannabinoides conduce a una conversión casi completa del CBGA en otros cannabinoides, dejando niveles residuales de CBG.
Sin embargo, mediante técnicas de selección genética o modificación de la expresión enzimática, es posible obtener variedades ricas en CBG, donde la actividad de estas sintasas está reducida o ausente. Estas variedades representan un modelo interesante para el estudio del metabolismo cannabinoide y han cobrado relevancia en investigación y desarrollo (Gülck & Møller, 2020).
Distribución en la planta y contexto fisiológico
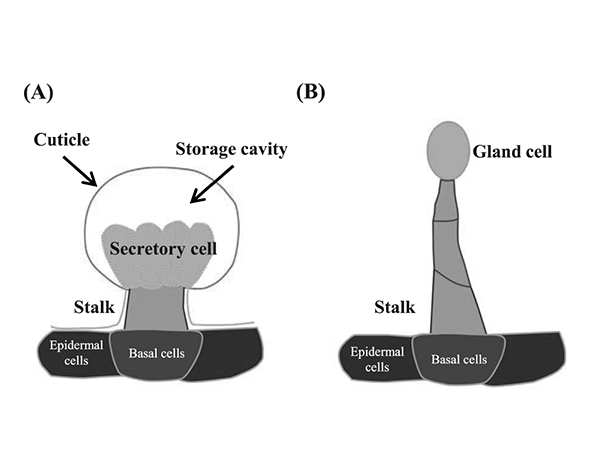
El cannabigerol (CBG) y su forma ácida precursora, el ácido cannabigerólico (CBGA), se sintetizan y acumulan principalmente en las estructuras glandulares de Cannabis sativa, especialmente en los tricomas glandulares que recubren las flores femeninas. Estos tricomas representan el principal sitio de biosíntesis y almacenamiento de fitocannabinoides, actuando como microcompartimentos especializados donde se concentran enzimas, precursores y metabolitos secundarios (Happyana et al., 2013).
Los tricomas glandulares del cannabis se clasifican en varios tipos —capitados pedunculados, capitados sésiles y bulbosos— siendo los capitados pedunculados los más relevantes desde el punto de vista cannabinoide. En estas estructuras, el CBGA se sintetiza en las células secretoras y posteriormente se acumula en la cavidad subcuticular del tricoma, donde también se encuentran otros cannabinoides y compuestos terpénicos (Livingston et al., 2020).
Desde un punto de vista espacial, la mayor concentración de CBGA (y por extensión, la base del CBG) se localiza en las inflorescencias femeninas en fases tempranas de desarrollo. A medida que la planta madura, la actividad de las enzimas sintasas (THCA sintasa, CBDA sintasa, etc.) transforma progresivamente el CBGA en otros cannabinoides, reduciendo la cantidad disponible para su conversión en CBG. Este patrón dinámico explica por qué el CBG suele encontrarse en niveles bajos en plantas completamente maduras (Taura et al., 2007).
En términos fisiológicos, la producción de CBGA y otros cannabinoides en los tricomas se ha asociado a funciones de defensa química de la planta. Estos compuestos pueden actuar como agentes protectores frente a herbívoros, patógenos y radiación ultravioleta, contribuyendo a la adaptación del cannabis a su entorno. La acumulación en estructuras externas como los tricomas sugiere un papel ecológico más que metabólico interno, en línea con otros metabolitos secundarios vegetales (Andre et al., 2016).
Además de las flores, cantidades menores de CBG/CBGA pueden detectarse en hojas, tallos y otras partes de la planta, aunque en concentraciones significativamente inferiores. Esta distribución desigual refleja la especialización funcional de las inflorescencias femeninas como centros de producción de metabolitos bioactivos.
Desde una perspectiva agronómica, la distribución del CBG está influida por factores genéticos y ambientales, incluyendo la variedad (chemovar), la intensidad lumínica, las condiciones de cultivo y el momento de cosecha. En particular, la selección de variedades con baja actividad de sintasas cannabinoides permite la acumulación de CBGA y, tras descarboxilación, de CBG, lo que ha dado lugar al desarrollo de cultivos específicamente ricos en este fitocannabinoide (Gülck & Møller, 2020).
En conjunto, la distribución del CBG en la planta refleja su papel como intermediario biosintético y su estrecha relación con la dinámica metabólica de los tricomas glandulares, consolidando su relevancia tanto en la biología del cannabis como en su aprovechamiento científico y agronómico.
Interacción con el sistema endocannabinoide y dianas moleculares
El cannabigerol (CBG) presenta un perfil farmacológico complejo caracterizado por su capacidad de interactuar con múltiples dianas moleculares más allá de los receptores cannabinoides clásicos. Aunque inicialmente fue considerado un ligando secundario dentro del sistema endocannabinoide, investigaciones posteriores han demostrado que su actividad se extiende a diversos sistemas de señalización, integrándose dentro del denominado endocannabinoidome, una red expandida de receptores, enzimas y lípidos bioactivos (Pertwee, 2008; Di Marzo, 2018).
Interacción con receptores cannabinoides CB1 y CB2
El CBG muestra afinidad moderada por los receptores cannabinoides CB1 y CB2, actuando principalmente como agonista parcial o modulador funcional dependiendo del contexto experimental. Su afinidad por CB1 es significativamente menor que la del THC, lo que explica la ausencia de efectos psicotrópicos asociados a este compuesto. En el caso de CB2, su interacción sugiere un posible papel en procesos relacionados con la señalización inmunológica y periférica (Pertwee, 2008; Cascio et al., 2010).
Además, algunos estudios han propuesto que el CBG puede comportarse como antagonista competitivo en determinadas condiciones, lo que refuerza la idea de que su actividad no es lineal ni uniforme, sino dependiente del entorno molecular y del sistema experimental utilizado.
Interacción con canales iónicos TRP
El CBG interactúa de manera significativa con varios canales de la familia TRP (Transient Receptor Potential), implicados en la transducción de estímulos físicos y químicos. En particular, se ha observado actividad sobre TRPV1, TRPA1 y TRPM8:
- Activación de TRPV1, canal implicado en la detección de calor y estímulos nociceptivos
- Activación de TRPA1, asociado a respuestas químicas irritantes
- Inhibición de TRPM8, relacionado con la percepción del frío
Estas interacciones sugieren un papel modulador del CBG en la señalización sensorial y en la regulación de la excitabilidad celular (De Petrocellis et al., 2011).
Interacción con receptores serotoninérgicos y adrenérgicos
El CBG también ha mostrado afinidad por el receptor serotoninérgico 5-HT1A, donde actúa como agonista parcial. Este receptor está implicado en múltiples procesos neuroquímicos, incluyendo la regulación del estado de ánimo, la ansiedad y la respuesta al estrés.
Adicionalmente, se ha descrito su actividad sobre receptores adrenérgicos α2, donde podría actuar como agonista, modulando la liberación de neurotransmisores y la actividad del sistema nervioso autónomo (Cascio et al., 2010).
Interacción con otras dianas moleculares
Más allá de los sistemas clásicos, el CBG también interactúa con otras proteínas y vías de señalización:
- Inhibición de la captación de anandamida, lo que podría aumentar su disponibilidad sináptica
- Interacción con receptores nucleares como PPARγ, implicados en regulación metabólica y expresión génica
- Modulación de canales de calcio y procesos intracelulares asociados a la señalización celular
Estas acciones refuerzan su papel como modulador pleiotrópico dentro del sistema endocannabinoide expandido.
CBG dentro del endocannabinoidome
El conjunto de interacciones descritas posiciona al CBG como un ligando multitarget, cuya actividad no puede explicarse únicamente a través de los receptores CB1 y CB2. Su capacidad para modular múltiples sistemas lo integra dentro del endocannabinoidome, un concepto que engloba una red funcional compleja donde convergen distintos tipos de receptores, enzimas y mediadores lipídicos (Di Marzo, 2018).
Este enfoque permite entender el CBG no como un compuesto aislado con un único mecanismo de acción, sino como una molécula capaz de influir en múltiples niveles de regulación biológica, dependiendo del contexto celular y fisiológico.
Farmacología del CBG
El perfil farmacológico del cannabigerol (CBG) se caracteriza por su naturaleza multitarget y su capacidad para modular múltiples sistemas de señalización biológica. A diferencia de otros fitocannabinoides más estudiados, el CBG no presenta un mecanismo de acción dominante único, sino que su actividad emerge de la interacción combinada con diversas dianas moleculares, lo que da lugar a efectos complejos y dependientes del contexto experimental (Pertwee, 2008; Di Marzo, 2018).
Modulación de la neurotransmisión
El CBG ha mostrado capacidad para influir en la liberación y regulación de neurotransmisores a través de su interacción con receptores cannabinoides, serotoninérgicos y adrenérgicos. Su actividad como agonista parcial en receptores 5-HT1A y su acción sobre receptores α2-adrenérgicos sugieren un papel modulador en circuitos neuronales relacionados con la excitabilidad, la respuesta al estrés y la señalización sináptica.
Además, la posible inhibición de la recaptación de anandamida podría incrementar la señalización endocannabinoide endógena, contribuyendo a efectos indirectos sobre la neurotransmisión sin actuar como agonista potente de CB1 (Cascio et al., 2010).
Regulación de la señalización inflamatoria
En modelos experimentales, el CBG ha sido estudiado por su interacción con vías relacionadas con la respuesta inflamatoria, incluyendo la modulación de mediadores celulares y la actividad de receptores implicados en procesos inmunológicos. Su afinidad por CB2 y su interacción con PPARγ sugieren una posible implicación en la regulación de la señalización periférica y la actividad celular en tejidos no neuronales.
No obstante, la evidencia disponible procede principalmente de estudios preclínicos, por lo que estos efectos deben interpretarse dentro de un contexto experimental y no como resultados extrapolables directamente a humanos (Borrelli et al., 2013).
Interacción con la señalización sensorial
El CBG modula canales iónicos de la familia TRP, incluyendo TRPV1, TRPA1 y TRPM8, lo que lo sitúa como un regulador potencial de la señalización sensorial. Estas interacciones están relacionadas con la transducción de estímulos físicos y químicos y pueden influir en la excitabilidad neuronal y en la percepción de estímulos externos.
La activación o inhibición diferencial de estos canales refleja un perfil farmacológico no lineal, donde el efecto final depende del equilibrio entre distintas vías de señalización (De Petrocellis et al., 2011).
Efectos sobre la homeostasis celular
El CBG también ha sido implicado en procesos relacionados con la homeostasis celular, incluyendo la regulación del calcio intracelular, la señalización redox y la actividad metabólica. Su interacción con receptores nucleares como PPARγ sugiere una posible influencia en la expresión génica y en la regulación de procesos metabólicos a nivel celular.
Este tipo de efectos refuerza la idea de que el CBG actúa no solo a nivel de receptores de membrana, sino también sobre mecanismos intracelulares que contribuyen al equilibrio funcional del organismo (O’Sullivan, 2016).
Perfil farmacológico global
En conjunto, el cannabigerol presenta un perfil farmacológico caracterizado por:
- Baja afinidad directa por CB1 → ausencia de efectos psicotrópicos
- Interacción moderada con CB2 → posible implicación en señalización periférica
- Actividad sobre múltiples dianas (TRP, 5-HT1A, α2, PPARγ)
- Modulación indirecta del sistema endocannabinoide
Este conjunto de propiedades sitúa al CBG como un modulador biológico complejo, cuya actividad no puede reducirse a un único mecanismo de acción.
Mecanismos moleculares de señalización del CBG
El cannabigerol (CBG) ejerce sus efectos biológicos a través de una combinación de mecanismos moleculares que implican tanto receptores de membrana como procesos intracelulares. A diferencia de ligandos con alta selectividad, el CBG actúa como un modulador pleiotrópico cuya señalización depende de la convergencia de múltiples vías, lo que genera respuestas celulares complejas y dependientes del contexto (Di Marzo, 2018; Pertwee, 2008).
Señalización mediada por receptores acoplados a proteína G (GPCRs)
El CBG interactúa con varios receptores acoplados a proteína G, incluyendo CB1, CB2, 5-HT1A y receptores adrenérgicos α2. En estos sistemas, la activación o modulación del receptor conduce a la regulación de proteínas G (principalmente Gi/o), lo que se traduce en:
- Inhibición de la adenilato ciclasa
- Disminución de los niveles intracelulares de AMPc
- Modulación de canales iónicos dependientes de voltaje
Este tipo de señalización puede reducir la excitabilidad celular y modular la liberación de neurotransmisores en terminales sinápticas, especialmente en contextos neuronales (Cascio et al., 2010).
Modulación de canales iónicos y flujo de calcio
El CBG influye en la actividad de canales iónicos, especialmente aquellos pertenecientes a la familia TRP (TRPV1, TRPA1, TRPM8). La activación de estos canales permite la entrada de cationes como Ca²⁺ y Na⁺, generando cambios en el potencial de membrana y activando cascadas de señalización intracelular.
El aumento del calcio intracelular actúa como segundo mensajero clave, desencadenando procesos como:
- Activación de quinasas dependientes de calcio
- Regulación de la liberación de neurotransmisores
- Modulación de la expresión génica
Este mecanismo sitúa al CBG como un modulador directo de la excitabilidad celular y de la señalización intracelular (De Petrocellis et al., 2011).
Interacción con receptores nucleares y regulación génica
El CBG también puede interactuar con receptores nucleares como PPARγ (Peroxisome Proliferator-Activated Receptor gamma), que actúan como factores de transcripción. La activación de estos receptores conduce a cambios en la expresión génica relacionados con:
- Metabolismo lipídico
- Respuesta inflamatoria
- Diferenciación celular
Este tipo de señalización es más lento pero tiene efectos más duraderos, ya que implica modificaciones en la maquinaria transcripcional de la célula (O’Sullivan, 2016).
Modulación de la señalización endocannabinoide endógena
El CBG puede influir indirectamente en el sistema endocannabinoide mediante la modulación de los niveles de endocannabinoides. En particular, se ha descrito su capacidad para inhibir la captación de anandamida, lo que podría aumentar su disponibilidad en el espacio sináptico y prolongar su efecto sobre receptores cannabinoides.
Este mecanismo no implica una activación directa del receptor, sino una amplificación de la señalización endógena, lo que añade una capa adicional de complejidad a su perfil farmacológico (Cascio et al., 2010).
Integración de señales y respuesta celular
La acción del CBG no se limita a una única vía, sino que resulta de la integración de múltiples señales simultáneas. Por ejemplo, la activación de canales TRP puede aumentar el calcio intracelular, mientras que la señalización vía GPCR puede modular la liberación de neurotransmisores y la actividad enzimática.
Esta convergencia de vías permite que el CBG genere respuestas celulares adaptativas, modulando procesos como la excitabilidad neuronal, la señalización metabólica y la regulación homeostática. La naturaleza multitarget de su acción implica que sus efectos finales dependen del tipo celular, la expresión de receptores y el entorno fisiológico.
Importancia en investigación científica
El cannabigerol (CBG) ha adquirido un interés creciente en la investigación científica contemporánea debido a su papel central en la biosíntesis de los fitocannabinoides y a su perfil farmacológico multitarget. A diferencia de otros compuestos más estudiados como el cannabidiol (CBD) o el Δ9-tetrahidrocannabinol (THC), el CBG ha sido históricamente menos investigado, lo que lo convierte en un área emergente dentro de la ciencia del cannabis y del sistema endocannabinoide (Gülck & Møller, 2020).
Uno de los principales motivos de su relevancia científica radica en su función como precursor biosintético universal. El estudio del CBGA y su conversión en otros cannabinoides ha permitido comprender con mayor precisión la regulación enzimática, la expresión génica y la variabilidad química entre distintas variedades de cannabis. Este conocimiento es clave tanto para la botánica como para la biotecnología vegetal, especialmente en el desarrollo de quimiotipos específicos mediante selección genética o ingeniería metabólica (Taura et al., 2007; Sirikantaramas et al., 2004).
En el ámbito de la farmacología, el CBG representa un modelo de estudio particularmente interesante debido a su interacción con múltiples dianas moleculares. Su perfil multitarget lo convierte en una herramienta útil para explorar la complejidad del endocannabinoidome y las interacciones entre sistemas de señalización aparentemente independientes. En este sentido, el CBG contribuye a ampliar la comprensión de cómo los lípidos bioactivos pueden modular procesos fisiológicos a diferentes niveles, desde la membrana celular hasta la regulación génica (Di Marzo, 2018).
Además, el creciente interés por fitocannabinoides “menores” ha impulsado el desarrollo de nuevas líneas de investigación centradas en compuestos que anteriormente eran considerados secundarios. Este cambio de enfoque refleja una evolución en la ciencia del cannabis, que ha pasado de estudiar moléculas individuales a analizar redes funcionales complejas donde múltiples compuestos interactúan entre sí y con el organismo.
Desde una perspectiva metodológica, el estudio del CBG también ha contribuido al avance de técnicas analíticas y experimentales, incluyendo métodos de cuantificación de cannabinoides, modelos celulares específicos y sistemas de expresión enzimática. Asimismo, la disponibilidad de variedades ricas en CBG ha facilitado la investigación experimental, permitiendo estudiar sus propiedades de forma más aislada y controlada (García et al., 2021).
No obstante, es importante señalar que gran parte de la evidencia disponible sobre el CBG procede de estudios preclínicos, incluyendo modelos in vitro y animales. La investigación en humanos es aún limitada, lo que subraya la necesidad de estudios clínicos bien diseñados que permitan evaluar su relevancia en contextos fisiológicos reales.
En conjunto, el cannabigerol se posiciona como una molécula clave en la investigación científica del cannabis, no solo por su papel en la biosíntesis de otros cannabinoides, sino también por su capacidad para servir como modelo en el estudio de sistemas biológicos complejos. Su estudio continúa aportando información valiosa sobre la química, la biología y la farmacología de los fitocannabinoides, consolidándolo como un elemento relevante dentro del conocimiento científico actual.
Referencias
- Andre, C. M., Hausman, J. F., & Guerriero, G. (2016). Cannabis sativa: The plant of the thousand and one molecules. Frontiers in Plant Science, 7, 19. - Borrelli, F., Fasolino, I., Romano, B., Capasso, R., Maiello, F., Coppola, D., Orlando, P., Battista, G., Pagano, E., Di Marzo, V., & Izzo, A. A. (2013). Beneficial effect of the non-psychotropic plant cannabinoid cannabigerol on experimental inflammatory bowel disease. Biochemical Pharmacology, 85(9), 1306–1316. - Cascio, M. G., Gauson, L. A., Stevenson, L. A., Ross, R. A., & Pertwee, R. G. (2010). Evidence that the plant cannabinoid cannabigerol is a highly potent α2-adrenoceptor agonist and moderately potent 5-HT1A receptor ligand. British Journal of Pharmacology, 159(1), 129–141. - De Petrocellis, L., Ligresti, A., Moriello, A. S., Allarà, M., Bisogno, T., Petrosino, S., Stott, C. G., & Di Marzo, V. (2011). Effects of cannabinoids and cannabinoid-enriched Cannabis extracts on TRP channels and endocannabinoid metabolic enzymes. British Journal of Pharmacology, 163(7), 1479–1494. - Di Marzo, V. (2018). New approaches and challenges to targeting the endocannabinoid system. Nature Reviews Drug Discovery, 17(9), 623–639. - Fellermeier, M., & Zenk, M. H. (1998). Prenylation of olivetolate by a hemp transferase yields cannabigerolic acid, the precursor of tetrahydrocannabinol. FEBS Letters, 427(2), 283–285. - Gagne, S. J., Stout, J. M., Liu, E., Boubakir, Z., Clark, S. M., & Page, J. E. (2012). Identification of olivetolic acid cyclase from Cannabis sativa reveals a unique catalytic route to plant polyketides. Proceedings of the National Academy of Sciences, 109(31), 12811–12816. - Gaoni, Y., & Mechoulam, R. (1964). Isolation, structure, and partial synthesis of an active constituent of hashish. Journal of the American Chemical Society, 86(8), 1646–1647. - Gülck, T., & Møller, B. L. (2020). Phytocannabinoids: Origins and biosynthesis. Trends in Plant Science, 25(10), 985–1004. - O’Sullivan, S. E. (2016). An update on PPAR activation by cannabinoids. British Journal of Pharmacology, 173(12), 1899–1910. - Pertwee, R. G. (2008). The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids. British Journal of Pharmacology, 153(2), 199–215. - Sirikantaramas, S., Morimoto, S., Shoyama, Y., Ishikawa, Y., Wada, Y., Shoyama, Y., & Taura, F. (2004). The gene controlling marijuana psychoactivity: Molecular cloning and heterologous expression of Δ1-tetrahydrocannabinolic acid synthase. Journal of Biological Chemistry, 279(38), 39767–39774. - Taura, F., Sirikantaramas, S., Shoyama, Y., Yoshikai, K., Shoyama, Y., & Morimoto, S. (2007). Cannabidiolic-acid synthase, the chemotype-determining enzyme in the fiber-type Cannabis sativa. FEBS Letters, 581(16), 2929–2934.