Introducción
El cannabidiol (CBD) es uno de los principales compuestos bioactivos presentes en la planta Cannabis sativa L., una especie vegetal que ha acompañado al ser humano durante miles de años con usos industriales, textiles y, más recientemente, científicos. A diferencia de otros cannabinoides como el tetrahidrocannabinol (THC), el CBD no produce efectos psicoactivos, lo que ha despertado un creciente interés en su estudio dentro de contextos relacionados con la biología, la farmacología y el bienestar general (Pertwee, 2008; Izzo et al., 2009).
En los últimos años, el CBD ha pasado de ser un compuesto prácticamente desconocido para el público general a convertirse en un término ampliamente buscado en internet, asociado tanto a productos derivados del cáñamo como a investigaciones científicas sobre el sistema endocannabinoide. Este crecimiento ha venido acompañado de una gran cantidad de información, no siempre rigurosa, que mezcla datos científicos con interpretaciones simplificadas o directamente erróneas, generando confusión en torno a qué es realmente el CBD y cómo interactúa con el organismo humano (Russo, 2011).
Desde un punto de vista científico, el interés por el CBD se debe principalmente a su capacidad para interactuar con múltiples dianas moleculares, incluyendo receptores, enzimas y canales iónicos, sin seguir un único mecanismo de acción definido. Esta característica lo diferencia de otros compuestos más específicos y lo sitúa dentro de un campo de estudio complejo, donde su papel se investiga en relación con procesos fisiológicos como la modulación de la señalización celular, el equilibrio homeostático y la comunicación intercelular (McPartland et al., 2015).
En paralelo, el desarrollo de productos derivados del cáñamo industrial ha acercado el término CBD al consumidor, especialmente en formatos como aceites, cosméticos o extractos, generando una nueva categoría dentro del mercado europeo. Sin embargo, este fenómeno también ha puesto de manifiesto la necesidad de separar claramente el conocimiento científico disponible de las expectativas comerciales o interpretaciones simplificadas, especialmente en un entorno regulatorio como el europeo, donde el uso del CBD está sujeto a restricciones específicas según su aplicación y presentación.
Este artículo tiene como objetivo ofrecer una explicación clara, rigurosa y actualizada sobre qué es el CBD, cómo se obtiene, cómo interactúa con el organismo y cuál es su contexto científico y regulatorio actual. A lo largo del contenido se abordarán los principales conceptos necesarios para entender este compuesto desde una perspectiva divulgativa, evitando afirmaciones exageradas y priorizando la información basada en evidencia disponible.
Historia del descubrimiento
El cannabidiol (CBD) fue aislado por primera vez en la década de 1940, en un contexto en el que la investigación sobre los compuestos del Cannabis sativa L. se encontraba todavía en una fase inicial y fragmentada. En 1940, el químico estadounidense Roger Adams logró obtener un extracto parcialmente purificado a partir de cáñamo industrial, identificando por primera vez un compuesto no psicoactivo distinto de otros componentes conocidos de la planta. Sin embargo, en ese momento no se conocía con precisión su estructura química ni su relevancia biológica (Adams et al., 1940).
Durante las décadas siguientes, el avance en la caracterización de los cannabinoides fue limitado, en parte debido a restricciones legales y a la complejidad química de los extractos vegetales. No fue hasta los años 60 cuando se produjo un avance decisivo gracias al trabajo del químico israelí Raphael Mechoulam y su equipo. En 1963, lograron describir por primera vez la estructura química completa del cannabidiol, estableciendo su fórmula molecular y diferenciándolo claramente de otros cannabinoides presentes en la planta (Mechoulam & Shvo, 1963).
Un año más tarde, en 1964, el mismo grupo identificó y aisló el tetrahidrocannabinol (THC), el principal compuesto psicoactivo del cannabis, lo que permitió establecer una distinción funcional clave entre ambos cannabinoides. Mientras que el THC mostraba efectos psicoactivos evidentes, el CBD carecía de estos efectos, lo que despertó interés en su perfil farmacológico diferenciado y en su posible interacción con sistemas biológicos distintos o moduladores (Gaoni & Mechoulam, 1964).
A partir de la década de 1970, el interés científico en el CBD continuó de forma intermitente, con estudios centrados en su farmacocinética, metabolismo y posibles efectos en modelos animales. Sin embargo, el verdadero punto de inflexión en la investigación de los cannabinoides no llegó hasta el descubrimiento del sistema endocannabinoide en la década de 1990, incluyendo la identificación de los receptores CB1 y CB2 y de ligandos endógenos como la anandamida. Este hallazgo proporcionó por primera vez un marco fisiológico en el que situar la acción del CBD, aunque su mecanismo de interacción seguía siendo menos directo que el de otros cannabinoides (Devane et al., 1992; Di Marzo et al., 1998).
En el siglo XXI, el CBD ha pasado a ocupar un lugar central en la investigación sobre cannabinoides, impulsado tanto por el avance en técnicas analíticas como por un cambio progresivo en la regulación del cáñamo industrial en distintas regiones del mundo. Este contexto ha permitido una mayor estandarización de extractos, una mejora en la calidad de los estudios y un interés creciente por comprender su interacción con múltiples dianas moleculares más allá de los receptores cannabinoides clásicos (McPartland et al., 2015).
Estructura química y propiedades fisicoquímicas
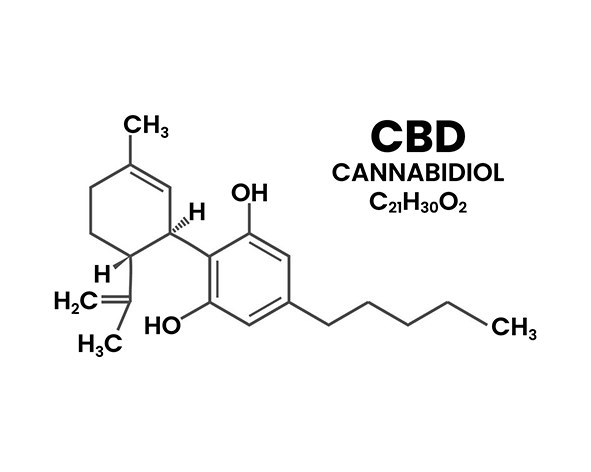
El cannabidiol (CBD) es un fitocannabinoide de naturaleza lipofílica cuya fórmula molecular es C₂₁H₃₀O₂ y cuya masa molecular aproximada es de 314,47 g/mol. Desde el punto de vista estructural, pertenece a la familia de los cannabinoides de tipo meroterpenoide, ya que deriva biosintéticamente de la combinación de una unidad terpénica (geranil pirofosfato) y un precursor fenólico (ácido olivetólico). Esta característica sitúa al CBD dentro de una clase de compuestos híbridos que combinan propiedades típicas de los terpenos y de los fenoles (Mechoulam & Shvo, 1963; Taura et al., 2007).
La estructura del CBD se caracteriza por la presencia de un núcleo aromático sustituido con dos grupos hidroxilo fenólicos y una cadena lateral pentílica, así como un sistema de anillos parcialmente abiertos en comparación con otros cannabinoides como el tetrahidrocannabinol (THC). A diferencia de este último, el CBD no presenta un anillo piránico cerrado, lo que influye de manera significativa en su interacción con los receptores cannabinoides y en su perfil farmacológico, al no encajar de forma directa en los sitios de unión clásicos de CB1 (Pertwee, 2008).
Desde el punto de vista fisicoquímico, el CBD es un compuesto altamente lipofílico y prácticamente insoluble en agua, pero soluble en disolventes orgánicos como etanol, metanol o aceites vegetales. Esta propiedad condiciona su formulación en productos comerciales, donde suele disolverse en aceites portadores para facilitar su manejo y biodisponibilidad. Su carácter lipofílico también influye en su distribución en sistemas biológicos, favoreciendo su acumulación en tejidos ricos en lípidos (Millar et al., 2018).
El CBD presenta además cierta inestabilidad frente a factores ambientales como la luz, el calor y el oxígeno. Bajo determinadas condiciones, puede sufrir procesos de oxidación o ciclación que dan lugar a otros cannabinoides o derivados, incluyendo la posible conversión en compuestos estructuralmente relacionados. Este comportamiento químico ha sido objeto de estudio, especialmente en el contexto de almacenamiento, estabilidad de formulaciones y control de calidad en productos derivados del cáñamo (Turner et al., 1980).
Otra propiedad relevante es su capacidad para actuar como antioxidante en sistemas químicos, atribuida a la presencia de grupos fenólicos capaces de donar electrones. Aunque este efecto se ha observado principalmente en modelos experimentales, refleja la versatilidad química del CBD y su potencial interacción con procesos redox a nivel celular, lo que ha contribuido a su interés dentro de diferentes líneas de investigación (Hampson et al., 1998).
En conjunto, las propiedades estructurales y fisicoquímicas del CBD explican en gran medida su comportamiento en sistemas biológicos, su interacción con múltiples dianas moleculares y su necesidad de formulación específica para su uso en productos derivados del cáñamo. Estas características lo diferencian claramente de otros cannabinoides y constituyen la base para comprender su perfil funcional dentro del sistema endocannabinoide y más allá.
Biosíntesis y origen en la planta
El cannabidiol (CBD) no se produce directamente en la planta de Cannabis sativa L. en su forma final neutra, sino que se sintetiza inicialmente como su precursor ácido, el ácido cannabidiólico (CBDA). Este proceso tiene lugar principalmente en las glándulas tricómicas de la planta, estructuras especializadas localizadas en la superficie de las flores femeninas, donde se concentra la maquinaria biosintética responsable de la producción de fitocannabinoides (Happyana et al., 2013).
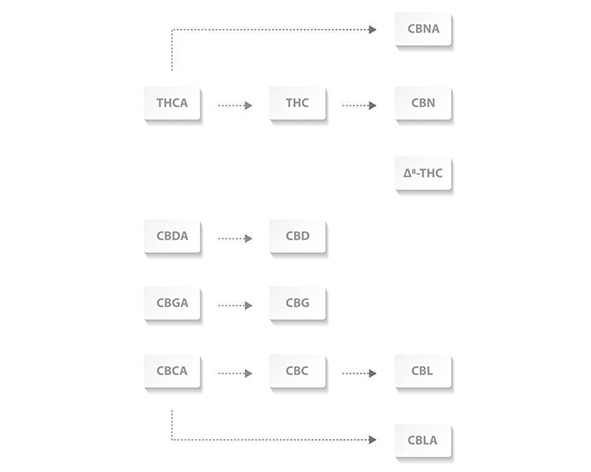
La biosíntesis del CBD forma parte de una ruta metabólica más amplia que combina dos vías fundamentales: la vía del poliquétido y la vía del mevalonato. En primer lugar, el ácido olivetólico se genera a partir de unidades de acetil-CoA mediante la acción de enzimas tipo poliquétido sintasa. Paralelamente, el geranil pirofosfato (GPP), un intermediario clave en la biosíntesis de terpenos, se produce a través de la vía del mevalonato. La condensación de ambos compuestos da lugar al cannabigerólico ácido (CBGA), considerado el precursor central de la mayoría de los cannabinoides conocidos (Taura et al., 2007).
El CBGA actúa como punto de ramificación en la biosíntesis de cannabinoides, ya que puede ser transformado en diferentes ácidos cannabinoides en función de la enzima específica presente en la planta. En el caso del CBD, la enzima clave es la CBDA sintasa, que cataliza la conversión del CBGA en CBDA mediante una reacción oxidativa altamente específica. La expresión diferencial de esta enzima es uno de los factores que determina el perfil químico de la planta, diferenciando variedades ricas en CBD de aquellas con mayor contenido en THC (Sirikantaramas et al., 2004).
Una vez formado, el CBDA puede convertirse en CBD a través de un proceso no enzimático conocido como descarboxilación. Este proceso implica la pérdida de un grupo carboxilo en forma de dióxido de carbono (CO₂) y puede ocurrir de manera natural con el tiempo o acelerarse mediante la exposición al calor, como sucede durante procesos de secado, extracción o formulación. Este paso es fundamental para obtener el CBD en su forma activa tal y como se encuentra en la mayoría de los productos derivados del cáñamo (Dussy et al., 2005).
Es importante destacar que la biosíntesis de cannabinoides está estrechamente regulada por factores genéticos y ambientales. Variables como la genética de la planta, la intensidad lumínica, la temperatura o las condiciones de cultivo pueden influir significativamente en la concentración final de CBDA y, por extensión, de CBD. Esta variabilidad ha llevado al desarrollo de cultivares específicos de cáñamo industrial optimizados para la producción de CBD, cumpliendo además con los límites legales de contenido en THC establecidos en diferentes jurisdicciones (Andre et al., 2016).
En conjunto, la formación del CBD en la planta responde a un proceso altamente especializado que integra rutas metabólicas complejas y una regulación enzimática precisa. Comprender este origen biosintético es esencial para interpretar las diferencias entre extractos, la variabilidad entre productos y el papel del CBD dentro del conjunto de compuestos presentes en el cáñamo.
Distribución en la planta y en productos derivados
El cannabidiol (CBD) se distribuye de forma heterogénea en la planta de Cannabis sativa L., concentrándose principalmente en las flores femeninas no fecundadas, donde se desarrollan en alta densidad las glándulas tricómicas. Estas estructuras epidérmicas especializadas actúan como centros de síntesis y almacenamiento de fitocannabinoides, incluyendo el ácido cannabidiólico (CBDA), precursor directo del CBD. En menor medida, también pueden encontrarse cannabinoides en hojas y tallos, aunque en concentraciones significativamente más bajas (Happyana et al., 2013).
Los tricomas glandulares, especialmente los de tipo capitado-sésil y capitado-pedunculado, contienen matrices resinosas ricas en cannabinoides, terpenos y otros compuestos lipofílicos. Esta resina constituye la base química de los extractos obtenidos a partir de la planta. La densidad y maduración de estos tricomas influyen directamente en la cantidad y composición de cannabinoides presentes, siendo factores clave en la calidad del material vegetal destinado a extracción (Andre et al., 2016).
En el contexto de los productos derivados del cáñamo, el CBD no se encuentra como tal en la materia prima vegetal en grandes cantidades, sino que suele obtenerse tras procesos de extracción y transformación. Técnicas como la extracción con CO₂ supercrítico o con disolventes orgánicos permiten aislar la fracción lipofílica de la planta, concentrando cannabinoides y otros compuestos asociados. Posteriormente, estos extractos pueden someterse a procesos de refinado, descarboxilación y estandarización para obtener formulaciones con perfiles específicos (Rovetto & Aieta, 2017).
Dependiendo del grado de procesamiento, los extractos pueden conservar diferentes proporciones de compuestos presentes en la planta original. En algunos casos, se mantienen múltiples cannabinoides y terpenos en lo que se denomina extracto de espectro completo, mientras que en otros se eliminan ciertos componentes para obtener perfiles más definidos o incluso compuestos aislados. Esta variabilidad da lugar a diferentes categorías de productos, que responden tanto a decisiones técnicas como regulatorias (Hazekamp, 2018).
En los productos finales, el CBD suele presentarse disuelto en matrices lipídicas, como aceites vegetales, debido a su naturaleza hidrofóbica. Esta formulación facilita su manipulación, estabilidad y aplicación en distintos formatos. Sin embargo, la concentración de CBD, la presencia de otros compuestos y la calidad del extracto dependen en gran medida del proceso de producción y de los estándares aplicados durante su elaboración, lo que introduce una notable heterogeneidad en el mercado (Millar et al., 2018).
En conjunto, la distribución del CBD desde la planta hasta el producto final implica una serie de transformaciones que van desde la biosíntesis en tricomas hasta su incorporación en formulaciones estandarizadas. Este recorrido es fundamental para entender las diferencias entre productos, la variabilidad en su composición y la importancia de los procesos de extracción y control de calidad en el contexto actual del cáñamo industrial.
Mecanismo de acción e interacción con el organismo
A diferencia de otros cannabinoides como el tetrahidrocannabinol (THC), el cannabidiol (CBD) no actúa como un agonista directo de los receptores cannabinoides clásicos CB1 y CB2. Su afinidad por estos receptores es relativamente baja, lo que implica que su mecanismo de acción no se basa en una activación directa, sino en una modulación indirecta de múltiples sistemas de señalización. Esta característica ha llevado a considerar al CBD como un compuesto de acción pleiotrópica, capaz de interactuar con diversas dianas moleculares de forma simultánea (Pertwee, 2008; McPartland et al., 2015).
En el contexto del sistema endocannabinoide, el CBD puede influir en la señalización endógena modulando la disponibilidad de ligandos como la anandamida. Se ha propuesto que el CBD puede interferir con la degradación de este endocannabinoide mediante la inhibición indirecta de enzimas como la FAAH (Fatty Acid Amide Hydrolase), lo que podría aumentar sus niveles en determinados contextos experimentales. Este tipo de interacción no implica una activación directa del sistema, sino una regulación de su equilibrio funcional (Bisogno et al., 2001).
Además de su relación con el sistema endocannabinoide, el CBD interactúa con otros sistemas de señalización relevantes. Entre ellos se encuentran los receptores serotoninérgicos, especialmente el receptor 5-HT1A, con el que ha mostrado afinidad en estudios experimentales, así como diversos canales iónicos de la familia TRP (Transient Receptor Potential), implicados en la percepción sensorial y en procesos celulares relacionados con el calcio intracelular (Russo et al., 2005; De Petrocellis et al., 2011).
El CBD también ha sido descrito como modulador alostérico negativo del receptor CB1, lo que significa que puede alterar la forma en la que otros ligandos, como el THC, interactúan con dicho receptor. Este efecto modulador puede influir en la intensidad o naturaleza de la señalización cannabinoide, añadiendo un nivel adicional de complejidad a su perfil farmacológico (Laprairie et al., 2015).
Otra línea de investigación relevante se centra en su interacción con receptores nucleares como PPARγ (Peroxisome Proliferator-Activated Receptor gamma), que participan en la regulación de la expresión génica y en procesos metabólicos. Esta interacción sugiere que el CBD podría influir en la actividad celular a nivel transcripcional, ampliando su rango de acción más allá de la señalización de membrana (O’Sullivan, 2007).
En conjunto, el mecanismo de acción del CBD no puede explicarse a través de una única vía o receptor, sino como el resultado de una red compleja de interacciones moleculares. Esta multifuncionalidad lo diferencia de compuestos con dianas más específicas y explica en parte la dificultad para definir de manera precisa sus efectos en sistemas biológicos. En lugar de actuar como un activador directo, el CBD parece desempeñar un papel modulador dentro de distintos sistemas de señalización, contribuyendo al equilibrio dinámico del organismo en contextos experimentales.
Interacción con el sistema endocannabinoide
El sistema endocannabinoide (SEC) es una red de señalización biológica compuesta por receptores cannabinoides, ligandos endógenos —como la anandamida (AEA) y el 2-araquidonoilglicerol (2-AG)— y enzimas responsables de su síntesis y degradación. Este sistema participa en la regulación de múltiples procesos fisiológicos, actuando como un modulador del equilibrio interno u homeostasis en distintos tejidos y sistemas del organismo (Di Marzo et al., 1998; Pertwee, 2008).
A diferencia de los endocannabinoides, que se unen directamente a los receptores CB1 y CB2 como agonistas, el cannabidiol (CBD) no muestra una afinidad significativa por estos receptores en condiciones fisiológicas. En lugar de activar directamente el sistema, el CBD interactúa con él de forma indirecta, modulando distintos componentes de la señalización endocannabinoide. Esta interacción indirecta es uno de los rasgos más característicos de su perfil molecular (McPartland et al., 2015).
Uno de los mecanismos propuestos es la influencia del CBD sobre los niveles de anandamida, un endocannabinoide clave en la señalización retrógrada sináptica. Se ha observado en estudios experimentales que el CBD puede interferir con su recaptación y degradación, posiblemente mediante la inhibición indirecta de la enzima FAAH. Este efecto podría contribuir a una mayor disponibilidad de anandamida en determinados contextos, alterando de forma moduladora la actividad del sistema endocannabinoide (Bisogno et al., 2001).
Además, el CBD puede actuar como modulador alostérico negativo del receptor CB1, lo que implica que no activa el receptor por sí mismo, sino que modifica la respuesta del receptor frente a otros ligandos. Este tipo de modulación puede influir en la intensidad y naturaleza de la señalización, especialmente en presencia de cannabinoides como el THC, introduciendo un nivel adicional de regulación dentro del sistema (Laprairie et al., 2015).
El sistema endocannabinoide se caracteriza por una señalización “on demand”, en la que los endocannabinoides se sintetizan y liberan en respuesta a estímulos específicos, en lugar de almacenarse en vesículas como otros neurotransmisores. En este contexto, el papel del CBD no sería el de iniciar la señal, sino el de modular su duración, intensidad o degradación, actuando como un regulador del sistema más que como un activador directo (Alger, 2002).
En conjunto, la interacción del CBD con el sistema endocannabinoide refleja un modelo de modulación compleja en lugar de una acción farmacológica clásica basada en un único receptor. Esta relación indirecta, combinada con su capacidad para interactuar con otras dianas moleculares, sitúa al CBD dentro de un marco de regulación fisiológica más amplio, donde su papel se investiga en términos de equilibrio y adaptación biológica en sistemas experimentales.
Diferencias entre CBD y otros cannabinoides
Los cannabinoides constituyen una familia diversa de compuestos químicos que interactúan, en mayor o menor medida, con el sistema endocannabinoide. Dentro de este grupo, el cannabidiol (CBD) y el tetrahidrocannabinol (THC) son los más estudiados, pero presentan diferencias significativas tanto a nivel estructural como funcional. Estas diferencias son fundamentales para comprender el comportamiento de los extractos de Cannabis sativa L. y su interacción con el organismo (Pertwee, 2008).
Desde el punto de vista estructural, CBD y THC comparten la misma fórmula molecular (C₂₁H₃₀O₂), pero difieren en la disposición de sus átomos. En particular, el THC presenta un anillo piránico cerrado que le permite interactuar de forma más eficiente con el receptor CB1, mientras que el CBD tiene una estructura abierta que limita esta interacción directa. Esta variación aparentemente sutil tiene consecuencias significativas en su actividad biológica (Mechoulam & Shvo, 1963).
En términos funcionales, el THC actúa como un agonista parcial del receptor CB1, altamente expresado en el sistema nervioso central, lo que explica sus efectos psicoactivos característicos. Por el contrario, el CBD no activa directamente este receptor y puede incluso modular su actividad de forma alostérica negativa, reduciendo la afinidad de otros ligandos por CB1. Esta diferencia es clave para entender por qué el CBD no produce efectos psicoactivos en condiciones normales (Laprairie et al., 2015).
Además del THC, existen otros fitocannabinoides relevantes como el cannabigerol (CBG), el cannabicromeno (CBC) o el cannabinol (CBN), cada uno con perfiles de interacción distintos. El CBG, por ejemplo, es un precursor biosintético de otros cannabinoides, mientras que el CBN se forma principalmente por oxidación del THC. En este contexto, el CBD destaca por su baja afinidad directa por los receptores cannabinoides y por su capacidad de interactuar con múltiples dianas moleculares, lo que lo sitúa en una categoría funcional diferente dentro del conjunto de cannabinoides (McPartland et al., 2015).
Otra diferencia relevante radica en el papel que desempeñan dentro de los extractos de espectro completo. Mientras que el THC puede tener un impacto dominante en la señalización cannabinoide debido a su acción directa sobre CB1, el CBD puede actuar como modulador de dicha señalización, influyendo en la actividad de otros compuestos presentes en el extracto. Esta interacción entre cannabinoides ha sido objeto de estudio bajo el concepto de efectos combinados o interacciones entre compuestos, aunque su interpretación sigue siendo objeto de investigación (Russo, 2011).
En conjunto, las diferencias entre CBD y otros cannabinoides no se limitan a la presencia o ausencia de efectos psicoactivos, sino que reflejan mecanismos de acción distintos, interacciones moleculares específicas y roles diferenciados dentro del sistema endocannabinoide. Comprender estas diferencias es esencial para interpretar tanto la investigación científica como la composición y comportamiento de los productos derivados del cáñamo.
Contexto científico actual y líneas de investigación
El cannabidiol (CBD) se ha convertido en uno de los compuestos más estudiados dentro del ámbito de los cannabinoides en las últimas décadas. Este interés creciente se debe, en parte, a su perfil farmacológico complejo, a la ausencia de efectos psicoactivos y al avance en la comprensión del sistema endocannabinoide. Sin embargo, a pesar del aumento significativo en el número de publicaciones científicas, la evidencia disponible sigue siendo heterogénea y, en muchos casos, limitada por el diseño de los estudios y la variabilidad en los modelos experimentales utilizados (Izzo et al., 2009; McPartland et al., 2015).
Una parte importante de la investigación sobre el CBD se ha desarrollado en modelos preclínicos, incluyendo estudios in vitro y en animales. Estos trabajos han permitido identificar múltiples dianas moleculares potenciales, así como explorar su interacción con sistemas de señalización implicados en procesos celulares diversos. No obstante, la extrapolación de estos resultados a humanos presenta limitaciones, ya que las condiciones experimentales, las dosis empleadas y las vías de administración pueden diferir significativamente de los contextos reales (Pertwee, 2008).
En el ámbito clínico, el número de ensayos en humanos ha aumentado progresivamente, aunque sigue siendo relativamente reducido en comparación con otras áreas de investigación biomédica. Algunos estudios se han centrado en evaluar la seguridad, farmacocinética y tolerabilidad del CBD, estableciendo rangos de dosis y perfiles de interacción con otros compuestos. Estos trabajos han contribuido a generar un marco inicial para comprender su comportamiento en el organismo humano, aunque todavía existen lagunas importantes en cuanto a efectos a largo plazo y variabilidad interindividual (Millar et al., 2018).
Otro aspecto relevante es la diversidad de formulaciones utilizadas en los estudios, que incluyen desde compuestos aislados hasta extractos complejos con múltiples cannabinoides y terpenos. Esta heterogeneidad dificulta la comparación directa entre estudios y complica la interpretación de los resultados, ya que las interacciones entre compuestos pueden influir en los efectos observados. Además, la falta de estandarización en muchos productos disponibles en el mercado introduce un factor adicional de variabilidad (Hazekamp, 2018).
En paralelo, la investigación sobre el CBD se ha expandido hacia áreas como la interacción con receptores no cannabinoides, la modulación de canales iónicos, la regulación de enzimas y la posible influencia en la expresión génica. Estas líneas de estudio reflejan la naturaleza multifuncional del CBD y su potencial como modulador de sistemas biológicos complejos, aunque también subrayan la dificultad de atribuir efectos específicos a mecanismos concretos (O’Sullivan, 2007).
En el contexto regulatorio y científico actual, el CBD se encuentra en una posición intermedia entre el interés experimental y la aplicación práctica. Mientras que su estudio continúa avanzando en distintos campos, la interpretación de la evidencia requiere un enfoque crítico que tenga en cuenta las limitaciones metodológicas, la calidad de los estudios y la necesidad de investigaciones adicionales. En este sentido, el CBD representa un área activa de investigación más que un campo completamente establecido, lo que exige cautela en la extrapolación de resultados y en la formulación de conclusiones definitivas.
Importancia y contexto actual
En las últimas décadas, el cannabidiol (CBD) ha pasado de ser un compuesto de interés principalmente académico a ocupar un lugar relevante en la intersección entre investigación científica, industria del cáñamo y marcos regulatorios internacionales. Este cambio ha sido impulsado por varios factores, entre ellos el avance en la caracterización del sistema endocannabinoide, la mejora en las técnicas de extracción y análisis, y una progresiva flexibilización de la regulación del cáñamo industrial en distintas regiones del mundo (Andre et al., 2016).
Desde el punto de vista científico, el CBD representa un ejemplo de compuesto con un perfil farmacológico complejo y aún en desarrollo. Su capacidad para interactuar con múltiples dianas moleculares, junto con su baja afinidad directa por los receptores cannabinoides clásicos, ha generado un interés sostenido en distintas áreas de investigación. Sin embargo, este mismo carácter multifuncional también plantea desafíos en la interpretación de los datos y en la construcción de modelos mecanísticos claros, lo que sitúa al CBD dentro de un campo activo pero todavía en consolidación (McPartland et al., 2015).
En paralelo, el desarrollo del mercado del CBD ha dado lugar a una amplia variedad de productos derivados del cáñamo, especialmente en Europa y América del Norte. Este crecimiento ha estado acompañado de una diversificación de formatos, procesos de producción y estándares de calidad, así como de una creciente demanda por parte del consumidor. No obstante, esta expansión también ha puesto de manifiesto la necesidad de establecer criterios claros de control, trazabilidad y cumplimiento normativo, dada la variabilidad existente entre productos y la complejidad del marco legal (Hazekamp, 2018).
El contexto regulatorio del CBD es particularmente heterogéneo y evolutivo. En la Unión Europea, por ejemplo, el uso del CBD está condicionado por su origen, su forma de presentación y su finalidad declarada, diferenciando entre productos cosméticos, alimentos, extractos o preparados técnicos. Esta diversidad de enfoques regulatorios refleja tanto el interés creciente por el compuesto como la necesidad de adaptar la legislación a un campo en rápida evolución, donde la evidencia científica y el desarrollo industrial avanzan a ritmos diferentes.
Otro aspecto relevante es el papel del CBD en la comunicación pública y la percepción social del cannabis. La aparición de este compuesto en el mercado ha contribuido a diferenciar el cáñamo industrial de otras formas de cannabis, generando un nuevo espacio de discusión en torno a su uso, su regulación y su interpretación. Sin embargo, esta visibilidad también ha favorecido la proliferación de información no siempre rigurosa, lo que refuerza la importancia de enfoques divulgativos basados en evidencia y libres de afirmaciones no sustentadas.
En conjunto, el CBD se sitúa actualmente en un punto de convergencia entre ciencia, industria y regulación. Su relevancia no radica únicamente en sus propiedades químicas o biológicas, sino en su papel como objeto de estudio dentro de un sistema más amplio que incluye el conocimiento del sistema endocannabinoide, el desarrollo del cáñamo industrial y la evolución de los marcos legales asociados. Este contexto dinámico convierte al CBD en un elemento clave para entender tanto el presente como el futuro de la investigación y aplicación de los cannabinoides.
REFERENCIAS
- Adams R, Hunt M, Clark JH. (1940). Structure of cannabidiol, a product isolated from the marihuana extract of Minnesota wild hemp. Journal of the American Chemical Society, 62(1), 196–200. - Mechoulam R, Shvo Y. (1963). Hashish—I: The structure of cannabidiol. Tetrahedron, 19(12), 2073–2078. - Gaoni Y, Mechoulam R. (1964). Isolation, structure, and partial synthesis of an active constituent of hashish. Journal of the American Chemical Society, 86(8), 1646–1647. - Di Marzo V, Melck D, Bisogno T, De Petrocellis L. (1998). Endocannabinoids: endogenous cannabinoid receptor ligands with neuromodulatory action. Trends in Neurosciences, 21(12), 521–528. - Pertwee RG. (2008). The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids: Δ9-tetrahydrocannabinol, cannabidiol and Δ9-tetrahydrocannabivarin. British Journal of Pharmacology, 153(2), 199–215. - Izzo AA, Borrelli F, Capasso R, Di Marzo V, Mechoulam R. (2009). Non-psychotropic plant cannabinoids: new therapeutic opportunities from an ancient herb. Trends in Pharmacological Sciences, 30(10), 515–527. - McPartland JM, Duncan M, Di Marzo V, Pertwee RG. (2015). Are cannabidiol and Δ9-tetrahydrocannabivarin negative modulators of the endocannabinoid system? British Journal of Pharmacology, 172(3), 737–753. - Russo EB. (2011). Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. British Journal of Pharmacology, 163(7), 1344–1364. - Bisogno T, Hanus L, De Petrocellis L, et al. (2001). Molecular targets for cannabidiol and its synthetic analogues: effect on vanilloid VR1 receptors and on the cellular uptake and enzymatic hydrolysis of anandamide. British Journal of Pharmacology, 134(4), 845–852. - Laprairie RB, Bagher AM, Kelly ME, Denovan-Wright EM. (2015). Cannabidiol is a negative allosteric modulator of the cannabinoid CB1 receptor. British Journal of Pharmacology, 172(20), 4790–4805. - De Petrocellis L, Ligresti A, Moriello AS, et al. (2011). Effects of cannabinoids and cannabinoid-enriched Cannabis extracts on TRP channels and endocannabinoid metabolic enzymes. - British Journal of Pharmacology, 163(7), 1479–1494. O’Sullivan SE. (2007). Cannabinoids go nuclear: evidence for activation of peroxisome proliferator-activated receptors. British Journal of Pharmacology, 152(5), 576–582. - Taura F, Sirikantaramas S, Shoyama Y, Yoshikai K, Shoyama Y, Morimoto S. (2007). Cannabidiolic-acid synthase, the chemotype-determining enzyme in the fiber-type Cannabis sativa. FEBS Letters, 581(16), 2929–2934. - Sirikantaramas S, Taura F, Morimoto S, Shoyama Y. (2004). Recent advances in Cannabis sativa research: biosynthetic studies and its potential in biotechnology. Current Pharmaceutical Biotechnology, 5(3), 217–230. - Dussy FE, Hamberg C, Luginbühl M, Schwerzmann T, Briellmann TA. (2005). Isolation of Δ9-THCA-A from hemp and analytical aspects concerning the determination of Δ9-THC in cannabis products. Forensic Science International, 149(1), 3–10. - Andre CM, Hausman JF, Guerriero G. (2016). Cannabis sativa: The plant of the thousand and one molecules. Frontiers in Plant Science, 7, 19. - Happyana N, Agnolet S, Muntendam R, et al. (2013). Analysis of cannabinoids in laser-microdissected trichomes of Cannabis sativa using LC-MS. Analytical and Bioanalytical Chemistry, 405(23), 7355–7365. - Rovetto LJ, Aieta NV. (2017). Supercritical carbon dioxide extraction of cannabinoids from Cannabis sativa L. The Journal of Supercritical Fluids, 129, 16–27. - Hazekamp A. (2018). The trouble with CBD oil. Medical Cannabis and Cannabinoids, 1(1), 65–72. - Millar SA, Stone NL, Yates AS, O’Sullivan SE. (2018). A systematic review on the pharmacokinetics of cannabidiol in humans. Frontiers in Pharmacology, 9, 1365. - Hampson AJ, Grimaldi M, Axelrod J, Wink D. (1998). Cannabidiol and (-)Δ9-tetrahydrocannabinol are neuroprotective antioxidants. Proceedings of the National Academy of Sciences, 95(14), 8268–8273.