Introducción
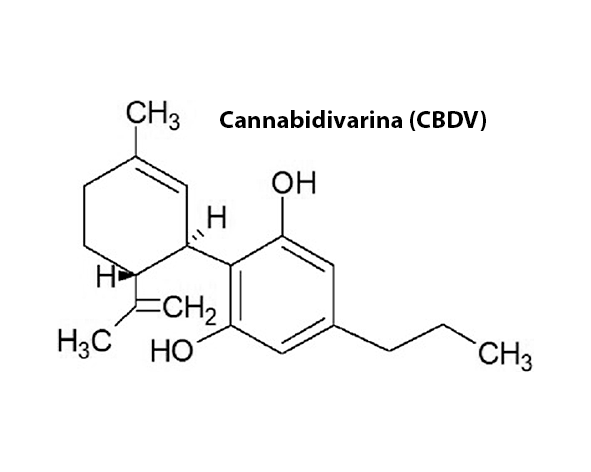
La cannabidivarina (CBDV) es un fitocannabinoide no psicotrópico perteneciente a la familia de los cannabinoides varínicos, caracterizados por presentar una cadena lateral propilo (C3) en lugar de la cadena pentilo (C5) típica de los cannabinoides más abundantes como el cannabidiol (CBD) o el Δ9-tetrahidrocannabinol (THC). Esta diferencia estructural, aparentemente menor, introduce cambios relevantes en sus propiedades fisicoquímicas y en su interacción con diferentes sistemas biológicos, particularmente en lo que respecta a su afinidad por receptores, su distribución en membranas lipídicas y su perfil farmacológico global (Citti et al., 2018).
Desde el punto de vista botánico, CBDV se encuentra en concentraciones variables dentro de Cannabis sativa L., con mayor presencia en quimiotipos específicos asociados a variedades tradicionales de origen asiático y africano. Estos quimiotipos presentan rutas biosintéticas alternativas basadas en el uso de ácido divarinólico como precursor, lo que da lugar a la formación de cannabinoides varínicos como CBDV, THCV o CBGV. No obstante, incluso en estas variedades, la concentración de CBDV suele ser considerablemente menor que la de cannabinoides mayoritarios, lo que históricamente ha dificultado su aislamiento y estudio sistemático (De Meijer et al., 2003).
El interés científico por CBDV ha aumentado de forma progresiva en la última década, en gran medida debido a la identificación de mecanismos de acción independientes del sistema endocannabinoide clásico. A diferencia de otros fitocannabinoides, CBDV muestra una interacción limitada con los receptores CB1 y CB2, actuando principalmente sobre canales iónicos y otras dianas moleculares implicadas en la regulación de la excitabilidad neuronal. Este perfil ha despertado especial interés en el estudio de trastornos neurológicos caracterizados por alteraciones en la señalización sináptica, como la epilepsia o los trastornos del neurodesarrollo (Iannotti et al., 2014; Zamberletti et al., 2019).
Además, la ausencia de efectos psicoactivos asociados a la activación de CB1 posiciona a CBDV como un compuesto particularmente interesante desde el punto de vista farmacológico, ya que permite explorar la modulación de sistemas neuronales sin las limitaciones funcionales que presentan otros cannabinoides con actividad central más marcada. En este contexto, CBDV representa un ejemplo paradigmático de la complejidad del fitocomplejo del cannabis, donde pequeñas variaciones estructurales pueden traducirse en perfiles biológicos profundamente diferenciados.
Historia del descubrimiento
La cannabidivarina (CBDV) fue identificada en el contexto de los primeros estudios fitoquímicos sistemáticos del cannabis desarrollados entre las décadas de 1960 y 1970, un periodo en el que se aislaron y caracterizaron la mayoría de los fitocannabinoides conocidos en la actualidad. Tras el aislamiento del Δ9-tetrahidrocannabinol (THC) por Raphael Mechoulam y la posterior identificación del cannabidiol (CBD), la atención de la comunidad científica se centró en la identificación de compuestos estructuralmente relacionados presentes en menores concentraciones dentro de la planta.
En este contexto, CBDV fue descrita como un análogo estructural del CBD, diferenciándose exclusivamente por la longitud de su cadena lateral alquílica. Este tipo de variación ya había sido observado en otros compuestos vegetales, pero en el caso del cannabis adquiría especial relevancia debido a la estrecha relación entre estructura química y actividad biológica en los cannabinoides (Mechoulam & Gaoni, 1965).
Durante las décadas posteriores a su identificación, CBDV permaneció en un segundo plano dentro de la investigación científica. Existen varias razones que explican esta falta de atención relativa. En primer lugar, su baja abundancia natural en la mayoría de las variedades de cannabis dificultaba su aislamiento en cantidades suficientes para estudios farmacológicos detallados. En segundo lugar, el foco principal de la investigación en ese momento estaba dirigido hacia el THC, debido a sus efectos psicoactivos, y posteriormente hacia el CBD, por su perfil no intoxicante y su potencial interés terapéutico emergente.
No fue hasta principios del siglo XXI cuando CBDV comenzó a recuperar interés dentro de la comunidad científica. Este resurgimiento estuvo estrechamente ligado a dos avances clave. Por un lado, la mejora en las técnicas analíticas, especialmente la cromatografía líquida de alta resolución (HPLC) y la espectrometría de masas, permitió identificar y cuantificar con mayor precisión cannabinoides minoritarios, incluyendo los compuestos varínicos. Por otro lado, el desarrollo de programas de selección genética en Cannabis sativa facilitó la obtención de quimiotipos enriquecidos en cannabinoides específicos, haciendo posible el estudio más sistemático de compuestos como CBDV (De Meijer et al., 2003).
El punto de inflexión en el estudio moderno de CBDV se produjo en la década de 2010, cuando comenzaron a publicarse trabajos que exploraban su papel en la modulación de la actividad neuronal. Estudios preclínicos mostraron que CBDV podía influir en la excitabilidad neuronal y en la señalización sináptica a través de mecanismos independientes de los receptores cannabinoides clásicos, lo que abrió nuevas líneas de investigación en neurociencia (Hill et al., 2012; Iannotti et al., 2014).
Este cambio de paradigma fue particularmente relevante porque coincidió con una expansión general del interés científico por el denominado endocannabinoidome, un concepto que amplía el sistema endocannabinoide clásico para incluir múltiples receptores, enzimas y mediadores lipídicos relacionados. En este contexto más amplio, CBDV dejó de ser considerado un cannabinoide “menor” para pasar a formar parte de un conjunto de compuestos con funciones potencialmente específicas dentro de redes de señalización complejas.
En la actualidad, aunque CBDV sigue siendo un compuesto relativamente poco abundante y menos estudiado que otros fitocannabinoides, su perfil farmacológico distintivo y su interacción con dianas moleculares no tradicionales lo han consolidado como un objeto de interés creciente en investigación básica y traslacional. Sin embargo, es importante señalar que gran parte de la evidencia disponible procede de modelos preclínicos, por lo que su relevancia en humanos continúa siendo objeto de estudio.
Estructura química
La cannabidivarina (CBDV) es un fitocannabinoide de tipo varínico cuya fórmula molecular es C19H26O2, diferenciándose del cannabidiol (CBD) principalmente por la presencia de una cadena lateral propilo (–C3H7) en lugar de la cadena pentilo (–C5H11). Esta variación estructural, aunque aparentemente menor, tiene implicaciones directas sobre las propiedades fisicoquímicas de la molécula y su interacción con distintas dianas biológicas (Citti et al., 2018; Pertwee, 2008).
Desde el punto de vista estructural, CBDV conserva el esqueleto característico de los cannabinoides tipo cannabidiol, compuesto por un núcleo aromático fenólico unido a una fracción terpénica derivada del geraniol. La molécula presenta dos grupos hidroxilo fenólicos libres, responsables en parte de su reactividad química y de su capacidad para establecer interacciones mediante enlaces de hidrógeno con proteínas y membranas biológicas. A diferencia del Δ9-tetrahidrocannabinol (THC), CBDV no presenta ciclación del anillo pirano, lo que le confiere una mayor flexibilidad conformacional y limita su afinidad por el receptor CB1 (Mechoulam & Hanus, 2000; Pertwee, 2008).
Cadena lateral y relación estructura-actividad (SAR)
La longitud de la cadena lateral alquílica constituye uno de los determinantes clave en la relación estructura-actividad (SAR) de los cannabinoides. En general, una mayor longitud de la cadena lateral se asocia con un incremento en la afinidad por los receptores cannabinoides CB1 y CB2, especialmente en el caso de ligandos agonistas. En este contexto, la presencia de una cadena propilo en CBDV se correlaciona con una baja afinidad por los receptores cannabinoides clásicos, lo que explica la ausencia de efectos psicoactivos (Pertwee, 2008; Cascio & Pertwee, 2014).
Además, esta modificación estructural puede influir en:
- La capacidad de inserción en la bicapa lipídica
- La orientación molecular en el entorno de membrana
- La interacción con proteínas transmembrana no canónicas
Estos factores son relevantes para comprender por qué CBDV muestra actividad sobre dianas moleculares distintas a CB1/CB2, incluyendo canales iónicos de la familia TRP (Iannotti et al., 2014).
Propiedades fisicoquímicas
CBDV presenta propiedades fisicoquímicas características de los fitocannabinoides:
- Alta lipofilicidad, aunque ligeramente inferior a la del CBD
- Baja solubilidad en medios acuosos
- Alta afinidad por entornos lipídicos
- Capacidad de atravesar membranas biológicas por difusión pasiva
La menor longitud de la cadena lateral puede traducirse en una ligera reducción de la lipofilicidad y, potencialmente, en diferencias en la distribución tisular y en la farmacocinética del compuesto. No obstante, estos aspectos aún no están completamente caracterizados a nivel clínico (Citti et al., 2018).
Configuración estereoquímica
CBDV, al igual que otros fitocannabinoides, presenta centros quirales derivados de su origen terpenofenólico. La biosíntesis en la planta genera formas estereoquímicas específicas, lo que indica un control enzimático preciso durante su formación.
La configuración tridimensional de la molécula influye en:
- La afinidad por proteínas diana
- La orientación en la membrana
- La actividad biológica global
Aunque la estereoquímica de CBDV ha sido menos estudiada que la del THC o el CBD, se considera un elemento relevante en la modulación de su actividad farmacológica (Mechoulam & Hanus, 2000).
Comparación estructural dentro del fitocomplejo
CBDV forma parte de una subfamilia de cannabinoides conocida como cannabinoides varínicos, que incluye:
- THCV (tetrahidrocannabivarina)
- CBGV (cannabigerovarina)
Estos compuestos comparten la presencia de una cadena lateral propilo, lo que los distingue de los cannabinoides “clásicos” pentílicos. Esta dualidad estructural sugiere la existencia de dos líneas biosintéticas paralelas dentro de la planta de cannabis, con implicaciones funcionales diferenciadas (De Meijer et al., 2003).
Implicaciones funcionales de la estructura
La arquitectura molecular de CBDV se traduce en un perfil funcional caracterizado por:
- Baja afinidad por CB1 y CB2
- Ausencia de psicoactividad
- Interacción con dianas no cannabinoides
- Capacidad de modular canales iónicos y señalización intracelular
En conjunto, estos elementos posicionan a CBDV como un compuesto con un mecanismo de acción multimodal, donde la estructura química condiciona una interacción más distribuida y menos específica que la observada en cannabinoides con alta afinidad por receptores clásicos (Iannotti et al., 2014; Zamberletti et al., 2019).
Distribución y biosíntesis en la planta
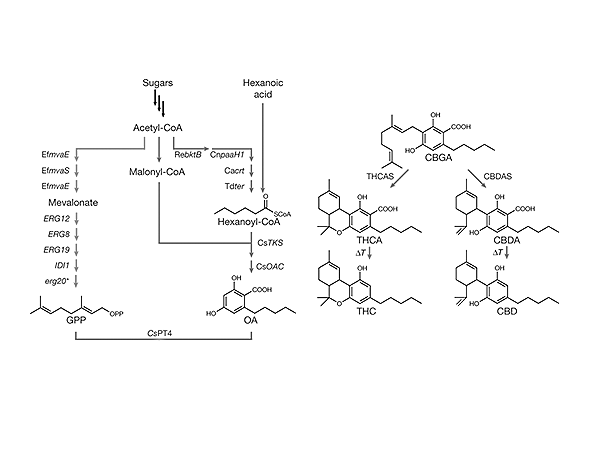
La cannabidivarina (CBDV) se origina a través de la vía biosintética de los cannabinoides varínicos, una ruta paralela a la de los cannabinoides pentílicos clásicos. La principal diferencia entre ambas radica en el precursor inicial: mientras que los cannabinoides como el CBD o el THC derivan del ácido olivetólico, los compuestos varínicos se sintetizan a partir de ácido divarinólico, lo que determina la presencia de una cadena lateral propilo en la estructura final (De Meijer et al., 2003; Taura et al., 2007).
Ruta biosintética varínica
La biosíntesis de CBDV sigue una secuencia enzimática análoga a la del CBD, pero utilizando precursores específicos:
- Ácido divarinólico
Se forma a partir de la vía policétida, empleando unidades de malonil-CoA en lugar de generar ácido olivetólico. - Formación de CBGVA (ácido cannabigerovarínico)
El ácido divarinólico se condensa con geranil pirofosfato (GPP) mediante una preniltransferasa, dando lugar al CBGVA, que actúa como precursor central de los cannabinoides varínicos. - Conversión en CBDVA
El CBGVA es transformado en ácido cannabidivarínico (CBDVA) por acción de enzimas sintasas específicas (CBDV-sintasas), en un proceso análogo a la conversión de CBGA en CBDA. - Descarboxilación a CBDV
Finalmente, el CBDVA sufre una descarboxilación (por calor, luz o envejecimiento), dando lugar a la forma neutra CBDV.
Esta ruta refleja un patrón biosintético conservado dentro del cannabis, donde pequeñas variaciones en los precursores conducen a familias completas de compuestos con propiedades diferenciadas (Taura et al., 2007; Gülck & Møller, 2020).
Localización en la planta
CBDV se sintetiza y acumula principalmente en los tricomas glandulares de la planta de Cannabis sativa L., estructuras especializadas responsables de la producción y almacenamiento de metabolitos secundarios lipofílicos.
Se localiza especialmente en:
- Tricomas capitados (cabeza glandular)
- Flores femeninas no polinizadas
- En menor medida, en hojas cercanas a las inflorescencias
La distribución de CBDV dentro de la planta sigue un patrón similar al de otros fitocannabinoides, aunque su concentración relativa suele ser considerablemente menor (Happyana et al., 2013).
Variabilidad según quimiotipo
La presencia de CBDV está fuertemente condicionada por el quimiotipo de la planta, es decir, por su perfil genético y bioquímico en cuanto a producción de cannabinoides.
CBDV se encuentra en mayor proporción en:
- Variedades ricas en cannabinoides no psicoactivos (tipo III)
- Landraces asiáticas y africanas
- Genéticas seleccionadas por perfiles varínicos
En la mayoría de las variedades comerciales modernas, dominadas por cannabinoides pentílicos, el contenido de CBDV es bajo o residual. Esto ha llevado al desarrollo de programas de mejora genética orientados a incrementar la producción de cannabinoides varínicos para fines de investigación (De Meijer et al., 2003).
Factores que afectan su biosíntesis
La producción de CBDV en la planta puede verse influida por múltiples factores:
- Genética: principal determinante del perfil cannabinoide
- Condiciones ambientales: luz, temperatura, estrés
- Estado de desarrollo de la planta
- Procesos postcosecha: secado, curado, almacenamiento
Estos factores pueden modificar tanto la cantidad de CBDVA producido como su conversión a CBDV, afectando el perfil final del extracto.
Relación con otros cannabinoides varínicos
CBDV forma parte de una red biosintética más amplia que incluye otros cannabinoides varínicos:
- THCV (tetrahidrocannabivarina)
- CBGV (cannabigerovarina)
Todos ellos comparten el mismo precursor central (CBGVA), lo que implica que la expresión diferencial de enzimas sintasas determina la proporción final de cada compuesto.
Este equilibrio enzimático dentro de la planta es clave para entender la diversidad química del cannabis y la coexistencia de múltiples perfiles cannabinoides dentro de una misma especie (Gülck & Møller, 2020).
La existencia de rutas biosintéticas paralelas basadas en ácido olivetólico y ácido divarinólico sugiere que la planta de cannabis posee una plasticidad metabólica considerable, capaz de generar familias completas de compuestos a partir de variaciones relativamente simples en los precursores. Esta capacidad biosintética es uno de los factores que explican la enorme diversidad química del cannabis y su interés en investigación farmacológica.
Interacción con el sistema endocannabinoide
La cannabidivarina (CBDV) presenta un perfil de interacción atípico dentro de los fitocannabinoides, caracterizado por una baja afinidad directa por los receptores cannabinoides clásicos CB1 y CB2. Esta característica la diferencia claramente de compuestos como el Δ9-tetrahidrocannabinol (THC), cuya actividad farmacológica está fuertemente mediada por la activación de CB1 en el sistema nervioso central (Pertwee, 2008; Cascio & Pertwee, 2014).
Diversos estudios han demostrado que CBDV no actúa como agonista significativo de CB1 ni CB2 a concentraciones fisiológicamente relevantes, lo que explica la ausencia de efectos psicoactivos y su perfil farmacológico diferenciado. En lugar de ello, su actividad se enmarca dentro de un modelo de modulación indirecta o no canónica del sistema endocannabinoide (Iannotti et al., 2014).
Interacción con receptores CB1 y CB2
La afinidad de CBDV por los receptores CB1 y CB2 es considerablemente baja en comparación con otros fitocannabinoides. Esto implica:
- Ausencia de activación directa significativa
- Baja probabilidad de efectos centrales mediados por CB1
- Interacción limitada con vías clásicas del sistema endocannabinoide
Algunos estudios sugieren que CBDV podría ejercer efectos moduladores indirectos, aunque estos mecanismos no están completamente definidos y podrían implicar cambios en la disponibilidad de endocannabinoides o en la señalización intracelular asociada (Pertwee, 2008).
Modulación del endocannabinoidome
Más allá del sistema endocannabinoide clásico, CBDV parece actuar dentro de un marco más amplio conocido como endocannabinoidome, que incluye:
- Receptores no cannabinoides
- Canales iónicos
- Enzimas metabólicas
- Lípidos señalizadores relacionados
En este contexto, CBDV se comporta como un modulador multimodal, capaz de influir en diferentes sistemas de señalización sin depender de una única diana dominante (Di Marzo & Piscitelli, 2015).
Interacción con canales TRP
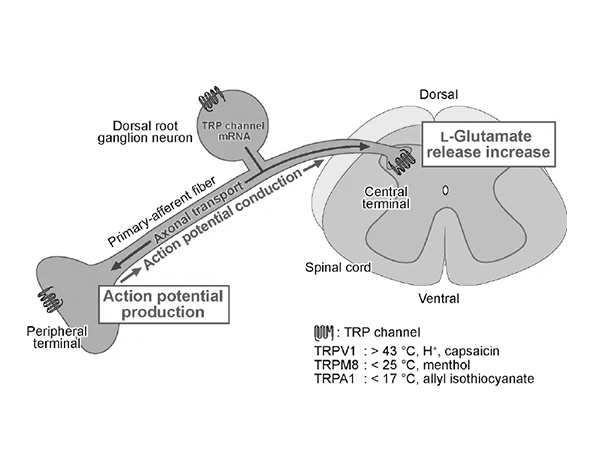
Uno de los aspectos más relevantes de la farmacología de CBDV es su interacción con canales de la familia TRP (Transient Receptor Potential), especialmente:
- TRPV1
- TRPV2
- TRPA1
Estos canales son proteínas transmembrana implicadas en la detección de estímulos físicos y químicos, incluyendo temperatura, pH y señales nociceptivas.
CBDV puede:
- Activar o modular estos canales
- Inducir cambios en la entrada de Ca²⁺
- Alterar la excitabilidad neuronal
Este mecanismo es particularmente relevante en sistemas neuronales donde la regulación del calcio intracelular desempeña un papel clave en la transmisión sináptica (Iannotti et al., 2014).
Regulación de la señalización neuronal
A través de su interacción con canales iónicos y otros elementos del endocannabinoidome, CBDV puede influir en:
- La liberación de neurotransmisores
- La plasticidad sináptica
- El equilibrio excitación/inhibición
Estos efectos no se producen mediante activación directa de receptores cannabinoides, sino a través de una modulación indirecta de redes de señalización neuronal, lo que sugiere un papel más sutil pero potencialmente relevante en la regulación del sistema nervioso.
Interacción con enzimas del sistema endocannabinoide
Aunque menos estudiado que en el caso del CBD, se ha propuesto que CBDV podría influir en enzimas implicadas en el metabolismo de endocannabinoides, como:
Sin embargo, la evidencia disponible es limitada y no permite establecer con claridad si CBDV actúa como inhibidor directo o si sus efectos son secundarios a otras interacciones moleculares (Iannotti et al., 2014).
Implicaciones funcionales
El perfil de interacción de CBDV sugiere un mecanismo de acción caracterizado por:
- Baja dependencia de CB1/CB2
- Alta implicación de canales iónicos
- Modulación indirecta de redes neuronales
- Actividad distribuida en múltiples dianas
Este tipo de comportamiento es coherente con la idea de que algunos fitocannabinoides actúan más como moduladores de sistemas complejos que como ligandos clásicos de un único receptor.
CBDV es un buen ejemplo de cómo el concepto de “cannabinoide” ha evolucionado desde una visión centrada en CB1/CB2 hacia un enfoque mucho más amplio. Su actividad fuera del eje clásico refleja la complejidad del sistema endocannabinoide expandido y pone de manifiesto la importancia de considerar múltiples niveles de regulación molecular al estudiar estos compuestos.
Farmacología
La cannabidivarina (CBDV) presenta un perfil farmacológico caracterizado por una actividad multimodal y una baja interacción directa con los receptores cannabinoides clásicos, lo que la sitúa dentro del grupo de fitocannabinoides no psicotrópicos con mecanismos de acción predominantemente no canónicos. A diferencia del Δ9-tetrahidrocannabinol (THC), cuya actividad se explica en gran medida por su acción agonista sobre CB1, CBDV ejerce sus efectos principalmente a través de la modulación de canales iónicos y otras dianas moleculares implicadas en la excitabilidad neuronal (Pertwee, 2008; Iannotti et al., 2014).
Uno de los ejes centrales de su farmacología es la interacción con canales de la familia TRP (Transient Receptor Potential). CBDV ha demostrado capacidad para activar o modular subtipos como TRPV1, TRPV2 y TRPA1, todos ellos implicados en la regulación del flujo de calcio intracelular y en la transducción de señales sensoriales. La activación o desensibilización de estos canales puede alterar la excitabilidad neuronal y modificar la liberación de neurotransmisores, lo que sitúa a CBDV como un modulador de la señalización neuronal dependiente de calcio (Iannotti et al., 2014; De Petrocellis et al., 2011).
En modelos preclínicos, esta modulación de canales TRP se ha asociado con una reducción de la hiperexcitabilidad neuronal, particularmente en contextos donde existe una alteración del equilibrio entre señales excitatorias e inhibitorias. Este efecto no depende de la activación de CB1, lo que sugiere la existencia de vías farmacológicas alternativas dentro del denominado endocannabinoidome (Hill et al., 2012).
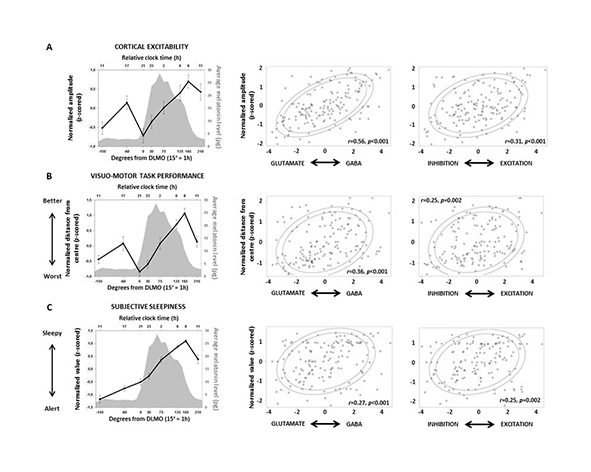
Además de su acción sobre canales iónicos, CBDV puede influir en la dinámica de neurotransmisores clave, como el glutamato y el GABA, contribuyendo a la regulación del equilibrio excitación/inhibición en redes neuronales. Esta propiedad es especialmente relevante en sistemas donde pequeñas alteraciones en la señalización sináptica pueden tener consecuencias funcionales amplificadas, como ocurre en diversos trastornos neurológicos (Zamberletti et al., 2019).
Desde el punto de vista intracelular, CBDV se ha relacionado con la modulación de vías dependientes de calcio y con la activación de cascadas de señalización que incluyen proteínas quinasas y otros mediadores secundarios. Estos efectos sugieren que su acción no se limita a la membrana celular, sino que se extiende a la regulación de procesos intracelulares complejos que afectan a la función neuronal global (Iannotti et al., 2014).
En cuanto a su interacción con enzimas del sistema endocannabinoide, la evidencia disponible es aún limitada. Algunos estudios han planteado la posibilidad de que CBDV pueda influir indirectamente en la actividad de enzimas como FAAH o MAGL, aunque no se ha establecido un papel claro como inhibidor directo, a diferencia de lo observado con otros fitocannabinoides como el CBD (Pertwee, 2008).
Desde una perspectiva farmacodinámica global, CBDV puede considerarse un compuesto con un mecanismo de acción distribuido, donde la suma de interacciones de baja intensidad sobre múltiples dianas genera un efecto modulador sobre sistemas biológicos complejos. Este patrón contrasta con el de ligandos clásicos altamente selectivos y refuerza la idea de que ciertos fitocannabinoides actúan como reguladores finos de la homeostasis neuronal.
En términos de seguridad, los estudios preclínicos disponibles sugieren que CBDV presenta un perfil favorable, sin evidencias de efectos psicoactivos ni de alteraciones conductuales significativas asociadas a la activación de CB1. No obstante, la evidencia clínica en humanos sigue siendo limitada, por lo que su caracterización farmacológica completa requiere aún de estudios adicionales bien controlados.
En conjunto, la farmacología de CBDV refleja una transición conceptual dentro del estudio de los cannabinoides, pasando de un modelo centrado en receptores específicos a un enfoque más amplio basado en la modulación de redes de señalización interconectadas, donde canales iónicos, neurotransmisores y vías intracelulares desempeñan un papel central.
Mecanismos moleculares
La cannabidivarina (CBDV) ejerce sus efectos a través de un conjunto de mecanismos moleculares que reflejan un patrón de modulación distribuida, en el que no existe una única diana dominante, sino una interacción coordinada con múltiples sistemas de señalización celular. Este comportamiento es característico de varios fitocannabinoides no psicotrópicos y se aleja del modelo clásico de ligando-receptor altamente selectivo (Iannotti et al., 2014; Zamberletti et al., 2019).
Uno de los mecanismos centrales de CBDV es la modulación de canales iónicos dependientes de potencial y ligando, especialmente aquellos pertenecientes a la familia TRP. La interacción con canales como TRPV1, TRPV2 y TRPA1 permite regular el flujo de Ca²⁺ hacia el interior celular, lo que constituye una señal clave en múltiples procesos neuronales. La activación inicial de estos canales puede ir seguida de fenómenos de desensibilización, reduciendo la respuesta celular ante estímulos posteriores y contribuyendo a la estabilización de la excitabilidad neuronal (De Petrocellis et al., 2011; Iannotti et al., 2014).
La entrada de calcio intracelular inducida por la activación de canales TRP desencadena una serie de cascadas de señalización intracelular, incluyendo la activación de proteínas quinasas como PKC y MAPK. Estas vías regulan la expresión génica, la plasticidad sináptica y la adaptación celular frente a estímulos persistentes. En este contexto, CBDV puede influir indirectamente en procesos de remodelación neuronal y en la respuesta adaptativa del sistema nervioso (Zamberletti et al., 2019).
Otro aspecto relevante es la capacidad de CBDV para modular el equilibrio entre neurotransmisión excitatoria e inhibitoria. A través de la regulación del calcio intracelular y de la actividad de canales iónicos, CBDV puede influir en la liberación de neurotransmisores como el glutamato (excitador) y el GABA (inhibidor). Este equilibrio es fundamental para el funcionamiento normal de las redes neuronales, y su alteración está implicada en múltiples condiciones neurológicas (Hill et al., 2012).
A nivel sináptico, CBDV puede actuar como modulador de la plasticidad neuronal, afectando procesos como la potenciación a largo plazo (LTP) y la depresión a largo plazo (LTD). Aunque estos efectos no han sido completamente caracterizados, se ha propuesto que la regulación del calcio intracelular y de las vías de señalización asociadas desempeña un papel clave en estos fenómenos (Iannotti et al., 2014).
Además, CBDV podría interactuar indirectamente con el sistema endocannabinoide mediante la modulación de la disponibilidad o el metabolismo de endocannabinoides, aunque este aspecto sigue siendo objeto de investigación. La ausencia de una acción directa significativa sobre CB1 y CB2 sugiere que estos efectos, de existir, se producirían a través de mecanismos secundarios o de interacción con enzimas metabólicas (Pertwee, 2008).
Desde una perspectiva más amplia, los mecanismos moleculares de CBDV pueden entenderse como parte de un sistema de regulación en el que múltiples señales convergen para ajustar la actividad celular. Este tipo de modulación es especialmente relevante en sistemas complejos como el sistema nervioso, donde pequeñas variaciones en la señalización pueden tener efectos amplificados a nivel funcional.
En conjunto, CBDV actúa como un modulador de la señalización celular dependiente de calcio, integrando la actividad de canales iónicos, vías intracelulares y procesos sinápticos. Este perfil refuerza la idea de que algunos fitocannabinoides no funcionan como interruptores binarios, sino como reguladores finos de sistemas biológicos dinámicos.
Importancia en la investigación científica
La cannabidivarina (CBDV) ha adquirido relevancia en investigación biomédica como consecuencia de su perfil farmacológico diferenciado, caracterizado por la ausencia de efectos psicotrópicos y por su capacidad para modular sistemas neuronales a través de mecanismos no dependientes de los receptores cannabinoides clásicos. Este conjunto de propiedades la sitúa como un compuesto de interés en el estudio de la señalización neuronal y de los trastornos asociados a alteraciones en la excitabilidad y la plasticidad sináptica (Iannotti et al., 2014; Zamberletti et al., 2019).
Uno de los principales ámbitos en los que se ha investigado CBDV es el de los trastornos neurológicos, particularmente aquellos en los que existe una disfunción en el equilibrio entre excitación e inhibición neuronal. En modelos preclínicos, CBDV ha mostrado capacidad para modular la actividad neuronal a través de la regulación del calcio intracelular y la interacción con canales iónicos, lo que ha motivado su estudio en contextos como la epilepsia. Estos efectos no se producen mediante la activación de CB1, lo que representa una vía alternativa de intervención dentro del estudio de los cannabinoides (Hill et al., 2012).
Otro campo de interés es el de los trastornos del neurodesarrollo, donde se ha explorado el impacto de CBDV sobre comportamientos relacionados con la función sináptica y la conectividad neuronal. Algunos estudios experimentales han analizado su influencia en conductas repetitivas y en el procesamiento sensorial, sugiriendo que la modulación de canales iónicos y de la señalización intracelular podría desempeñar un papel en estos procesos (Zamberletti et al., 2019).
Desde una perspectiva más amplia, CBDV contribuye a la expansión del marco conceptual del sistema endocannabinoide hacia el denominado endocannabinoidome, en el que múltiples receptores, canales iónicos y mediadores lipídicos interactúan de forma integrada. Su actividad fuera de los ejes CB1/CB2 ha sido especialmente relevante para comprender que los fitocannabinoides pueden ejercer efectos biológicos significativos sin actuar como agonistas directos de estos receptores, lo que ha abierto nuevas líneas de investigación en farmacología (Di Marzo & Piscitelli, 2015).
Además, CBDV representa un modelo útil para estudiar la relación estructura-actividad (SAR) dentro de los cannabinoides. La comparación entre compuestos pentílicos y varínicos ha permitido identificar cómo modificaciones estructurales relativamente pequeñas pueden traducirse en cambios relevantes en la afinidad por receptores y en los mecanismos de acción. Este enfoque ha sido clave para entender la diversidad funcional del fitocomplejo del cannabis y para orientar el desarrollo de nuevos compuestos con perfiles farmacológicos específicos (Citti et al., 2018).
En el ámbito de la investigación traslacional, CBDV ha despertado interés debido a su perfil de seguridad observado en estudios preclínicos y a la ausencia de efectos psicoactivos, lo que facilita su evaluación en modelos experimentales sin las limitaciones asociadas a cannabinoides con actividad central marcada. No obstante, la evidencia clínica en humanos sigue siendo limitada, y gran parte del conocimiento disponible procede de estudios in vitro o en modelos animales, lo que requiere una interpretación cautelosa de sus posibles aplicaciones (Iannotti et al., 2014).
En conjunto, la importancia de CBDV en investigación no reside únicamente en sus posibles efectos biológicos, sino en su capacidad para cuestionar y ampliar los modelos clásicos de acción de los cannabinoides. Su estudio ha contribuido a una comprensión más compleja y matizada de la señalización endocannabinoide y de la interacción entre compuestos vegetales y sistemas biológicos, consolidándose como una pieza relevante dentro del análisis científico del cannabis.
Referencias
– Mechoulam, R., & Gaoni, Y. (1965). A total synthesis of dl-Δ1-tetrahydrocannabinol. Journal of the
American Chemical Society, 87(14), 3273–3275.
– Mechoulam, R., & Hanus, L. (2000). A historical overview of chemical research on cannabinoids.
Chemistry and Physics of Lipids, 108(1–2), 1–13.
– Pertwee, R. G. (2008). The diverse CB1 and CB2 receptor pharmacology of cannabinoids. British Journal
of Pharmacology, 153(2), 199–215.
– Cascio, M. G., & Pertwee, R. G. (2014). Known pharmacological actions of Δ9-tetrahydrocannabinol and
of four other chemical constituents of cannabis. British Journal of Pharmacology, 171(14), 3256–3270.
– De Meijer, E. P. M., Hammond, K. M., & Micheler, M. (2003). The inheritance of chemical phenotype
in Cannabis sativa L. Genetics, 163(1), 335–346.
– Taura, F., Sirikantaramas, S., Shoyama, Y., Yoshikai, K., Shoyama, Y., & Morimoto, S. (2007). Cannabidiolic-acid
synthase, the chemotype-determining enzyme in the fiber-type Cannabis sativa. FEBS Letters, 581(16), 2929–2934.
– De Petrocellis, L., Ligresti, A., Schiano Moriello, A., Allarà, M., Bisogno, T., Petrosino, S., Stott, C. G., &
Di Marzo, V. (2011). Effects of cannabinoids and cannabinoid-enriched extracts on TRP channels and endocannabinoid
metabolic enzymes. British Journal of Pharmacology, 163(7), 1479–1494.
– Iannotti, F. A., Hill, C. L., Leo, A., Alhusaini, A., Soubrane, C., Mazzarella, E., Russo, E. B., Whalley, B. J.,
& Di Marzo, V. (2014). Nonpsychotropic plant cannabinoids: new therapeutic opportunities from an ancient herb.
Neurotherapeutics, 11(4), 735–746.
– Hill, T. D. M., Cascio, M. G., Romano, B., Duncan, M., Pertwee, R. G., Williams, C. M., & Whalley, B. J. (2012).
Cannabidivarin is anticonvulsant in mouse and rat. British Journal of Pharmacology, 167(8), 1629–1642.
– Zamberletti, E., Gabaglio, M., & Parolaro, D. (2019). The endocannabinoid system and autism spectrum disorders:
Insights from animal models. Frontiers in Neuroscience, 13, 1264.
– Di Marzo, V., & Piscitelli, F. (2015). The endocannabinoid system and its modulation by phytocannabinoids.
Neurotherapeutics, 12(4), 692–698.
– Citti, C., Linciano, P., Panseri, S., Vezzalini, F., Forni, F., Vandelli, M. A., & Cannazza, G. (2018). Cannabinoid
profiling of hemp seed oil by LC-MS/MS. Journal of Pharmaceutical and Biomedical Analysis, 150, 208–215.
– Gülck, T., & Møller, B. L. (2020). Phytocannabinoids: Origins and biosynthesis. Trends in Plant Science, 25(10), 985–1004.