Introducción
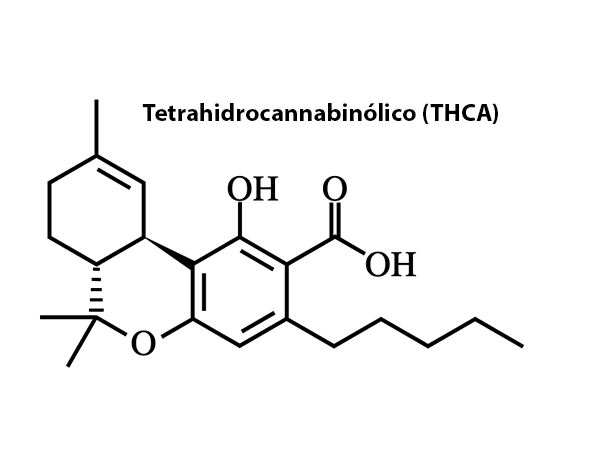
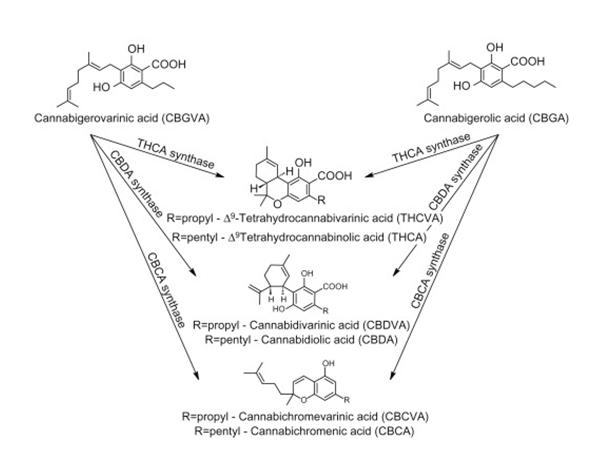
El ácido tetrahidrocannabinólico (THCA) es el principal fitocannabinoide ácido sintetizado en la planta de Cannabis sativa L. y constituye la forma biosintética predominante del Δ⁹-tetrahidrocannabinol (THC) en tejido vegetal fresco. Desde una perspectiva bioquímica, el THCA se origina a partir del ácido cannabigerólico (CBGA) mediante la acción de la enzima THCA sintasa, una oxidociclasa dependiente de FAD que cataliza una reacción clave en la diversificación química de los cannabinoides (Taura et al., 1996; Sirikantaramas et al., 2004).
Los fitocannabinoides como el THCA pertenecen a la familia de los meroterpenoides, compuestos híbridos que integran rutas biosintéticas de origen policétido y terpénico. En este contexto, la formación del THCA refleja la convergencia entre el ácido olivetólico y el geranil pirofosfato, dando lugar a una estructura compleja que combina propiedades fenólicas y terpénicas. Esta dualidad estructural es fundamental para entender tanto su comportamiento químico como su interacción con sistemas biológicos (Gülck & Møller, 2020).
A diferencia del THC, el THCA presenta un grupo carboxilo (-COOH) que define su naturaleza como cannabinoide ácido y condiciona profundamente sus propiedades fisicoquímicas. Este grupo funcional incrementa su polaridad relativa, reduce su lipofilicidad y limita su capacidad para atravesar membranas biológicas, incluyendo la barrera hematoencefálica. Como consecuencia, el THCA carece de efectos psicoactivos en condiciones fisiológicas normales, debido en parte a su baja afinidad por los receptores cannabinoides CB1 (Pertwee, 2008; Moreno-Sanz, 2016).
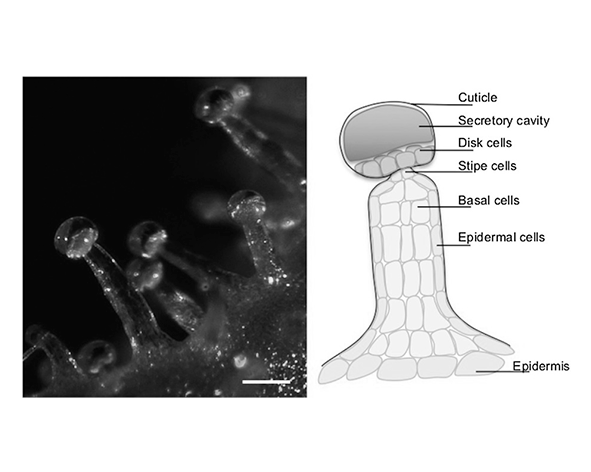
En la planta, el THCA se acumula en los tricomas glandulares, estructuras especializadas en la biosíntesis y almacenamiento de metabolitos secundarios. Estas estructuras actúan como microreactores bioquímicos donde se sintetizan y concentran cannabinoides, terpenos y otros compuestos, formando un sistema químico altamente organizado y regulado (Happyana et al., 2013; Livingston et al., 2020).
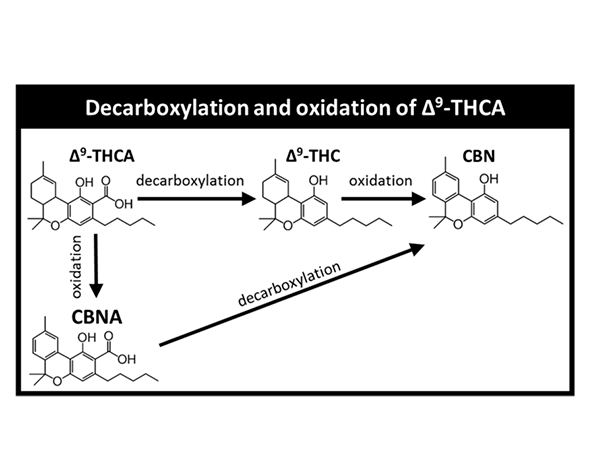
Una característica clave del THCA es su inestabilidad térmica, ya que puede transformarse en THC mediante un proceso de descarboxilación que implica la pérdida de dióxido de carbono (CO₂). Este proceso puede ser inducido por calor, radiación ultravioleta o envejecimiento, y representa un cambio estructural aparentemente simple pero con profundas implicaciones farmacológicas, al generar una molécula con mayor lipofilicidad y afinidad por receptores cannabinoides (Dussy et al., 2005).
Desde un punto de vista farmacológico, el THCA ha sido tradicionalmente considerado un precursor inactivo del THC. Sin embargo, investigaciones más recientes han puesto de manifiesto que el THCA posee un perfil de interacción molecular propio, caracterizado por una actividad limitada sobre receptores cannabinoides clásicos y una posible implicación en dianas alternativas como canales TRP o receptores nucleares. Este cambio de perspectiva ha ampliado el interés científico en los cannabinoides ácidos como entidades bioquímicas independientes (De Petrocellis et al., 2011; Nadal et al., 2017).
En conjunto, el THCA representa un compuesto clave tanto en la bioquímica del cannabis como en la investigación contemporánea sobre cannabinoides, actuando como nexo entre la química vegetal, la farmacología y los mecanismos moleculares del sistema endocannabinoide.
Historia del descubrimiento
El estudio del THCA se enmarca dentro del desarrollo de la química de los cannabinoides durante el siglo XX, cuando los primeros trabajos comenzaron a aislar y caracterizar los compuestos presentes en Cannabis sativa. Aunque inicialmente se asumió que el Δ⁹-tetrahidrocannabinol (THC) era el principal componente activo de la planta, investigaciones posteriores revelaron que en el material vegetal fresco predominan las formas ácidas, siendo el THCA el principal fitocannabinoide en variedades ricas en THC (Mechoulam, 1964; ElSohly & Slade, 2005).
Durante las décadas de 1960 y 1970, los avances en técnicas de cromatografía y espectrometría permitieron diferenciar entre cannabinoides neutros y sus precursores ácidos. En este contexto, se estableció que el THC no se encuentra en cantidades significativas en la planta intacta, sino que se genera a partir del THCA mediante procesos de descarboxilación inducidos por calor o envejecimiento, lo que supuso un cambio conceptual en la comprensión de la química del cannabis (Mechoulam, 1970; Dussy et al., 2005).
El avance clave en la comprensión del THCA tuvo lugar en la década de 1990, cuando se identificaron las enzimas responsables de la biosíntesis de cannabinoides. En particular, los trabajos de Taura y colaboradores permitieron aislar y caracterizar la THCA sintasa, demostrando que el THCA se forma enzimáticamente a partir de CBGA mediante una reacción oxidativa específica, consolidando el modelo biosintético actual (Taura et al., 1996).
Posteriormente, estudios estructurales y moleculares profundizaron en la caracterización de la THCA sintasa, incluyendo su estructura tridimensional, su mecanismo catalítico y su expresión específica en los tricomas glandulares. Estos hallazgos permitieron integrar la biosíntesis de cannabinoides dentro del metabolismo secundario de la planta, estableciendo una base sólida para la investigación moderna en fitocannabinoides (Sirikantaramas et al., 2004).
En paralelo, el desarrollo del concepto de sistema endocannabinoide en la década de 1990, con el descubrimiento de receptores cannabinoides y ligandos endógenos, abrió nuevas líneas de investigación sobre la interacción de los fitocannabinoides con sistemas biológicos. En este contexto, el THCA pasó de ser considerado un precursor inactivo a un compuesto con potencial interés propio dentro de la investigación básica (Di Marzo et al., 1998; Pertwee, 2008).
En conjunto, la historia del THCA refleja la evolución del conocimiento sobre el cannabis, desde una visión centrada en compuestos aislados hacia una comprensión más compleja de sus rutas biosintéticas y su diversidad química, consolidando su papel como uno de los principales metabolitos primarios de la planta.
Estructura o componentes
El THCA es un fitocannabinoide ácido perteneciente a la familia de los meroterpenoides, cuya estructura resulta de la condensación entre el ácido olivetólico y el geranil pirofosfato, seguida de una ciclación enzimática que da lugar a su esqueleto característico. Este origen biosintético híbrido explica la presencia simultánea de dominios fenólicos y terpénicos en su estructura molecular (Gülck & Møller, 2020).
A nivel químico, el THCA presenta una fórmula molecular C₂₂H₃₀O₄ y una arquitectura basada en un núcleo tricíclico tipo dibenzopirano modificado, característico de los fitocannabinoides derivados del THC. Este núcleo está formado por un sistema aromático fusionado con un anillo terpénico, lo que confiere rigidez estructural y una conformación tridimensional definida (Mechoulam, 1964; Pertwee, 2008).
Uno de los elementos estructurales más relevantes es la cadena lateral pentílica (C5), que se extiende desde el anillo aromático y desempeña un papel clave en la interacción con dianas biológicas. La longitud y naturaleza de esta cadena han demostrado ser determinantes en la afinidad por receptores cannabinoides en otros fitocannabinoides, lo que sugiere un papel estructural conservado en el THCA (Pertwee, 2008).
El rasgo diferencial del THCA respecto al THC es la presencia de un grupo carboxilo (-COOH) unido al anillo fenólico. Este grupo funcional introduce una serie de modificaciones fisicoquímicas relevantes, incluyendo un aumento de la polaridad, una menor lipofilicidad y una mayor capacidad de formar enlaces de hidrógeno. Estas propiedades afectan directamente a su solubilidad, estabilidad y comportamiento en sistemas biológicos (Moreno-Sanz, 2016).
Desde el punto de vista estereoquímico, el THCA presenta varios centros quirales que determinan su configuración tridimensional. Esta conformación influye en su capacidad de interacción con proteínas, especialmente en comparación con el THC, cuya estructura más lipofílica y compacta facilita el acoplamiento con receptores CB1. En el caso del THCA, la presencia del grupo carboxilo genera impedimentos estéricos que limitan este tipo de interacciones (Pertwee, 2008).
El proceso de descarboxilación constituye una transformación estructural clave en el THCA. Este proceso implica la pérdida de un grupo carboxilo en forma de dióxido de carbono (CO₂), dando lugar a la formación de THC. Aunque químicamente se trata de una modificación puntual, el cambio resultante altera significativamente las propiedades farmacológicas de la molécula, incrementando su lipofilicidad y su capacidad de atravesar la barrera hematoencefálica (Dussy et al., 2005).
Además, el THCA presenta una estabilidad limitada frente a factores ambientales como temperatura, luz y oxidación. Estas condiciones pueden inducir tanto su descarboxilación como procesos de degradación adicionales, lo que afecta a su integridad estructural y a su proporción relativa en muestras de cannabis en función del tiempo y las condiciones de almacenamiento (Pellati et al., 2018).
En conjunto, la estructura del THCA representa un equilibrio entre complejidad química y funcionalidad biológica, donde pequeñas modificaciones, como la presencia o ausencia de un grupo carboxilo, determinan diferencias profundas en su comportamiento farmacológico y su interacción con el organismo.
Mecanismos moleculares
El THCA presenta un perfil de interacción molecular complejo que difiere significativamente del THC, caracterizado por una actividad limitada sobre los receptores cannabinoides clásicos y una mayor implicación en dianas no canónicas. Esta diferencia está directamente relacionada con la presencia del grupo carboxilo, que condiciona tanto su conformación como su capacidad de interacción con proteínas de membrana (Pertwee, 2008).
En relación con los receptores CB1 y CB2, el THCA muestra una afinidad significativamente reducida, lo que limita su capacidad para actuar como agonista directo de estos GPCR. Esta baja afinidad se traduce en una actividad funcional débil o prácticamente ausente en comparación con el THC, especialmente en el sistema nervioso central (Pertwee, 2008; Moreno-Sanz, 2016).
Sin embargo, el THCA ha mostrado actividad sobre canales TRP, particularmente TRPV1 y TRPA1, implicados en la transducción sensorial y la regulación de la homeostasis celular. Estas interacciones sugieren un papel potencial en la modulación de señales intracelulares dependientes de calcio, aunque su relevancia fisiológica sigue siendo objeto de estudio (De Petrocellis et al., 2011).
Además, se ha descrito que el THCA puede interactuar con receptores nucleares como PPARγ, lo que implicaría una posible capacidad de regulación transcripcional. Este tipo de interacción sitúa al THCA dentro de un grupo de compuestos capaces de influir en procesos metabólicos y de expresión génica, aunque los mecanismos exactos aún no están completamente definidos (Nadal et al., 2017).
Algunos estudios también han sugerido una posible interacción indirecta con enzimas como la ciclooxigenasa (COX) y otras vías inflamatorias, lo que podría indicar un papel modulador en cascadas bioquímicas celulares. No obstante, estos efectos se han observado principalmente en modelos experimentales y requieren validación adicional (Rock et al., 2013).
En conjunto, el THCA se comporta más como un modulador molecular multifuncional que como un agonista cannabinoide clásico, interactuando con diversas dianas en función del contexto celular y experimental. Este perfil lo diferencia claramente del THC y lo posiciona como un compuesto de interés en la investigación básica del sistema endocannabinoide (Moreno-Sanz, 2016).
Distribución o contexto fisiológico
El THCA se encuentra predominantemente en la planta de Cannabis sativa L., donde se sintetiza y acumula en los tricomas glandulares, estructuras epidérmicas especializadas responsables de la producción de metabolitos secundarios como cannabinoides y terpenos. Estas estructuras presentan una alta actividad biosintética y concentran el THCA en niveles significativamente superiores a los observados en otras partes de la planta, como hojas o tallos (Happyana et al., 2013; Livingston et al., 2020).
La distribución del THCA en la planta es heterogénea y está influenciada por factores genéticos, ambientales y de desarrollo. Las inflorescencias femeninas maduras presentan las mayores concentraciones, lo que refleja tanto la densidad de tricomas como la actividad enzimática de la THCA sintasa en estas regiones. Esta localización específica se ha relacionado con funciones ecológicas como la protección frente a radiación ultravioleta, herbívoros y estrés ambiental (Russo, 2011; Andre et al., 2016).
En el contexto biológico humano, el THCA no se produce de forma endógena, por lo que su presencia depende exclusivamente de la exposición externa. Una vez introducido en el organismo, su comportamiento farmacocinético está condicionado por sus propiedades fisicoquímicas, especialmente su menor lipofilicidad en comparación con el THC y su mayor polaridad relativa (Pertwee, 2008).
Tras su administración, el THCA presenta una absorción limitada en comparación con cannabinoides neutros, debido a su menor capacidad para atravesar membranas biológicas por difusión pasiva. Este factor condiciona su biodisponibilidad y su distribución tisular, favoreciendo una mayor presencia en compartimentos periféricos frente al sistema nervioso central (Moreno-Sanz, 2016).
La distribución sistémica del THCA parece restringida por su dificultad para cruzar la barrera hematoencefálica, lo que limita su acceso al cerebro y explica en parte su ausencia de efectos psicoactivos. Como resultado, su actividad se ha asociado principalmente a tejidos periféricos, aunque los datos en humanos siguen siendo escasos (Pellati et al., 2018).
En términos de metabolismo, el THCA puede experimentar procesos de descarboxilación in vivo o ex vivo, dependiendo de condiciones como temperatura, pH o tiempo. Este fenómeno introduce una variable importante en su estudio, ya que parte del THCA administrado puede convertirse en THC, alterando el perfil farmacológico observado (Dussy et al., 2005).
Asimismo, el THCA presenta una estabilidad limitada, siendo susceptible a degradación térmica, oxidativa y fotoquímica. Estas transformaciones afectan a su integridad estructural y a su proporción relativa en matrices biológicas o vegetales, lo que debe tenerse en cuenta en estudios experimentales y análisis analíticos (Pellati et al., 2018).
En conjunto, la distribución del THCA está determinada por un equilibrio entre su origen vegetal, sus propiedades fisicoquímicas y su comportamiento dinámico en sistemas biológicos, configurando un perfil distinto al de cannabinoides neutros como el THC.
Interacción con fitocannabinoides
El THCA forma parte del conjunto de fitocannabinoides presentes en Cannabis sativa, donde coexiste con compuestos como el Δ⁹-tetrahidrocannabinol (THC), el cannabidiol (CBD) y otros cannabinoides menores. Esta coexistencia configura un entorno químico complejo en el que múltiples moléculas pueden interactuar de forma simultánea, aunque en el caso del THCA estas interacciones han sido menos estudiadas en comparación con cannabinoides neutros (Russo, 2011; Pertwee, 2008).
Desde un punto de vista biosintético, la relación entre THCA y THC es directa, ya que el THC se genera mediante la descarboxilación del THCA. Este vínculo convierte al THCA en un precursor clave dentro del perfil químico del cannabis, determinando en gran medida la cantidad potencial de THC que puede formarse en función de variables como temperatura, tiempo y condiciones de almacenamiento (Taura et al., 1996; Dussy et al., 2005).
En sistemas experimentales, se ha planteado que el THCA podría influir en la actividad de otros fitocannabinoides a través de interacciones indirectas, como la modulación del entorno lipídico de membranas celulares o la competencia por dianas moleculares compartidas. Sin embargo, estos efectos no están claramente definidos y su relevancia fisiológica sigue siendo objeto de investigación (Moreno-Sanz, 2016; Nadal et al., 2017).
En relación con el denominado “efecto séquito”, el THCA ha sido incluido en ocasiones dentro de modelos teóricos que proponen una acción sinérgica entre cannabinoides y otros compuestos de la planta, como terpenos y flavonoides. No obstante, la evidencia científica que respalda estas interacciones específicas es limitada y, en muchos casos, se basa en extrapolaciones o modelos preclínicos que no permiten establecer conclusiones robustas (Russo, 2019).
Además, la presencia del grupo carboxilo en el THCA introduce diferencias fisicoquímicas que pueden alterar su comportamiento en sistemas mixtos de cannabinoides, incluyendo su solubilidad, estabilidad y afinidad por diferentes compartimentos celulares. Estas características podrían influir en la dinámica de interacción con otros compuestos, aunque este aspecto ha sido poco explorado en la literatura científica (Pellati et al., 2018).
En conjunto, la interacción del THCA con otros fitocannabinoides debe entenderse dentro de un marco de complejidad química y evidencia limitada, donde las posibles sinergias o modulaciones aún no están completamente caracterizadas. Este enfoque crítico es especialmente relevante en el contexto de la interpretación científica del cannabis, evitando simplificaciones excesivas sobre interacciones que aún no han sido plenamente demostradas.
Importancia en investigación biomédica
El THCA ha despertado interés en la investigación biomédica debido a su perfil farmacológico diferenciado respecto al THC, especialmente por su ausencia de efectos psicoactivos y su posible interacción con múltiples dianas moleculares. Este interés se ha centrado principalmente en estudios preclínicos que exploran su comportamiento en modelos celulares y animales (Pertwee, 2008; Moreno-Sanz, 2016).
Diversas investigaciones han sugerido que el THCA podría participar en la modulación de procesos biológicos como la inflamación, la señalización neuronal o la homeostasis celular. Estos efectos se han observado en modelos experimentales donde el THCA interactúa con canales iónicos, receptores nucleares y vías de señalización intracelular, aunque sin una caracterización completa de sus mecanismos (Nadal et al., 2017; Rock et al., 2013).
En el ámbito neurobiológico, el THCA ha sido estudiado en relación con su posible influencia sobre la excitabilidad neuronal y la señalización sináptica, particularmente a través de su interacción con canales TRP. Sin embargo, estos hallazgos se limitan a modelos experimentales y no permiten establecer conclusiones definitivas sobre su relevancia fisiológica en humanos (De Petrocellis et al., 2011).
Asimismo, el THCA ha sido objeto de interés en estudios relacionados con metabolismo y regulación génica, debido a su posible interacción con receptores como PPARγ. Estas observaciones apuntan a un papel potencial en la modulación de procesos celulares complejos, aunque la evidencia disponible sigue siendo preliminar (Nadal et al., 2017).
En conjunto, el THCA representa un compuesto de interés en la investigación básica sobre cannabinoides, especialmente por su perfil no psicoactivo y su diversidad de interacciones moleculares. No obstante, la mayor parte de la evidencia procede de estudios preclínicos, por lo que su relevancia en contextos fisiológicos humanos aún requiere una validación más amplia y rigurosa.
Referencias
- Taura F, Morimoto S, Shoyama Y. (1996). Purification and characterization of cannabidiolic-acid synthase from Cannabis sativa L. Journal of Biological Chemistry. - Sirikantaramas S, Taura F, Tanaka Y, Ishikawa Y, Morimoto S, Shoyama Y. (2004). Tetrahydrocannabinolic acid synthase, the enzyme controlling marijuana psychoactivity. Journal of Biological Chemistry. - Gülck T, Møller BL. (2020). Phytocannabinoids: Origins and biosynthesis. Trends in Plant Science. - Mechoulam R, Gaoni Y. (1964). Isolation, structure, and partial synthesis of an active constituent of hashish. Journal of the American Chemical Society. - Pertwee RG. (2008). The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids: Δ9-tetrahydrocannabinol, cannabidiol and Δ9-tetrahydrocannabivarin. British Journal of Pharmacology. - Dussy FE, Hamberg C, Luginbühl M, Schwerzmann T, Briellmann TA. (2005). Isolation of Δ9-THCA-A from hemp and analytical aspects concerning the determination of Δ9-THC in cannabis products. Forensic Science International. - Happyana N, Agnolet S, Muntendam R, van Dam A, Schneider B, Kayser O. (2013). Analysis of cannabinoids in laser-microdissected trichomes of medicinal cannabis. Analytical and Bioanalytical Chemistry. - Livingston SJ, Quilichini TD, Booth JK, Wong DCJ, Rensing KH, Laflamme-Yonkman J, Bohlmann J, Page JE, Samuels AL. (2020). Cannabis glandular trichomes alter morphology and metabolite content during flower maturation. The Plant Journal. - Andre CM, Hausman JF, Guerriero G. (2016). Cannabis sativa: The plant of the thousand and one molecules. Frontiers in Plant Science. - Moreno-Sanz G. (2016). Can you pass the acid test? Critical review and novel therapeutic perspectives of Δ9-tetrahydrocannabinolic acid A. Cannabis and Cannabinoid Research. - Pellati F, Brighenti V, Sperlea J, Marchetti L, Bertelli D, Benvenuti S. (2018). New methods for the analysis of cannabinoids in cannabis products. Journal of Pharmaceutical and Biomedical Analysis. - De Petrocellis L, Ligresti A, Moriello AS, Allarà M, Bisogno T, Petrosino S, Stott CG, Di Marzo V. (2011). Effects of cannabinoids and cannabinoid-enriched cannabis extracts on TRP channels. British Journal of Pharmacology. - Nadal X, Del Río C, Casano S, Palomares B, Ferreiro-Vera C, Navarrete C, Sánchez-Carnerero C, Cantarero I, Bellido ML, Meyer S, et al. (2017). Tetrahydrocannabinolic acid is a potent PPARγ agonist. Biochemical Pharmacology. - Rock EM, Bolognini D, Limebeer CL, Cascio MG, Anavi-Goffer S, Fletcher PJ, Mechoulam R, Pertwee RG, Parker LA. (2013). Cannabinoid receptor-independent effects of Δ9-THCA. British Journal of Pharmacology. - Russo EB. (2011). Taming THC: Potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. British Journal of Pharmacology. - Russo EB. (2019). The case for the entourage effect and conventional breeding of clinical cannabis. Frontiers in Plant Science. - Di Marzo V, Fontana A, Cadas H, Schinelli S, Cimino G, Schwartz JC, Piomelli D. (1994). Formation and inactivation of endogenous cannabinoid anandamide. Nature.