Introducción
El PPARα (Peroxisome Proliferator-Activated Receptor Alpha) es un receptor nuclear que actúa como factor de transcripción dependiente de ligando y forma parte de la familia de los receptores activados por proliferadores de peroxisomas (PPARs). Se expresa de manera predominante en tejidos con elevada capacidad oxidativa, como el hígado, el corazón, el músculo esquelético y el riñón, donde desempeña un papel central en la regulación del metabolismo energético basado en lípidos (Kersten, 2014; Pawlak et al., 2015).
Desde una perspectiva funcional, PPARα puede entenderse como un sensor intracelular de disponibilidad lipídica. Su activación se produce en respuesta a la unión de ácidos grasos y sus derivados, lo que refleja cambios en el estado metabólico celular. Una vez activado, forma un heterodímero con el receptor RXR (Retinoid X Receptor) y se une a secuencias específicas del ADN denominadas PPRE (Peroxisome Proliferator Response Elements), regulando la expresión de genes implicados en la captación, transporte y oxidación de ácidos grasos (Evans et al., 2004; Kersten, 2014).
Este receptor adquiere especial relevancia en condiciones de ayuno o demanda energética elevada, donde facilita el cambio metabólico desde el uso de glucosa hacia la oxidación de ácidos grasos. A través de este mecanismo, PPARα promueve procesos como la β-oxidación mitocondrial y peroxisomal, así como la cetogénesis hepática, contribuyendo al mantenimiento de la homeostasis energética sistémica (Pawlak et al., 2015).
Además de su papel metabólico, PPARα también participa en la modulación de procesos inflamatorios, lo que amplía su relevancia más allá del metabolismo energético y lo posiciona como un nodo integrador entre metabolismo y señalización celular. En conjunto, su actividad refleja una adaptación transcripcional coordinada frente a cambios en la disponibilidad de nutrientes y el estado fisiológico del organismo.
Historia y descubrimiento
La historia de PPARα se sitúa en la intersección entre la bioquímica de lípidos, la toxicología hepática y la biología de los receptores nucleares. Antes de su identificación molecular, ya se había descrito que ciertos compuestos químicos, denominados proliferadores de peroxisomas, inducían un aumento significativo en el número y tamaño de estos orgánulos en hepatocitos de roedores, acompañado de una activación de rutas de oxidación de ácidos grasos. Sin embargo, durante décadas se desconocía el mecanismo molecular que mediaba estos efectos (Reddy & Krishnakantha, 1975; Lazarow & De Duve, 1976).
El avance clave se produjo en 1990, cuando Issemann y Green identificaron un receptor nuclear perteneciente a la superfamilia de receptores hormonales que podía ser activado por estos compuestos. Este descubrimiento proporcionó por primera vez un marco mecanístico para entender cómo señales químicas exógenas podían modular la expresión génica relacionada con el metabolismo lipídico. El receptor fue denominado PPAR (Peroxisome Proliferator-Activated Receptor), y el isoformo inicialmente caracterizado corresponde a lo que posteriormente se definiría como PPARα(Issemann & Green, 1990).
Durante la década de 1990, estudios posteriores permitieron identificar otros isoformas de la familia PPAR, como PPARγ y PPARδ (también conocido como PPARβ), lo que consolidó la idea de que estos receptores constituían una subfamilia funcionalmente especializada dentro de los receptores nucleares. En este contexto, PPARα fue el primero en ser caracterizado y el que mostró una asociación más directa con la regulación del metabolismo de ácidos grasos en tejidos altamente oxidativos (Kliewer et al., 1994).
A medida que avanzaba la investigación, se demostró que PPARα no era simplemente un mediador de la respuesta a xenobióticos, sino un regulador fisiológico clave del metabolismo energético. La identificación de ligandos endógenos, como ácidos grasos libres y eicosanoides, reforzó la idea de que este receptor actúa como un sensor metabólico que integra señales nutricionales con respuestas transcripcionales adaptativas (Forman et al., 1997).
En paralelo, el desarrollo de agonistas farmacológicos selectivos, como los fibratos, permitió trasladar estos conocimientos al ámbito clínico. Estos compuestos, utilizados en el tratamiento de dislipidemias, demostraron que la activación de PPARα podía modular de forma efectiva el perfil lipídico plasmático, reduciendo triglicéridos y aumentando colesterol HDL. Este vínculo entre farmacología y fisiología consolidó a PPARα como una diana terapéutica relevante en enfermedades metabólicas (Fruchart, 2009).
Con el cambio de siglo, la investigación sobre PPARα se integró en un marco más amplio de biología de sistemas, donde se reconoció su papel como nodo regulador en la homeostasis energética, la inflamación y la interacción entre metabolismo y señalización celular. Estudios transcriptómicos y genómicos han permitido mapear extensamente sus genes diana y comprender su papel en la adaptación metabólica al ayuno, el ejercicio y el estrés fisiológico (Kersten, 2014).
En conjunto, el recorrido histórico de PPARα refleja una transición desde la observación toxicológica hacia la comprensión de un sistema regulador central en biología metabólica, con implicaciones tanto fisiológicas como farmacológicas.
Estructura y organización molecular
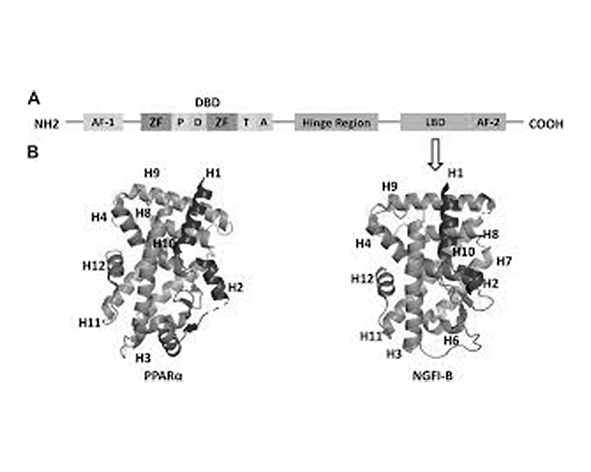
El PPARα presenta la arquitectura modular característica de los receptores nucleares, organizada en dominios funcionales que permiten la integración de señales lipídicas con la regulación de la transcripción génica. Esta organización estructural está altamente conservada dentro de la superfamilia y es clave para su mecanismo de acción como factor de transcripción dependiente de ligando (Evans et al., 2004; Xu et al., 1999).
En el extremo N-terminal se localiza el dominio A/B, que contiene la función de activación AF-1 (Activation Function-1). Este dominio permite una regulación transcripcional en gran medida independiente del ligando y participa en la interacción con cofactores celulares. Su actividad puede estar modulada por modificaciones postraduccionales, como la fosforilación, lo que introduce una capa adicional de regulación dependiente del contexto celular (Gelman et al., 1999).
A continuación se encuentra el dominio C o dominio de unión al ADN (DBD), uno de los elementos más conservados estructuralmente. Este dominio contiene dos motivos tipo “zinc finger” que permiten el reconocimiento específico de secuencias PPRE en el ADN. Estas secuencias suelen consistir en repeticiones directas del motivo AGGTCA separadas por un nucleótido (DR1), lo que facilita la unión del heterodímero PPARα–RXR y la posterior regulación de genes diana (Evans et al., 2004).
El dominio D, también denominado región bisagra, proporciona flexibilidad estructural entre el DBD y el dominio de unión a ligando. Aunque inicialmente se consideraba una región pasiva, se ha demostrado que participa en la regulación de la localización nuclear y en la interacción con proteínas coreguladoras, contribuyendo a la dinámica funcional del receptor (Kersten, 2014).
En el extremo C-terminal se sitúa el dominio E/F, que incluye el dominio de unión a ligando (LBD) y la función de activación AF-2. Este dominio presenta una cavidad hidrofóbica relativamente amplia y flexible, lo que permite la unión de una gran diversidad de ligandos lipídicos, desde ácidos grasos hasta compuestos sintéticos como los fibratos. La unión del ligando induce un cambio conformacional que reposiciona la hélice 12 del LBD, facilitando la interacción con coactivadores transcripcionales y desplazando a correpresores (Xu et al., 1999).
La funcionalidad de PPARα depende además de su capacidad para formar heterodímeros con el receptor RXR, una interacción esencial para su unión al ADN. Este complejo heterodimérico reconoce los elementos PPRE y coordina el reclutamiento de maquinaria transcripcional, integrando señales metabólicas con respuestas génicas específicas (Evans et al., 2004).
En conjunto, la estructura de PPARα refleja un diseño molecular optimizado para detectar señales lipídicas y traducirlas en cambios coordinados en la expresión génica, permitiendo una adaptación eficiente a variaciones en el entorno metabólico.
Distribución tisular
El PPARα presenta un patrón de expresión altamente específico, predominando en tejidos con elevada capacidad para la oxidación de ácidos grasos y una demanda energética sostenida. Esta distribución refleja su papel central en la regulación del metabolismo lipídico y la adaptación a cambios en la disponibilidad de nutrientes (Kersten, 2014; Pawlak et al., 2015).
El tejido donde se expresa de forma más abundante es el hígado, considerado el principal órgano regulador del metabolismo energético sistémico. En este contexto, PPARα controla la expresión de genes implicados en la captación, activación y degradación de ácidos grasos, así como en la cetogénesis, especialmente durante el ayuno prolongado (Kersten, 2014).
También se observa una expresión significativa en el corazón, donde los ácidos grasos constituyen la principal fuente de energía. La activación de PPARα en cardiomiocitos favorece la oxidación lipídica mitocondrial, contribuyendo al mantenimiento de la función contráctil y del equilibrio energético (Pawlak et al., 2015).
En el músculo esquelético, PPARα participa en la utilización de ácidos grasos como sustrato energético, particularmente en fibras musculares de tipo oxidativo. Aunque su expresión es menor que en el hígado o el corazón, su actividad contribuye a la flexibilidad metabólica del tejido muscular (Kersten, 2014).
El riñón, especialmente en el túbulo proximal, también presenta niveles relevantes de expresión de PPARα, donde regula procesos relacionados con el metabolismo energético y la reabsorción tubular, altamente dependientes de la oxidación de lípidos (Pawlak et al., 2015).
En menor medida, PPARα se expresa en el intestino delgado, donde participa en la absorción y procesamiento de lípidos dietarios, así como en la regulación de genes implicados en el transporte y metabolismo de ácidos grasos a nivel enterocitario (Kersten, 2014).
Asimismo, su expresión en células del sistema inmunitario, como macrófagos, sugiere un papel adicional en la modulación de la respuesta inflamatoria, integrando señales metabólicas con funciones inmunológicas (Pawlak et al., 2015).
Mecanismo de acción
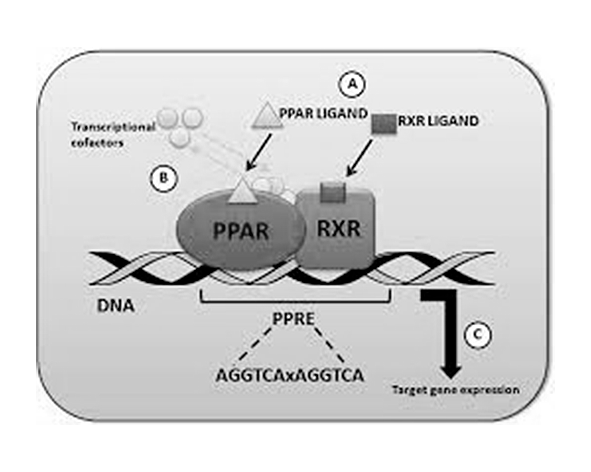
El PPARα actúa como un factor de transcripción dependiente de ligando cuya actividad se basa en la regulación directa de la expresión génica mediante unión a elementos específicos del ADN. Este proceso comienza con la unión de ligandos lipídicos —como ácidos grasos libres, eicosanoides o compuestos sintéticos— al dominio de unión a ligando (LBD), lo que induce un cambio conformacional en el receptor (Evans et al., 2004; Kersten, 2014).
Tras su activación, PPARα forma un heterodímero con el receptor RXR (Retinoid X Receptor). Este complejo es funcionalmente activo y se une a secuencias específicas del ADN denominadas PPRE (Peroxisome Proliferator Response Elements), localizadas en las regiones promotoras de genes diana. Estas secuencias suelen consistir en repeticiones directas del motivo AGGTCA separadas por un nucleótido (DR1), lo que permite el reconocimiento estructural del heterodímero (Evans et al., 2004).
En ausencia de ligando, el complejo PPARα–RXR puede encontrarse asociado a correpresores que mantienen la cromatina en un estado transcripcionalmente inactivo. La unión del ligando provoca un cambio conformacional que favorece la liberación de estos correpresores y el reclutamiento de coactivadores transcripcionales, como PGC-1α, SRC-1 o CBP/p300, que facilitan la remodelación de la cromatina y la activación de la transcripción génica (Kersten, 2014).
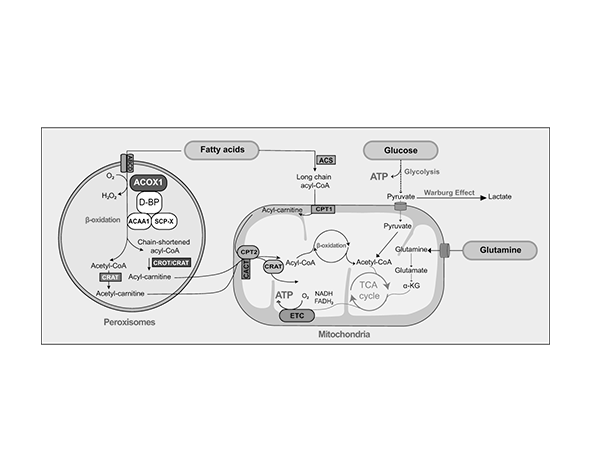
Como resultado, se incrementa la expresión de genes implicados en múltiples procesos metabólicos, incluyendo la captación de ácidos grasos (CD36), su transporte intracelular (proteínas FABP) y su oxidación en mitocondrias (CPT1) y peroxisomas (ACOX1). Este programa transcripcional permite una adaptación coordinada al uso de lípidos como fuente energética (Pawlak et al., 2015).
Además de su función como activador transcripcional, PPARα también puede ejercer efectos de transrepresión, interfiriendo con la actividad de factores de transcripción proinflamatorios como NF-κB y AP-1. Este mecanismo no requiere necesariamente la unión directa al ADN, sino que implica interacciones proteína-proteína que reducen la expresión de genes implicados en la respuesta inflamatoria (Kersten, 2014).
La actividad de PPARα está modulada por múltiples factores adicionales, incluyendo la disponibilidad de ligandos, modificaciones postraduccionales y la interacción con cofactores específicos, lo que permite una regulación fina y dependiente del contexto fisiológico (Evans et al., 2004).
Rol fisiológico
El PPARα desempeña un papel central en la regulación de la homeostasis energética, especialmente en situaciones donde el organismo debe adaptarse a cambios en la disponibilidad de nutrientes. Su función está estrechamente ligada a la capacidad de movilizar y utilizar ácidos grasos como fuente principal de energía, particularmente durante el ayuno o el ejercicio prolongado (Kersten, 2014; Pawlak et al., 2015).
En el hígado, PPARα coordina la activación de rutas metabólicas clave como la β-oxidación de ácidos grasos y la cetogénesis. Durante el ayuno, su activación permite transformar ácidos grasos en cuerpos cetónicos, que pueden ser utilizados como combustible por tejidos periféricos como el cerebro, el músculo o el corazón, reduciendo así la dependencia de la glucosa (Kersten, 2014).
En el corazón, donde la demanda energética es constante y elevada, PPARα favorece el uso de ácidos grasos como principal sustrato energético. Esta regulación es esencial para mantener la eficiencia metabólica del tejido cardíaco, cuya función depende de un suministro continuo de ATP (Pawlak et al., 2015).
En el músculo esquelético, PPARα contribuye a la flexibilidad metabólica, permitiendo la alternancia entre el uso de glucosa y ácidos grasos en función de la disponibilidad energética. Su actividad es especialmente relevante en fibras musculares oxidativas, donde facilita la utilización sostenida de lípidos durante esfuerzos prolongados (Kersten, 2014).
Además de su papel metabólico, PPARα participa en la modulación de procesos inflamatorios. A través de mecanismos de transrepresión, puede reducir la expresión de genes proinflamatorios, contribuyendo a un equilibrio entre metabolismo y respuesta inmune. Este aspecto resulta especialmente relevante en tejidos donde la inflamación y el metabolismo están estrechamente interconectados (Pawlak et al., 2015).
En conjunto, PPARα actúa como un regulador adaptativo que integra señales nutricionales y energéticas para ajustar la expresión génica a las necesidades fisiológicas del organismo, permitiendo una respuesta coordinada frente a cambios metabólicos.
Farmacología
El PPARα constituye una diana farmacológica bien establecida en el contexto del metabolismo lipídico, especialmente en el tratamiento de alteraciones como la hipertrigliceridemia. Los principales agonistas de este receptor son los fibratos, una clase de compuestos que incluyen moléculas como el fenofibrato, gemfibrozilo o bezafibrato, utilizados clínicamente para modular el perfil lipídico plasmático (Fruchart, 2009; Staels et al., 1998).
Los fibratos actúan como agonistas del dominio de unión a ligando (LBD) de PPARα, induciendo su activación y desencadenando el programa transcripcional asociado a la oxidación de ácidos grasos. Como consecuencia, se incrementa la expresión de genes implicados en la β-oxidación, se reduce la síntesis hepática de triglicéridos y se favorece el catabolismo de lipoproteínas ricas en triglicéridos (Kersten, 2014).
Uno de los efectos más característicos de estos fármacos es la disminución de los niveles plasmáticos de triglicéridos, acompañada de un aumento moderado del colesterol HDL. Este efecto se relaciona con la regulación de apolipoproteínas como ApoA-I y ApoA-II, así como con la disminución de ApoC-III, una proteína que inhibe la lipoproteína lipasa (Staels et al., 1998).
Además de sus efectos sobre el metabolismo lipídico, los agonistas de PPARα han mostrado propiedades antiinflamatorias, mediadas en parte por la inhibición de vías como NF-κB. Este componente añade una dimensión adicional a su perfil farmacológico, aunque su relevancia clínica puede variar en función del contexto patológico (Kersten, 2014).
En los últimos años, se han desarrollado moduladores más selectivos, conocidos como SPPARMα (Selective PPARα Modulators), diseñados para optimizar los efectos beneficiosos sobre el metabolismo lipídico minimizando efectos adversos. Estos compuestos representan una evolución en la farmacología de PPARα, basada en una activación más específica y dependiente del contexto conformacional del receptor (Fruchart, 2013).
A pesar de su utilidad clínica, el uso de agonistas de PPARα requiere una evaluación cuidadosa, ya que su activación puede implicar efectos sistémicos complejos, especialmente en combinación con otros tratamientos hipolipemiantes.
Interacción con el sistema endocannabinoide
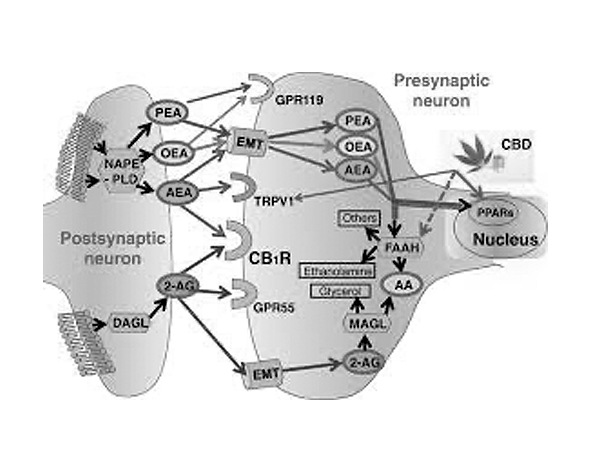
El PPARα mantiene una relación funcional relevante con el sistema endocannabinoide (SEC), actuando como una diana nuclear para diversos lípidos bioactivos estructuralmente relacionados con los endocannabinoides. Esta interacción representa un punto de convergencia entre señalización lipídica y regulación transcripcional, ampliando el alcance fisiológico de ambos sistemas (Lo Verme et al., 2005; O’Sullivan, 2016).
Entre los ligandos endógenos más relevantes se encuentran las N-aciletanolamidas, como la palmitoiletanolamida (PEA) y la oleoiletanolamida (OEA). Aunque no son endocannabinoides clásicos en el sentido estricto —ya que no activan directamente los receptores CB1 o CB2— comparten rutas biosintéticas con la anandamida (AEA) y pueden activar directamente PPARα, induciendo cambios en la expresión génica relacionados con metabolismo e inflamación (Lo Verme et al., 2005).
La activación de PPARα por estos lípidos conduce a efectos más lentos pero sostenidos en comparación con la señalización mediada por receptores de membrana como CB1 o CB2. Mientras que estos últimos generan respuestas rápidas a través de cascadas de señalización intracelular, PPARα modula programas transcripcionales completos, lo que implica adaptaciones fisiológicas a medio y largo plazo (O’Sullivan, 2016).
Además, existe una interrelación metabólica entre el SEC y PPARα a nivel enzimático. Enzimas como FAAH, responsables de la degradación de la anandamida, también regulan la disponibilidad de otras N-aciletanolamidas capaces de activar PPARα, lo que sugiere una regulación cruzada entre ambos sistemas (Lo Verme et al., 2005).
Por otro lado, algunos fitocannabinoides han mostrado capacidad para interactuar de forma indirecta con PPARα o modular vías relacionadas, aunque estos mecanismos no están completamente caracterizados y continúan siendo objeto de investigación. En este contexto, PPARα se posiciona como una diana potencial dentro del marco más amplio de la farmacología cannabinoide, más allá de los receptores clásicos del SEC (O’Sullivan, 2016).
Esta interacción entre el sistema endocannabinoide y PPARα pone de manifiesto la existencia de una red integrada de señalización lipídica que conecta receptores de membrana, enzimas metabólicas y factores de transcripción nuclear en la regulación de la homeostasis.
Importancia en investigación científica
El PPARα se ha consolidado como un eje central en la investigación biomédica relacionada con el metabolismo energético, debido a su papel en la regulación de la oxidación de ácidos grasos y la adaptación al ayuno. Su estudio ha permitido comprender mejor los mecanismos moleculares que subyacen a patologías metabólicas como la dislipidemia, la esteatosis hepática y el síndrome metabólico (Kersten, 2014; Pawlak et al., 2015).
En el ámbito de la enfermedad hepática, PPARα ha sido ampliamente investigado por su capacidad para modular la acumulación de lípidos en el hígado. Modelos experimentales han demostrado que su activación favorece la oxidación lipídica y reduce la acumulación de triglicéridos hepáticos, lo que lo posiciona como un objetivo relevante en el estudio de la esteatosis hepática no alcohólica (NAFLD) (Pawlak et al., 2015).
En el contexto cardiovascular, su papel en la regulación del metabolismo lipoproteico y la inflamación ha despertado interés en relación con el riesgo aterogénico. La modulación de PPARα influye en el equilibrio entre lipoproteínas plasmáticas y en la respuesta inflamatoria vascular, aspectos clave en la investigación de enfermedades cardiovasculares (Fruchart, 2009).
Además, la capacidad de PPARα para interactuar con vías inflamatorias ha ampliado su relevancia hacia campos como la inmunometabolismo, donde se estudia la conexión entre metabolismo celular y función inmunitaria. Su actividad como modulador de factores como NF-κB lo sitúa en un punto estratégico entre metabolismo e inflamación (Kersten, 2014).
En los últimos años, el desarrollo de tecnologías ómicas (transcriptómica, lipidómica) ha permitido caracterizar con mayor precisión los genes diana de PPARα y su papel en redes regulatorias complejas. Estos enfoques han revelado que su actividad no se limita a la oxidación de lípidos, sino que participa en procesos más amplios de adaptación celular al entorno metabólico (Pawlak et al., 2015).
Asimismo, el interés por PPARα se ha extendido al estudio de ligandos endógenos y exógenos, incluyendo compuestos derivados de lípidos y moléculas bioactivas relacionadas con el sistema endocannabinoide. Este enfoque ha abierto nuevas líneas de investigación sobre la señalización lipídica integrada y su impacto en la fisiología y la farmacología (O’Sullivan, 2016).
Referencias
- Reddy JK, Krishnakantha TP. (1975). Hepatic peroxisome proliferation: induction by hypolipidemic drugs. Science. - Lazarow PB, De Duve C. (1976). A fatty acyl-CoA oxidizing system in rat liver peroxisomes. Proceedings of the National Academy of Sciences. - Issemann I, Green S. (1990). Activation of a member of the steroid hormone receptor superfamily by peroxisome proliferators. Nature. - Kliewer SA, Forman BM, Blumberg B, et al. (1994). Differential expression and activation of a family of murine peroxisome proliferator-activated receptors. Proceedings of the National Academy of Sciences. - Forman BM, Chen J, Evans RM. (1997). Hypolipidemic drugs, polyunsaturated fatty acids, and eicosanoids are ligands for PPARα. Proceedings of the National Academy of Sciences. - Staels B, Dallongeville J, Auwerx J, et al. (1998). Mechanism of action of fibrates on lipid and lipoprotein metabolism. Circulation. - Xu HE, Lambert MH, Montana VG, et al. (1999). Molecular basis of PPARα activation by ligands. Molecular Cell. - Evans RM, Barish GD, Wang YX. (2004). PPARs and the complex journey to obesity. Nature Medicine. - Lo Verme J, Gaetani S, Fu J, et al. (2005). The nuclear receptor PPAR-α mediates the anti-inflammatory actions of palmitoylethanolamide. Molecular Pharmacology. - Fruchart JC. (2009). Selective peroxisome proliferator-activated receptor alpha modulators. European Heart Journal. - Kersten S. (2014). Integrated physiology and systems biology of PPARα. Molecular Metabolism. - Pawlak M, Lefebvre P, Staels B. (2015). Molecular mechanism of PPARα action and its impact on lipid metabolism. Journal of Hepatology. - Fruchart JC. (2013). Peroxisome proliferator-activated receptor-α (PPARα): At the crossroads of obesity, diabetes and cardiovascular disease. Atherosclerosis. - O’Sullivan SE. (2016). An update on PPAR activation by cannabinoids. British Journal of Pharmacology.