Introducción
El canal TRPA1 (Transient Receptor Potential Ankyrin 1) es una proteína de membrana perteneciente a la familia de canales iónicos TRP (Transient Receptor Potential), caracterizada por su papel en la detección de estímulos químicos potencialmente nocivos y en la transducción de señales sensoriales asociadas al daño tisular. Dentro de esta familia, TRPA1 constituye el único miembro funcional de la subfamilia TRPA en mamíferos, lo que refuerza su singularidad estructural y funcional.
Desde una perspectiva fisiológica, TRPA1 actúa como un sensor molecular altamente reactivo frente a compuestos electrofílicos, muchos de los cuales se originan tanto en el entorno (irritantes ambientales, productos de combustión, compuestos presentes en alimentos) como en procesos endógenos asociados al estrés oxidativo y la inflamación. Esta capacidad de detectar alteraciones químicas en el medio interno y externo posiciona a TRPA1 como un componente clave en la protección del organismo frente a agresiones químicas, funcionando como una interfaz entre el entorno y el sistema nervioso sensorial (Jordt et al., 2004; Viana, 2016).
A nivel celular, TRPA1 se expresa predominantemente en neuronas sensoriales periféricas, especialmente en aquellas implicadas en la nocicepción, donde contribuye a la generación de señales eléctricas en respuesta a estímulos irritantes o lesivos. Su activación conduce a la entrada de cationes, principalmente calcio, desencadenando procesos de despolarización neuronal y liberación de mediadores neurogénicos que participan en la percepción del dolor y en la modulación de la inflamación (Bautista et al., 2006).
En el marco conceptual del sistema endocannabinoide ampliado o endocannabinoidome, TRPA1 se reconoce como una diana molecular no clásica modulada por diversos lípidos endógenos y fitocannabinoides. Esta interacción amplía la visión tradicional centrada en los receptores CB1 y CB2, integrando a TRPA1 dentro de una red más compleja de señalización que conecta procesos sensoriales, inflamatorios y metabólicos (Zygmunt et al., 2013).
En conjunto, TRPA1 representa un nodo funcional relevante en la biología sensorial y en la investigación biomédica contemporánea, no solo por su papel en la detección de estímulos nocivos, sino también por su implicación en procesos fisiopatológicos donde la inflamación, el estrés celular y la señalización lipídica convergen.
Historia y descubrimiento
El canal TRPA1 fue identificado a comienzos de la década de 2000 en el contexto de la búsqueda sistemática de nuevos miembros de la familia de canales TRP (Transient Receptor Potential), un grupo de proteínas implicadas en la transducción de estímulos sensoriales. Inicialmente, esta proteína fue descrita bajo el nombre de ANKTM1 (Ankyrin-like transmembrane protein 1), debido a la presencia de múltiples repeticiones de anquirina en su región N-terminal, una característica estructural poco común dentro de la familia TRP (Jaquemar et al., 1999).
En sus primeras descripciones, ANKTM1 se detectó en fibroblastos humanos, lo que llevó a pensar inicialmente en funciones relacionadas con procesos celulares generales más que en la señalización sensorial. Sin embargo, estudios posteriores demostraron que su expresión era particularmente relevante en neuronas sensoriales primarias, lo que marcó un cambio en la interpretación de su función biológica.
El avance decisivo en la caracterización funcional de TRPA1 se produjo cuando diversos grupos de investigación demostraron su activación por compuestos químicos irritantes, como el isotiocianato de alilo (presente en la mostaza) y la alicina (derivada del ajo). Estos hallazgos permitieron establecer a TRPA1 como un sensor químico clave en neuronas nociceptivas, capaz de detectar sustancias potencialmente dañinas mediante mecanismos directos de activación (Bandell et al., 2004; Jordt et al., 2004).
Durante los años siguientes, la investigación sobre TRPA1 se expandió rápidamente, revelando su sensibilidad a una amplia gama de compuestos electrofílicos y especies reactivas generadas durante procesos inflamatorios y de estrés oxidativo. Este descubrimiento fue especialmente relevante, ya que introdujo un mecanismo de activación basado en la modificación covalente de residuos de cisteína en la proteína, diferenciándolo de otros canales TRP que responden principalmente a estímulos físicos o ligandos no reactivos.
Paralelamente, se consolidó su papel en la fisiología sensorial, particularmente en la nocicepción química y en la respuesta a irritantes ambientales. Estudios en modelos animales demostraron que la ausencia de TRPA1 alteraba la respuesta frente a determinados estímulos nocivos, confirmando su implicación en la detección del dolor y en la señalización inflamatoria (Bautista et al., 2006).
En etapas más recientes, TRPA1 ha sido integrado dentro del concepto de endocannabinoidome, al identificarse su modulación por lípidos bioactivos y fitocannabinoides. Este enfoque ha ampliado su relevancia más allá de la nocicepción clásica, situándolo en una red más compleja de señalización molecular donde convergen mecanismos sensoriales, metabólicos e inflamatorios (Zygmunt et al., 2013).
Estructura y organización molecular
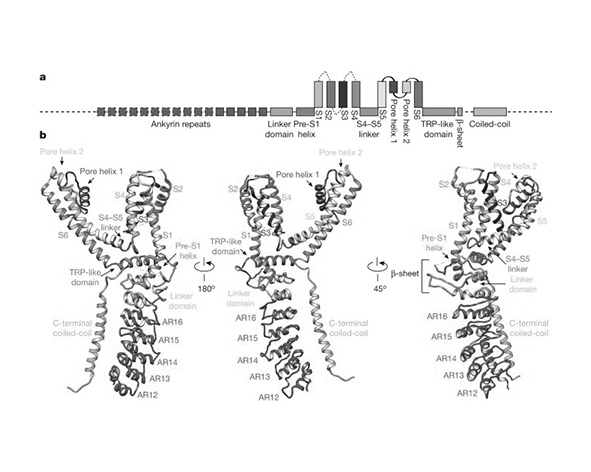
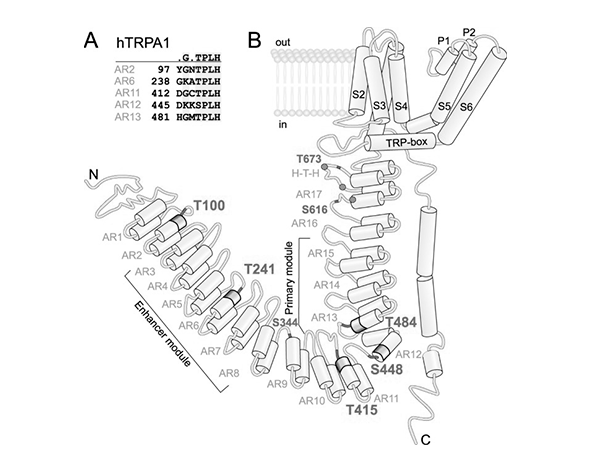
El canal TRPA1 es una proteína de membrana que forma un canal iónico tetramérico, donde cuatro subunidades idénticas se ensamblan para constituir un poro central permeable a cationes. Cada subunidad presenta una arquitectura característica de la familia TRP, compuesta por seis dominios transmembrana (S1–S6), con una región de poro situada entre los segmentos S5 y S6. Esta organización estructural es esencial para la conducción iónica y la selectividad funcional del canal.
Una de las características más distintivas de TRPA1 es su extensa región N-terminal intracelular, que contiene entre 14 y 18 repeticiones de anquirina. Estas repeticiones forman estructuras helicoidales implicadas en la detección de estímulos y en la interacción con otras proteínas y componentes del citoesqueleto. A diferencia de otros canales TRP, la longitud y complejidad de esta región en TRPA1 sugieren un papel relevante en la integración de señales mecánicas y químicas (Paulsen et al., 2015).
El dominio del poro presenta propiedades de permeabilidad no selectiva a cationes, permitiendo el paso de sodio (Na⁺) y calcio (Ca²⁺), siendo este último especialmente relevante en la activación de cascadas intracelulares. La entrada de Ca²⁺ no solo contribuye a la despolarización neuronal, sino que también puede modular la propia actividad del canal mediante mecanismos de retroalimentación.
A nivel molecular, TRPA1 contiene múltiples residuos de cisteína y lisina altamente reactivos en su dominio intracelular, particularmente en la región N-terminal. Estos residuos son fundamentales para su mecanismo de activación, ya que pueden sufrir modificaciones covalentes por compuestos electrofílicos. Esta propiedad confiere a TRPA1 una sensibilidad única frente a sustancias químicas reactivas, diferenciándolo de otros canales TRP cuya activación depende principalmente de interacciones no covalentes (Hinman et al., 2006).
Estudios estructurales recientes mediante criomicroscopía electrónica (cryo-EM) han permitido visualizar la conformación tridimensional de TRPA1 con mayor resolución, revelando detalles sobre la disposición de sus dominios, la arquitectura del poro y los posibles estados conformacionales asociados a su activación. Estos estudios han mostrado que la apertura del canal implica cambios estructurales coordinados que afectan tanto a los dominios transmembrana como a las regiones intracelulares, reflejando la complejidad de su regulación funcional.
En conjunto, la estructura de TRPA1 integra elementos típicos de los canales TRP con adaptaciones únicas que le permiten actuar como sensor químico altamente especializado, capaz de responder a una amplia variedad de estímulos mediante mecanismos moleculares distintivos.
Distribución y expresión
El canal TRPA1 presenta un patrón de expresión predominantemente asociado al sistema sensorial periférico, aunque su distribución se extiende a diversos tejidos y tipos celulares, reflejando su papel como sensor molecular de estímulos químicos y señales de estrés celular.
A nivel neuronal, TRPA1 se expresa principalmente en neuronas sensoriales primarias de pequeño diámetro, localizadas en los ganglios de la raíz dorsal y en el ganglio trigeminal. Estas neuronas están implicadas en la nocicepción y en la detección de estímulos potencialmente dañinos, donde TRPA1 actúa como un detector de irritantes químicos y mediadores inflamatorios. En muchos casos, su expresión se solapa con la de otros canales como TRPV1, lo que sugiere una cooperación funcional en la transducción de señales nociceptivas (Story et al., 2003; Bautista et al., 2006).
Más allá del sistema nervioso, TRPA1 también se ha identificado en tejidos periféricos, lo que amplía su relevancia fisiológica:
- En el epitelio respiratorio, donde participa en la detección de irritantes inhalados y en la activación de reflejos defensivos como la tos.
- En el tracto gastrointestinal, donde puede contribuir a la detección de compuestos químicos presentes en los alimentos y a la modulación de respuestas viscerales.
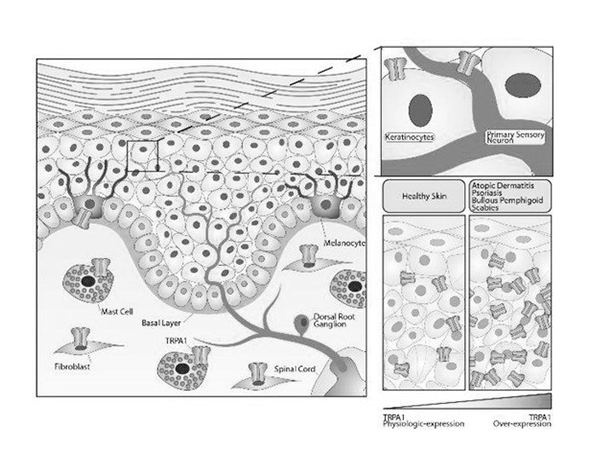
- En la piel, particularmente en queratinocitos y terminaciones nerviosas cutáneas, donde interviene en la percepción de estímulos irritantes y en procesos inflamatorios locales.
- En células inmunitarias, incluyendo macrófagos y mastocitos, lo que sugiere un papel en la modulación de la respuesta inflamatoria.
- En la vasculatura, donde puede influir en la regulación del tono vascular y en respuestas neurogénicas.
Esta distribución multisistémica indica que TRPA1 no se limita a una función estrictamente sensorial, sino que participa en la integración de señales químicas en distintos contextos fisiológicos. Su presencia en tejidos expuestos al entorno, como el sistema respiratorio y la piel, refuerza su papel como primera línea de detección frente a agentes potencialmente dañinos.
Además, la coexpresión de TRPA1 con receptores y canales implicados en la señalización lipídica y en la inflamación sugiere su integración en redes moleculares complejas, donde contribuye a la amplificación o modulación de respuestas adaptativas frente a estrés químico y tisular.
Activación y mecanismos de señalización
El canal TRPA1 presenta un perfil de activación altamente versátil, siendo capaz de responder a una amplia variedad de estímulos químicos tanto exógenos como endógenos. Su característica más distintiva es su capacidad para activarse mediante la modificación covalente directa de residuos específicos en la proteína, lo que lo diferencia de otros canales iónicos que dependen de interacciones ligando-receptor más convencionales.
Activación por compuestos electrofílicos
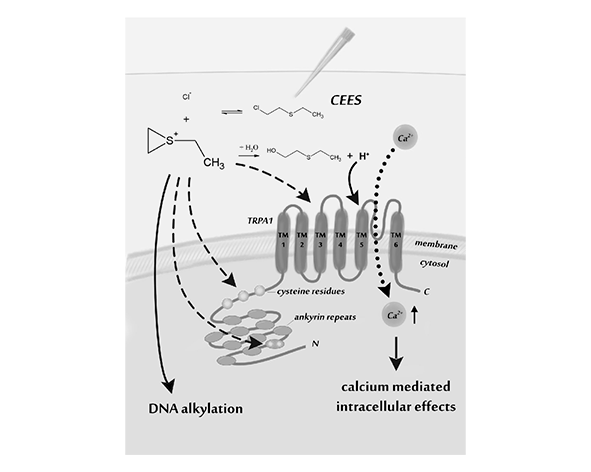
El mecanismo más representativo de TRPA1 implica la modificación covalente de residuos de cisteína y lisina en su dominio N-terminal intracelular. Estos residuos nucleofílicos reaccionan con compuestos electrofílicos altamente reactivos, induciendo cambios conformacionales que favorecen la apertura del canal (Hinman et al., 2006; Macpherson et al., 2007).
Entre los activadores más estudiados se encuentran compuestos presentes en alimentos y en el entorno, como el isotiocianato de alilo, la alicina o el cinamaldehído, así como irritantes derivados de procesos de combustión. Este mecanismo convierte a TRPA1 en un sensor directo de reactividad química, más que en un receptor clásico dependiente de afinidad molecular reversible.
Activación por mediadores endógenos
TRPA1 también responde a moléculas generadas durante procesos fisiológicos y patológicos, especialmente en contextos de inflamación y estrés oxidativo. Entre estos activadores destacan productos de la peroxidación lipídica como el 4-hidroxinonenal, prostaglandinas reactivas y especies reactivas de oxígeno.
Estos compuestos pueden activar el canal mediante mecanismos similares de modificación covalente, estableciendo un vínculo directo entre el daño celular, el estrés químico y la señalización sensorial (Trevisani et al., 2007).
Entrada de cationes y señalización intracelular
La activación de TRPA1 da lugar a la apertura de su poro iónico, permitiendo la entrada de cationes, principalmente calcio (Ca²⁺) y sodio (Na⁺). La entrada de calcio desempeña un papel central en la señalización intracelular, contribuyendo tanto a la despolarización de la membrana como a la activación de vías de señalización dependientes de calcio.
Además, el Ca²⁺ puede modular la actividad del propio canal, generando mecanismos de retroalimentación que ajustan la intensidad y duración de la respuesta.
Liberación de neuropéptidos
En neuronas sensoriales, la activación de TRPA1 desencadena la liberación de neuropéptidos como la sustancia P y el péptido relacionado con el gen de la calcitonina (CGRP). Estos mediadores participan en la inflamación neurogénica, promoviendo vasodilatación, aumento de la permeabilidad vascular y activación de células inmunitarias.
Este proceso conecta directamente la activación del canal con respuestas inflamatorias locales, integrando señalización neuronal e inmunológica.
Integración en redes de señalización
TRPA1 funciona como un integrador de señales dentro de redes moleculares más amplias. Su coexpresión con otros canales como TRPV1, así como su modulación por lípidos bioactivos y rutas de fosforilación intracelular, permite una regulación dinámica en función del contexto fisiológico.
Esta integración refuerza su papel como nodo clave en la detección de estímulos nocivos y en la coordinación de respuestas adaptativas frente al estrés químico y tisular.
Interacción con fitocannabinoides y sistema endocannabinoide
El canal TRPA1 forma parte del conjunto de dianas moleculares integradas dentro del denominado endocannabinoidome, un marco conceptual que amplía la visión clásica del sistema endocannabinoide más allá de los receptores CB1 y CB2. En este contexto, TRPA1 actúa como una diana no canónica capaz de ser modulada por diversos lípidos bioactivos, incluyendo fitocannabinoides y endocannabinoides.
A diferencia de los receptores cannabinoides clásicos, cuya señalización se basa en mecanismos acoplados a proteínas G, la interacción de TRPA1 con estos compuestos se produce a nivel de modulación directa del canal iónico, alterando su probabilidad de apertura y su dinámica de activación.
Fitocannabinoides
Diversos fitocannabinoides han demostrado capacidad para interactuar con TRPA1 en modelos experimentales:
- Cannabidiol (CBD): actúa como agonista de TRPA1, promoviendo la activación del canal y la entrada de Ca²⁺ en células que lo expresan. Este efecto ha sido descrito en sistemas heterólogos y en neuronas sensoriales, aunque su relevancia fisiológica depende del contexto experimental (Zygmunt et al., 2013).
- Δ9-tetrahidrocannabinol (THC): también puede modular TRPA1, aunque generalmente con menor potencia en comparación con CBD. Su acción sobre este canal se considera secundaria respecto a su interacción con CB1 y CB2.
- Otros fitocannabinoides menores, como CBG o CBC, han mostrado interacción con canales TRP en general, aunque los datos específicos sobre TRPA1 son más limitados y dependen del modelo utilizado.
Estas interacciones reflejan la capacidad de los fitocannabinoides para actuar sobre múltiples dianas moleculares, más allá del sistema cannabinoide clásico.
Endocannabinoides y lípidos relacionados
Algunos endocannabinoides también pueden modular TRPA1:
- Anandamida (AEA): ha demostrado capacidad para activar TRPA1 en determinadas condiciones, actuando como ligando endógeno no selectivo sobre canales TRP.
- Otros lípidos derivados de ácidos grasos poliinsaturados pueden influir en la actividad del canal, ya sea de forma directa o mediante la generación de metabolitos reactivos.
Estas interacciones sitúan a TRPA1 dentro de una red más amplia de señalización lipídica, donde diferentes mediadores pueden converger sobre una misma diana molecular.
Implicaciones funcionales
La interacción entre TRPA1 y compuestos cannabinoides tiene varias implicaciones relevantes:
- Refuerza la idea de que la señalización cannabinoide no se limita a CB1 y CB2
- Conecta la señalización lipídica con mecanismos de nocicepción e inflamación
- Introduce complejidad en la interpretación farmacológica de los fitocannabinoides
Es importante destacar que la activación de TRPA1 por ciertos compuestos no implica necesariamente un efecto fisiológico lineal o clínicamente definido, ya que estos mecanismos dependen de múltiples variables, incluyendo concentración, contexto tisular y coactivación de otras dianas moleculares.
En conjunto, TRPA1 representa una interfaz relevante entre la señalización química mediada por lípidos y la respuesta sensorial del organismo, integrándose dentro de un sistema más amplio donde convergen fitocannabinoides, endocannabinoides y mediadores inflamatorios.
Rol fisiológico
El canal TRPA1 desempeña un papel central en la detección de estímulos químicos potencialmente dañinos y en la integración de respuestas adaptativas frente al estrés celular. Su función se extiende más allá de la nocicepción clásica, participando en múltiples sistemas fisiológicos donde actúa como sensor molecular de alteraciones químicas, inflamatorias y ambientales.
Nocicepción química y dolor
TRPA1 es uno de los principales detectores de estímulos nocivos de origen químico. Su activación en neuronas sensoriales periféricas contribuye a la generación de señales asociadas al dolor, especialmente en contextos de exposición a irritantes o daño tisular.
A diferencia de otros canales implicados en la percepción térmica o mecánica, TRPA1 responde de forma particularmente eficiente a compuestos reactivos, lo que lo convierte en un sensor especializado en dolor químico. Además, su coexpresión con otros canales como TRPV1 permite una amplificación de la señal nociceptiva, contribuyendo a fenómenos de sensibilización periférica.
Inflamación neurogénica
La activación de TRPA1 en terminaciones nerviosas sensoriales induce la liberación de neuropéptidos como la sustancia P y el CGRP, desencadenando respuestas de inflamación neurogénica.
Este tipo de inflamación se caracteriza por:
- Vasodilatación local
- Aumento de la permeabilidad vascular
- Reclutamiento de células inmunitarias
TRPA1 actúa así como un puente funcional entre el sistema nervioso y el sistema inmunitario, facilitando respuestas rápidas frente a agresiones químicas o tisulares.
Detección de estrés oxidativo
Uno de los roles más relevantes de TRPA1 es su capacidad para detectar productos derivados del estrés oxidativo, como aldehídos reactivos y especies reactivas de oxígeno. Esta función lo posiciona como un sensor intracelular de daño metabólico y peroxidación lipídica.
En este contexto, TRPA1 no solo detecta el daño, sino que participa en la señalización que permite al organismo responder a condiciones de estrés, integrando información química con respuestas celulares y sistémicas.
Sistema respiratorio
En el tracto respiratorio, TRPA1 se expresa en fibras sensoriales que detectan irritantes inhalados, como contaminantes ambientales o productos de combustión. Su activación puede inducir reflejos defensivos como la tos, la broncoconstricción y la sensación de irritación.
Este papel es especialmente relevante en la protección frente a agentes inhalados potencialmente dañinos, actuando como un sistema de alerta temprana.
Sistema gastrointestinal
En el sistema digestivo, TRPA1 participa en la detección de compuestos químicos presentes en los alimentos, así como en la modulación de la sensibilidad visceral. Su activación puede influir en la motilidad intestinal y en la percepción de estímulos irritantes a nivel gastrointestinal.
Además, su interacción con mediadores inflamatorios sugiere un papel en condiciones donde existe alteración de la homeostasis intestinal.
Piel y sistema sensorial periférico
En la piel, TRPA1 se encuentra en terminaciones nerviosas y en células cutáneas, donde participa en la detección de irritantes tópicos y en la generación de sensaciones como picor o escozor.
Su activación también contribuye a respuestas inflamatorias locales, integrando señalización sensorial y procesos inmunitarios en el tejido cutáneo.
Sistema vascular
TRPA1 también está implicado en la regulación del tono vascular. Su activación en fibras nerviosas perivasculares puede inducir vasodilatación mediada por neuropéptidos, contribuyendo a la regulación del flujo sanguíneo en respuesta a estímulos locales.
Integración funcional
En conjunto, TRPA1 actúa como un sensor químico multifuncional que conecta:
- Detección de daño celular
- Señalización nociceptiva
- Respuesta inflamatoria
- Adaptación a estímulos ambientales
Su capacidad para responder a señales endógenas y exógenas lo convierte en un nodo clave en la fisiología de la respuesta al estrés químico, integrando sistemas aparentemente independientes dentro de una misma red funcional.
Importancia en investigación científica
El canal TRPA1 se ha consolidado como una diana molecular de interés en investigación biomédica debido a su implicación en procesos donde convergen nocicepción, inflamación y estrés celular. Su capacidad para detectar compuestos reactivos y traducir estas señales en respuestas neuronales y tisulares lo sitúa en una posición estratégica dentro de la fisiopatología de múltiples condiciones.
Uno de los principales focos de estudio es su papel en el dolor crónico, especialmente en contextos de dolor inflamatorio y neuropático. La activación sostenida de TRPA1 por mediadores endógenos derivados del daño tisular puede contribuir a fenómenos de sensibilización periférica, aumentando la excitabilidad de las neuronas sensoriales. Este mecanismo ha llevado a investigar el desarrollo de antagonistas selectivos de TRPA1 como posibles moduladores de la señal nociceptiva, aunque la traslación clínica de estos compuestos aún presenta limitaciones (Viana, 2016).
En el ámbito de la inflamación, TRPA1 se considera un elemento relevante en la denominada inflamación neurogénica. Su activación promueve la liberación de neuropéptidos que amplifican la respuesta inflamatoria local, estableciendo un vínculo funcional entre el sistema nervioso y el sistema inmunitario. Este papel ha despertado interés en patologías donde la inflamación persistente es un componente clave, aunque su modulación terapéutica requiere una comprensión más precisa de sus efectos sistémicos.
Otro campo relevante es el estudio de TRPA1 como sensor de estrés oxidativo y daño celular. La capacidad del canal para activarse mediante productos de peroxidación lipídica y especies reactivas lo convierte en un marcador funcional de alteraciones metabólicas. En este contexto, TRPA1 se investiga como parte de las respuestas adaptativas del organismo frente a condiciones de estrés químico, más que como un objetivo terapéutico aislado.
En el sistema respiratorio, TRPA1 ha sido estudiado en relación con la detección de irritantes inhalados y la generación de reflejos protectores. Su implicación en la respuesta frente a contaminantes ambientales y agentes químicos ha abierto líneas de investigación en patologías respiratorias, donde podría contribuir a la sintomatología asociada a la exposición a irritantes.
En paralelo, la integración de TRPA1 dentro del concepto de endocannabinoidome ha ampliado su relevancia en el estudio de la señalización lipídica compleja. La interacción con fitocannabinoides y endocannabinoides sugiere que TRPA1 forma parte de una red de dianas moleculares interconectadas, donde los efectos biológicos no dependen de un único receptor, sino de la modulación conjunta de múltiples sistemas (Zygmunt et al., 2013).
A pesar del interés creciente, es importante señalar que la investigación sobre TRPA1 presenta desafíos significativos. Su amplia distribución, la diversidad de estímulos que lo activan y su integración en múltiples vías de señalización dificultan la interpretación de sus efectos en contextos fisiológicos complejos. Además, los resultados obtenidos en modelos experimentales no siempre son directamente extrapolables a sistemas humanos.
En conjunto, TRPA1 representa una diana relevante en investigación básica y traslacional, no tanto por ofrecer soluciones terapéuticas directas en la actualidad, sino por aportar una comprensión más profunda de los mecanismos mediante los cuales el organismo detecta y responde a estímulos químicos, inflamatorios y metabólicos.
Referencias
- Jaquemar, D., Schenker, T., & Trueb, B. (1999). An ankyrin-like protein with transmembrane domains is specifically lost after oncogenic transformation of human fibroblasts. Journal of Biological Chemistry. Story, G. M., Peier, A. M., Reeve, A. J., et al. (2003). ANKTM1, a TRP-like channel expressed in nociceptive neurons, is activated by cold temperatures. Cell. - Bandell, M., Story, G. M., Hwang, S. W., et al. (2004). Noxious cold ion channel TRPA1 is activated by pungent compounds. Neuron. - Jordt, S. E., Bautista, D. M., Chuang, H. H., et al. (2004). Mustard oils and cannabinoids excite sensory nerve fibres through the TRPA1 ion channel. Nature. - Bautista, D. M., Jordt, S. E., Nikai, T., et al. (2006). TRPA1 mediates the inflammatory actions of environmental irritants. Cell. - Hinman, A., Chuang, H. H., Bautista, D. M., & Julius, D. (2006). TRPA1 is activated by covalent modification of cysteines. Proceedings of the National Academy of Sciences. - Macpherson, L. J., Dubin, A. E., Evans, M. J., et al. (2007). Noxious compounds activate TRPA1 ion channels through covalent modification of cysteines. Nature. - Trevisani, M., Siemens, J., Materazzi, S., et al. (2007). 4-Hydroxynonenal, an endogenous aldehyde, causes pain through activation of the irritant receptor TRPA1. Proceedings of the National Academy of Sciences. - Viana, F. (2016). TRPA1 channels: molecular sentinels of cellular stress and tissue damage. Journal of Physiology. - Paulsen, C. E., Armache, J. P., Gao, Y., et al. (2015). Structure of the TRPA1 ion channel suggests regulatory mechanisms. Nature. - Zygmunt, P. M., Ermund, A., Movahed, P., et al. (2013). Monoacylglycerols activate TRPA1 channels in sensory neurons. British Journal of Pharmacology.