Introducción
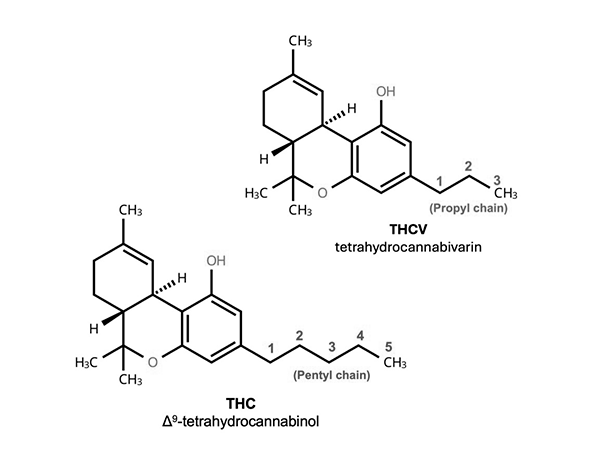
La tetrahidrocannabivarina (THCV) es un fitocannabinoide presente en Cannabis sativa que pertenece a la familia de los cannabinoides neutros derivados de ácidos cannabinoides específicos. Desde el punto de vista estructural, la THCV es un análogo del Δ9-tetrahidrocannabinol (Δ9-THC), diferenciándose principalmente por la longitud de su cadena lateral alquílica, que en este caso está compuesta por tres átomos de carbono (propilo) en lugar de los cinco característicos del THC (pentilo). Esta variación estructural condiciona de forma significativa su interacción con las dianas moleculares del sistema endocannabinoide. (Pertwee, 2008; Morales et al., 2017)
La THCV se biosintetiza en la planta a partir del ácido tetrahidrocannabivarínico (THCVA), que a su vez deriva de precursores distintos a los del THC convencional, concretamente del ácido divarínico en lugar del ácido olivetólico. Este origen biosintético alternativo explica su presencia diferencial en determinadas quimiovariedades de Cannabis, especialmente en genéticas de origen africano donde su concentración puede ser relativamente más elevada. (Citti et al., 2019; Berman et al., 2018)
Desde una perspectiva farmacológica, la THCV presenta un perfil complejo que no puede extrapolarse directamente a partir del Δ9-THC. Estudios experimentales han mostrado que su interacción con el receptor CB1 es dependiente del contexto y la concentración, describiéndose comportamientos que incluyen antagonismo funcional o modulación negativa en determinadas condiciones. En paralelo, su actividad sobre CB2 y otras dianas del denominado endocannabinoidoma sugiere un espectro de acción más amplio, aún en fase de caracterización. (Pertwee, 2008; Di Marzo, 2018)
El interés científico por la THCV ha aumentado en los últimos años debido a su valor como modelo para comprender cómo variaciones estructurales sutiles en los fitocannabinoides pueden traducirse en diferencias relevantes en señalización molecular, farmacodinámica y distribución funcional en el organismo. En este sentido, la THCV representa un ejemplo paradigmático dentro del estudio comparado de cannabinoides de cadena lateral corta frente a sus análogos clásicos. (Morales et al., 2017; Citti et al., 2019)
Historia del descubrimiento
La tetrahidrocannabivarina (THCV) fue identificada por primera vez en la década de 1970 en el contexto de los estudios fitoquímicos destinados a caracterizar la diversidad de cannabinoides presentes en Cannabis sativa. Durante este periodo, grupos de investigación centrados en el aislamiento y elucidación estructural de compuestos minoritarios detectaron la presencia de un análogo del Δ9-THC con una cadena lateral más corta, lo que llevó a su clasificación dentro de la familia de los cannabinoides varínicos. (Gill et al., 1970; Mechoulam & Gaoni, 1972)
El avance en técnicas analíticas como la cromatografía de gases acoplada a espectrometría de masas (GC-MS) y posteriormente la cromatografía líquida de alta resolución (HPLC) permitió diferenciar con mayor precisión estos compuestos de cadena propílica frente a sus equivalentes pentílicos. En este contexto, la THCV fue reconocida como un fitocannabinoide estructuralmente relacionado con el THC, pero derivado de una ruta biosintética distinta basada en precursores de tipo divarínico. (Turner et al., 1980; Hazekamp et al., 2005)
Durante décadas, la THCV fue considerada un cannabinoide minoritario con escasa relevancia funcional, en parte debido a su baja abundancia en la mayoría de quimiovariedades comerciales y a las limitaciones técnicas para su aislamiento en cantidades suficientes. Sin embargo, el interés por este compuesto resurgió a partir de finales de los años 2000, coincidiendo con una mayor atención hacia el endocannabinoidoma y la complejidad de la señalización cannabinoide más allá del Δ9-THC y el cannabidiol (CBD). (Di Marzo, 2018)
Uno de los hitos clave en la reevaluación de la THCV fue la descripción de su comportamiento diferencial sobre el receptor CB1, donde estudios farmacológicos comenzaron a evidenciar que, en determinadas condiciones, podía actuar como antagonista funcional o modulador negativo, en contraste con la actividad agonista típica del THC. Este hallazgo contribuyó a posicionar la THCV como un modelo relevante para estudiar la relación entre estructura química y actividad biológica dentro de los fitocannabinoides. (Pertwee, 2008)
En la actualidad, la THCV forma parte del conjunto de cannabinoides que han pasado de ser considerados meros compuestos secundarios a constituir elementos clave en la investigación sobre diversidad química del cannabis, variabilidad genética de la planta y complejidad farmacológica del sistema endocannabinoide. Su estudio continúa evolucionando a medida que se desarrollan métodos más precisos de análisis, síntesis y evaluación funcional. (Citti et al., 2019; Berman et al., 2018)
Estructura química
La tetrahidrocannabivarina (THCV) pertenece a la familia de los fitocannabinoides con estructura dibenzopirano, compartiendo el núcleo tricíclico característico de compuestos como el Δ9-tetrahidrocannabinol (Δ9-THC). Este núcleo está formado por un sistema aromático fusionado con un anillo ciclohexénico y un anillo pirano, que constituye la base estructural responsable de su interacción con múltiples dianas biológicas. (Mechoulam & Gaoni, 1972; Pertwee, 2008)
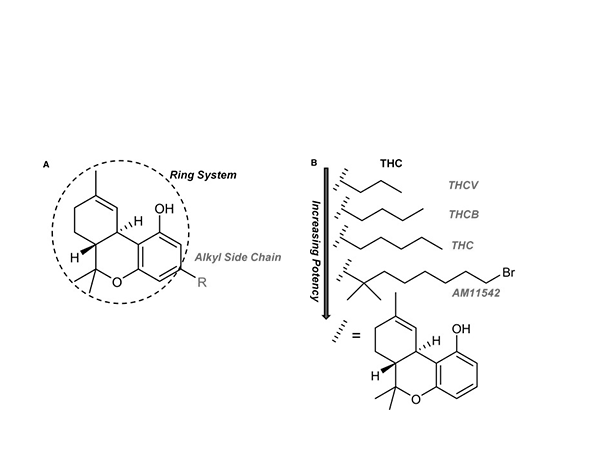
La principal diferencia estructural entre la THCV y el Δ9-THC reside en la cadena lateral alquílica unida al anillo resorcinólico. En el caso de la THCV, esta cadena es de tipo propilo (C3), mientras que en el THC es de tipo pentilo (C5). Esta variación aparentemente menor tiene implicaciones significativas en términos de afinidad por receptores cannabinoides, ya que la longitud de la cadena lateral es un determinante clave en la interacción con el sitio hidrofóbico del receptor CB1. (Pertwee, 2008; Morales et al., 2017)
Desde una perspectiva estructural comparada, se ha observado que la reducción de la cadena lateral tiende a disminuir la potencia agonista sobre CB1, lo que ayuda a explicar por qué la THCV presenta un perfil farmacológico distinto al del THC. En modelos experimentales, los cannabinoides con cadenas laterales más cortas muestran una menor eficacia en la activación del receptor, e incluso pueden comportarse como antagonistas funcionales en determinadas condiciones. (Pertwee, 2008)
La THCV presenta además estereoquímica específica, con centros quirales que influyen en su actividad biológica. La configuración natural en la planta corresponde a la forma (−)-trans, que es la que se ha asociado con la mayor parte de la actividad farmacológica descrita en estudios preclínicos. Como ocurre con otros fitocannabinoides, la relación entre estereoquímica y actividad es un elemento crítico en la comprensión de su interacción con receptores y enzimas del sistema endocannabinoide. (Mechoulam & Hanus, 2000)
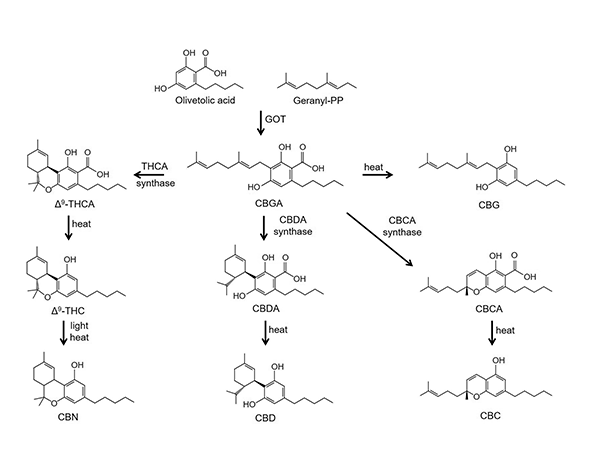
A nivel biosintético, la THCV deriva del ácido tetrahidrocannabivarínico (THCVA) mediante un proceso de descarboxilación inducido por calor o envejecimiento. El THCVA, a su vez, se forma a partir de la condensación de geranil pirofosfato (GPP) con ácido divarínico, en contraste con la ruta clásica del THC que utiliza ácido olivetólico. Esta diferencia en los precursores explica la existencia de dos grandes familias de fitocannabinoides: los de tipo pentilo y los de tipo propilo o varínico. (Citti et al., 2019)
En conjunto, la estructura química de la THCV ilustra cómo modificaciones sutiles en la arquitectura molecular de los cannabinoides pueden traducirse en cambios relevantes en su comportamiento farmacológico, reforzando la importancia de la relación estructura-actividad dentro del estudio del sistema endocannabinoide y sus ligandos. (Di Marzo, 2018)
Distribución y biosíntesis en la planta
La tetrahidrocannabivarina (THCV) se encuentra en Cannabis sativa como parte del grupo de los fitocannabinoides varínicos, cuya característica distintiva es la presencia de una cadena lateral propílica. Su distribución en la planta no es homogénea, concentrándose principalmente en los tricomas glandulares, estructuras epidérmicas especializadas responsables de la biosíntesis y acumulación de cannabinoides y terpenos. (Happyana et al., 2013; Livingston et al., 2020)
Desde el punto de vista quimiotaxonómico, la THCV aparece en concentraciones variables dependiendo de la genética de la planta. Se ha descrito una mayor presencia relativa en quimiovariedades de origen africano, especialmente en ciertas líneas sativa, lo que sugiere una base genética asociada a la expresión diferencial de enzimas implicadas en su biosíntesis. No obstante, en la mayoría de variedades comerciales su concentración suele ser baja en comparación con cannabinoides mayoritarios como el Δ9-THC o el CBD. (Citti et al., 2019; Berman et al., 2018)
La biosíntesis de la THCV sigue una ruta paralela a la del THC, pero con diferencias clave en los precursores. El proceso se inicia con la formación de ácido divarínico, que sustituye al ácido olivetólico utilizado en la vía clásica de cannabinoides pentílicos. Este ácido se condensa con geranil pirofosfato (GPP) para formar el ácido cannabigerovarínico (CBGVA), que actúa como intermediario central en la ruta biosintética de los cannabinoides varínicos. (Taura et al., 2007; Citti et al., 2019)
A partir del CBGVA, la acción de enzimas específicas, en particular la THCVA sintasa, conduce a la formación de ácido tetrahidrocannabivarínico (THCVA). Este compuesto representa la forma ácida precursora de la THCV y, como ocurre con otros fitocannabinoides, se convierte en su forma neutra mediante un proceso de descarboxilación inducido por factores como el calor, la luz o el envejecimiento del material vegetal. (Taura et al., 2007; Sirikantaramas et al., 2004)
La expresión de estas rutas biosintéticas está regulada tanto por factores genéticos como ambientales, incluyendo condiciones de cultivo, estrés abiótico y fase de desarrollo de la planta. En este contexto, la producción de THCV no solo depende de la presencia de genes codificantes para enzimas específicas, sino también de la disponibilidad de precursores metabólicos dentro de la vía policétida. (Livingston et al., 2020)
En conjunto, la distribución y biosíntesis de la THCV reflejan la complejidad metabólica de Cannabis sativa, donde múltiples rutas paralelas generan una diversidad de fitocannabinoides cuya abundancia relativa está determinada por la interacción entre genética, fisiología vegetal y condiciones ambientales. (Citti et al., 2019; Happyana et al., 2013)
Interacción con el sistema endocannabinoide
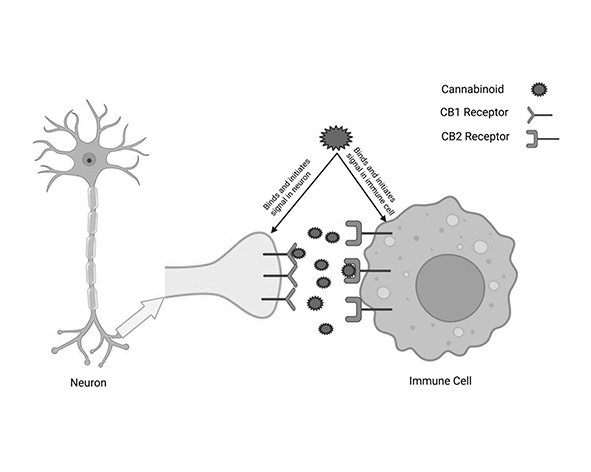
La tetrahidrocannabivarina (THCV) presenta un perfil de interacción con el sistema endocannabinoide que difiere de manera significativa del observado en otros fitocannabinoides como el Δ9-THC. Estas diferencias se deben, en gran medida, a su estructura química particular, especialmente a la longitud reducida de su cadena lateral, lo que condiciona su afinidad y eficacia en la activación de receptores cannabinoides. (Pertwee, 2008; Morales et al., 2017)
En relación con el receptor CB1, la THCV ha mostrado un comportamiento dependiente de la concentración y del sistema experimental. En estudios preclínicos, se ha descrito que a bajas concentraciones puede actuar como antagonista o modulador negativo, interfiriendo con la señalización inducida por agonistas como el Δ9-THC o endocannabinoides como la anandamida. Sin embargo, a concentraciones más elevadas, algunos trabajos sugieren la posibilidad de una actividad agonista parcial, lo que indica un perfil farmacológico no lineal. (Pertwee, 2008; Di Marzo, 2018)
Este comportamiento bifásico convierte a la THCV en un compuesto de interés para el estudio de la modulación fina de la señalización cannabinoide, ya que pone de manifiesto que la activación de CB1 no es un fenómeno binario, sino que puede ser modulada en intensidad y dirección dependiendo de múltiples variables, incluyendo la concentración del ligando y el contexto fisiológico. (Morales et al., 2017)
En el caso del receptor CB2, la evidencia disponible indica que la THCV puede actuar como agonista parcial, aunque con una eficacia inferior a la de otros fitocannabinoides. Este tipo de interacción sugiere una posible participación en procesos periféricos asociados al sistema endocannabinoide, si bien los mecanismos exactos y su relevancia fisiológica continúan en investigación. (Pertwee, 2008)
Más allá de los receptores cannabinoides clásicos, la THCV también ha sido estudiada en relación con otras dianas del denominado endocannabinoidoma, incluyendo canales iónicos y receptores acoplados a proteínas G no clásicos. Aunque la evidencia en este ámbito es aún limitada, estos hallazgos apuntan a un espectro de acción más amplio que podría contribuir a su perfil funcional diferenciado. (Di Marzo, 2018)
En conjunto, la interacción de la THCV con el sistema endocannabinoide ilustra cómo pequeñas variaciones estructurales pueden generar cambios relevantes en la farmacodinámica de los cannabinoides, reforzando la necesidad de analizar cada compuesto de forma individual en lugar de extrapolar propiedades a partir de analogías estructurales con el Δ9-THC. (Morales et al., 2017; Pertwee, 2008)
Farmacología
La tetrahidrocannabivarina (THCV) presenta un perfil farmacológico complejo que refleja tanto su interacción diferencial con los receptores cannabinoides como su capacidad para modular múltiples vías de señalización. A diferencia de otros fitocannabinoides más estudiados, su comportamiento no puede describirse mediante un único mecanismo de acción, sino que depende de variables como la concentración, el contexto biológico y el sistema experimental. (Pertwee, 2008; Morales et al., 2017)
Uno de los aspectos más característicos de la THCV es su actividad sobre el receptor CB1, donde se ha descrito un comportamiento bifásico. En condiciones de baja concentración, actúa como antagonista o modulador negativo, reduciendo la activación inducida por agonistas como el Δ9-THC. Este efecto ha sido observado en modelos animales y sistemas in vitro, donde la THCV modula la señalización mediada por proteínas G asociadas a CB1. A concentraciones más elevadas, algunos estudios sugieren una posible actividad agonista parcial, aunque este efecto no es uniforme y depende del modelo utilizado. (Pertwee, 2008; Di Marzo, 2018)
En relación con el receptor CB2, la THCV ha mostrado una actividad agonista parcial, con menor eficacia que otros cannabinoides. Este perfil sugiere una posible implicación en procesos periféricos regulados por CB2, aunque la relevancia fisiológica de esta interacción continúa siendo objeto de investigación. (Pertwee, 2008)
Desde el punto de vista farmacodinámico, la THCV también ha sido evaluada en modelos preclínicos en relación con funciones metabólicas, neurológicas y conductuales. Algunos estudios han explorado su papel en la modulación de la ingesta alimentaria, el metabolismo energético y la actividad locomotora, aunque estos efectos no son consistentes entre diferentes modelos y no permiten establecer conclusiones definitivas sobre su función en humanos. (Wargent et al., 2013; Riedel et al., 2009)
A nivel de dianas no clásicas, la THCV ha mostrado interacción con componentes del endocannabinoidoma, incluyendo canales iónicos y receptores no cannabinoides. Estas interacciones amplían su perfil farmacológico más allá de CB1 y CB2, sugiriendo que su actividad puede estar mediada por múltiples mecanismos simultáneos, aunque la evidencia disponible sigue siendo limitada y en muchos casos preliminar. (Di Marzo, 2018)
En términos de farmacocinética, los datos específicos sobre THCV son aún escasos en comparación con otros fitocannabinoides. Sin embargo, se asume que comparte características generales como su alta lipofilia, lo que influye en su distribución tisular y en su metabolismo hepático, presumiblemente mediado por enzimas del citocromo P450. (Morales et al., 2017)
En conjunto, la farmacología de la THCV pone de manifiesto la complejidad inherente al estudio de los fitocannabinoides, donde pequeñas diferencias estructurales pueden traducirse en perfiles funcionales significativamente distintos. Este carácter multifactorial refuerza la necesidad de abordar su estudio desde una perspectiva integradora que combine química, biología molecular y farmacología experimental. (Pertwee, 2008; Di Marzo, 2018)
Mecanismos moleculares
La tetrahidrocannabivarina (THCV) ejerce sus efectos a través de la modulación de múltiples vías de señalización intracelular, principalmente mediadas por receptores acoplados a proteínas G, aunque también involucra dianas no clásicas dentro del denominado endocannabinoidoma. Su perfil molecular está condicionado por su comportamiento diferencial sobre los receptores cannabinoides, especialmente CB1 y CB2, así como por su interacción con sistemas de señalización secundarios. (Pertwee, 2008; Di Marzo, 2018)
En el receptor CB1, la THCV ha mostrado capacidad para actuar como modulador negativo o antagonista funcional en determinadas condiciones. A nivel molecular, esto implica una reducción en la activación de proteínas Gi/o, lo que se traduce en una menor inhibición de la adenilato ciclasa y, por tanto, en una modulación de los niveles intracelulares de AMPc. Este efecto influye directamente en la actividad de múltiples rutas de señalización, incluyendo la fosforilación de proteínas dependientes de AMPc (PKA) y la regulación de canales iónicos. (Pertwee, 2008; Morales et al., 2017)
Además, la modulación de CB1 por THCV puede afectar la señalización retrógrada característica del sistema endocannabinoide, alterando la liberación de neurotransmisores en sinapsis específicas. Este fenómeno tiene implicaciones en la regulación de la excitabilidad neuronal y la plasticidad sináptica, aunque su relevancia funcional depende del contexto fisiológico y de la presencia de otros ligandos endógenos. (Di Marzo, 2018)
En relación con el receptor CB2, la THCV actúa como agonista parcial, activando vías de señalización también acopladas a proteínas Gi/o. Esto puede dar lugar a la modulación de cascadas intracelulares como la vía de las MAP quinasas (ERK1/2), implicadas en procesos de regulación celular, respuesta a estímulos y mantenimiento de la homeostasis tisular. (Pertwee, 2008)
Más allá de los receptores cannabinoides clásicos, la THCV ha sido estudiada en relación con otras dianas moleculares. Entre ellas destacan canales iónicos y receptores no cannabinoides, cuya modulación puede contribuir a efectos celulares adicionales. Aunque la evidencia es aún limitada, se ha propuesto que estos mecanismos podrían implicar cambios en la entrada de calcio intracelular, la actividad de canales TRP y la regulación de señales excitatorias e inhibitorias. (Di Marzo, 2018)
A nivel intracelular, la THCV también puede influir en procesos relacionados con la expresión génica, a través de la modulación indirecta de factores de transcripción dependientes de rutas como MAPK o AMPc. Estos efectos, aunque menos caracterizados, forman parte del impacto a largo plazo de la señalización cannabinoide en distintos tipos celulares. (Morales et al., 2017)
En conjunto, los mecanismos moleculares asociados a la THCV reflejan un patrón de señalización complejo y altamente dependiente del contexto biológico, en el que la modulación parcial o selectiva de receptores y vías intracelulares juega un papel central. Este comportamiento subraya la importancia de estudiar cada fitocannabinoide como una entidad funcional independiente dentro del sistema endocannabinoide ampliado. (Pertwee, 2008; Di Marzo, 2018)
Importancia en investigación científica
La tetrahidrocannabivarina (THCV) ha adquirido relevancia en investigación científica como modelo para estudiar la relación entre estructura química y actividad biológica dentro del sistema endocannabinoide. Su principal valor no reside en su abundancia en la planta, sino en su capacidad para ilustrar cómo modificaciones sutiles, como la reducción de la cadena lateral de pentilo a propilo, pueden traducirse en cambios significativos en la interacción con receptores y en la señalización intracelular. (Pertwee, 2008; Morales et al., 2017)
Uno de los aspectos más relevantes de la THCV en investigación es su comportamiento diferencial sobre el receptor CB1, especialmente su capacidad para actuar como modulador negativo o antagonista funcional en determinadas condiciones. Este perfil ha permitido explorar con mayor profundidad los mecanismos de regulación de la señalización cannabinoide, así como los efectos derivados de la inhibición parcial de CB1 frente a su activación completa. (Pertwee, 2008; Di Marzo, 2018)
Además, la THCV ha sido utilizada en estudios preclínicos orientados a comprender la complejidad del denominado endocannabinoidoma, un sistema ampliado que incluye no solo CB1 y CB2, sino también múltiples receptores, enzimas y mediadores lipídicos. En este contexto, la THCV contribuye a ampliar el conocimiento sobre la diversidad funcional de los fitocannabinoides y su interacción con diferentes dianas moleculares. (Di Marzo, 2018)
Desde una perspectiva farmacológica, la THCV también ha sido objeto de investigación en modelos experimentales relacionados con procesos metabólicos, neurológicos y conductuales. No obstante, los resultados disponibles son heterogéneos y, en muchos casos, limitados a estudios preclínicos, lo que refuerza la necesidad de interpretar estos datos con cautela y dentro de un marco estrictamente científico. (Wargent et al., 2013; Riedel et al., 2009)
Otro punto de interés radica en su papel como referencia dentro del estudio comparado de cannabinoides varínicos frente a sus homólogos pentílicos. Este enfoque permite analizar de forma sistemática cómo las variaciones estructurales afectan parámetros como la afinidad por receptores, la eficacia intrínseca y la selectividad funcional, aportando información clave para el desarrollo de modelos farmacológicos más precisos. (Citti et al., 2019)
En conjunto, la THCV se ha consolidado como un compuesto de interés en investigación básica y aplicada, no por su uso directo, sino por su capacidad para aportar conocimiento sobre la complejidad del sistema endocannabinoide y la diversidad funcional de los fitocannabinoides. Su estudio continúa contribuyendo a una comprensión más matizada de la señalización cannabinoide y de los factores que determinan la actividad biológica de estos compuestos. (Pertwee, 2008; Di Marzo, 2018)
Referencias
- Pertwee, R. G. (2008). The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids: Δ9-tetrahydrocannabinol, cannabidiol and Δ9-tetrahydrocannabivarin. British Journal of Pharmacology, 153(2), 199–215. - Morales, P., Reggio, P. H., & Jagerovic, N. (2017). An overview on medicinal chemistry of synthetic and natural derivatives of cannabidiol. Frontiers in Pharmacology, 8, 422. - Di Marzo, V. (2018). New approaches and challenges to targeting the endocannabinoid system. Nature Reviews Drug Discovery, 17(9), 623–639. - Citti, C., Linciano, P., Russo, F., Luongo, L., Iannotta, M., Maione, S., & Vandelli, M. A. (2019). A novel phytocannabinoid isolated from Cannabis sativa L. with an in vivo cannabimimetic activity higher than Δ9-tetrahydrocannabinol. Scientific Reports, 9, 20335. - Berman, P., Futoran, K., Lewitus, G. M., Mukha, D., Benami, M., Shlomi, T., Meiri, D., & Shabat, D. (2018). A new ESI-LC/MS approach for comprehensive metabolic profiling of phytocannabinoids in cannabis. Analytical Chemistry, 90(19), 11705–11713. - Taura, F., Morimoto, S., & Shoyama, Y. (2007). Purification and characterization of cannabidiolic-acid synthase from Cannabis sativa L. Journal of Biological Chemistry, 282(29), 20739–20745. - Sirikantaramas, S., Taura, F., Tanaka, Y., Ishikawa, Y., Morimoto, S., & Shoyama, Y. (2004). Tetrahydrocannabinolic acid synthase, the enzyme controlling marijuana psychoactivity, is secreted into the storage cavity of the glandular trichomes. Plant and Cell Physiology, 45(6), 741–747. - Happyana, N., Agnolet, S., Muntendam, R., van Dam, A., Schneider, B., & Kayser, O. (2013). Analysis of cannabinoids in laser-microdissected trichomes of Cannabis sativa using LCMS and cryogenic NMR. Phytochemistry, 87, 51–59. - Livingston, S. J., Quilichini, T. D., Booth, J. K., Wong, D. C. J., Rensing, K. H., Laflamme-Yonkman, J., Castellarin, S. D., Bohlmann, J., Page, J. E., & Samuels, A. L. (2020). Cannabis glandular trichomes alter morphology and metabolite content during flower maturation. The Plant Journal, 101(1), 37–56. - Wargent, E. T., Zaibi, M. S., Silvestri, C., Hislop, D. C., Stocker, C. J., Stott, C. G., Guy, G. W., Duncan, M., Di Marzo, V., & Cawthorne, M. A. (2013). The cannabinoid Δ9-tetrahydrocannabivarin (THCV) ameliorates insulin sensitivity in two mouse models of obesity. Nutrition & Diabetes, 3, e68. - Riedel, G., Fadda, P., McKillop-Smith, S., Pertwee, R. G., Platt, B., & Robinson, L. (2009). Synthetic and plant-derived cannabinoid receptor antagonists show hypophagic properties in fasted and non-fasted mice. British Journal of Pharmacology, 156(7), 1154–1166. - Mechoulam, R., & Gaoni, Y. (1972). The isolation and structure of Δ1-tetrahydrocannabinol and other neutral cannabinoids from hashish. Journal of the American Chemical Society, 94(17), 6159–6165. - Mechoulam, R., & Hanus, L. (2000). A historical overview of chemical research on cannabinoids. Chemistry and Physics of Lipids, 108(1–2), 1–13.