Introducción
El cannabicromeno (CBC) es uno de los principales fitocannabinoides identificados en Cannabis sativa L., perteneciente al grupo de compuestos derivados del ácido cannabigerólico (CBGA), considerado el precursor biosintético común de múltiples cannabinoides. Aunque durante décadas ha sido clasificado como un cannabinoide “menor” debido a su menor presencia en muchas variedades comerciales modernas, el CBC desempeña un papel relevante en la diversidad química de la planta y en la comprensión del funcionamiento del sistema endocannabinoide ampliado (endocannabinoidome) (DeLong et al., 2010; Pollastro et al., 2018).
A nivel estructural y funcional, el CBC presenta características diferenciadas respecto a otros fitocannabinoides más estudiados como el Δ9-tetrahidrocannabinol (THC) o el cannabidiol (CBD). En particular, su baja afinidad por los receptores cannabinoides clásicos CB1 y CB2, junto con su interacción con otras dianas moleculares como canales de la familia TRP, lo sitúan como un compuesto de interés para explorar mecanismos de señalización no canónicos dentro del sistema endocannabinoide (Ligresti et al., 2006; Cascio & Pertwee, 2014).
En los últimos años, el creciente interés por los cannabinoides menos abundantes ha impulsado nuevas investigaciones sobre el CBC, especialmente en modelos preclínicos que analizan su papel en la modulación de procesos celulares complejos. Este cambio de enfoque refleja una evolución en la investigación del cannabis, que ha pasado de centrarse en compuestos individuales a estudiar la interacción entre múltiples moléculas y su contribución conjunta a los perfiles farmacológicos observados en extractos vegetales complejos (Izzo et al., 2009).
Historia del descubrimiento
El cannabicromeno (CBC) fue identificado por primera vez durante la década de 1960 en el marco de los estudios sistemáticos sobre la composición química de Cannabis sativa L., un periodo caracterizado por el aislamiento y elucidación estructural de los principales fitocannabinoides. Estos trabajos, liderados por grupos de investigación en Estados Unidos e Israel, permitieron establecer las bases de la química del cannabis moderna, incluyendo la identificación de Δ9-tetrahidrocannabinol (THC), cannabidiol (CBD) y otros cannabinoides estructuralmente relacionados como el CBC (Gaoni & Mechoulam, 1966).
A diferencia del THC, cuya actividad psicotrópica impulsó gran parte del interés científico inicial, el CBC no mostró efectos psicoactivos evidentes, lo que contribuyó a que su estudio quedara en un segundo plano durante décadas. Esta menor prioridad investigadora se vio reforzada por la tendencia a centrar la investigación en compuestos con efectos farmacológicos más inmediatos o clínicamente evidentes, relegando a cannabinoides como el CBC a un papel secundario dentro del perfil fitoquímico del cannabis (ElSohly et al., 2005).
No obstante, a medida que avanzó la caracterización analítica de los extractos de cannabis, se observó que el CBC podía estar presente en concentraciones significativas en determinadas quimiovariedades, especialmente en fases específicas del desarrollo de la planta o en genotipos particulares. Este hallazgo contribuyó a replantear su consideración como cannabinoide menor y a integrarlo dentro de la complejidad química global de la planta (DeLong et al., 2010).
En las últimas décadas, el interés por el CBC ha resurgido en paralelo al desarrollo del concepto de endocannabinoidome, que amplía el marco clásico del sistema endocannabinoide e incorpora múltiples dianas moleculares adicionales. Este nuevo paradigma ha favorecido la reevaluación de fitocannabinoides previamente infraestudiados, situando al CBC como un compuesto relevante para comprender la diversidad funcional y la plasticidad de los sistemas de señalización asociados al cannabis (Cascio & Pertwee, 2014).
Estructura química
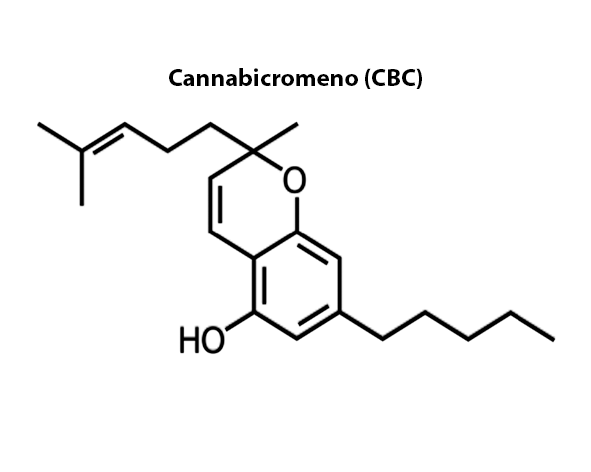
El cannabicromeno (CBC) es un fitocannabinoide de naturaleza lipofílica cuya estructura deriva biosintéticamente del ácido cannabigerólico (CBGA), precursor común de los principales cannabinoides presentes en Cannabis sativa L.. Su fórmula molecular es C₂₁H₃₀O₂, compartida con otros fitocannabinoides como el cannabidiol (CBD) o el Δ9-tetrahidrocannabinol (THC), aunque presenta diferencias estructurales clave en la organización de su sistema de anillos, lo que determina un comportamiento farmacológico diferenciado (Pollastro et al., 2018).
Desde un punto de vista estructural, el CBC se caracteriza por un sistema tricíclico abierto, en contraste con el sistema bicíclico del CBD o el anillo cerrado característico del THC. Esta configuración se origina durante la conversión enzimática del CBGA a ácido cannabicroménico (CBCA) mediante la acción de la CBCA sintasa, seguida de su descarboxilación a CBC neutro. La ausencia de un anillo piránico cerrado, como ocurre en el THC, es uno de los factores determinantes de su baja afinidad por el receptor CB1 y, por tanto, de la ausencia de efectos psicotrópicos (Taura et al., 2007).
La estructura del CBC incluye:
- Una cadena lateral pentílica, común a muchos fitocannabinoides
- Grupos funcionales fenólicos responsables de su reactividad química
- Un sistema de anillos que condiciona su interacción con membranas biológicas
Estas características confieren al CBC una elevada afinidad por entornos lipídicos, facilitando su inserción en membranas celulares y su interacción con proteínas de membrana, como canales iónicos y receptores acoplados a proteínas G. A diferencia de otros cannabinoides con afinidad más definida por receptores CB1 o CB2, la conformación estructural del CBC favorece interacciones más distribuidas y menos selectivas, lo que se traduce en un perfil farmacológico más difuso y dependiente del contexto celular (Cascio & Pertwee, 2014).
Además, la relativa flexibilidad conformacional del CBC, derivada de su estructura menos rigidizada, puede influir en su capacidad para modular múltiples dianas moleculares dentro del endocannabinoidome, lo que refuerza su interés como compuesto modelo en el estudio de interacciones no canónicas de los fitocannabinoides (Ligresti et al., 2006).
Distribución y biosíntesis en la planta
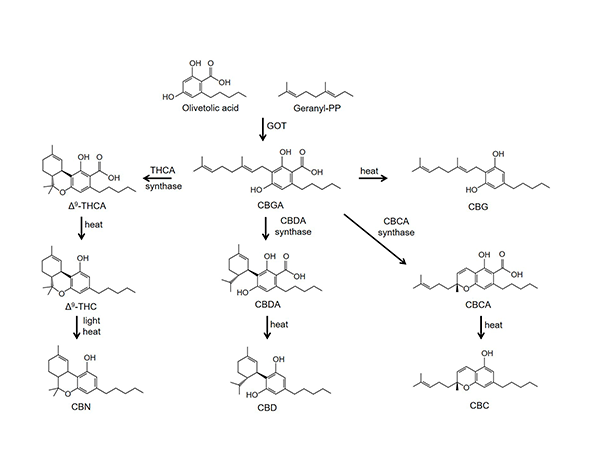
El cannabicromeno (CBC) se origina a partir del ácido cannabicroménico (CBCA), uno de los principales derivados biosintéticos del ácido cannabigerólico (CBGA), que actúa como nodo central en la ruta metabólica de los fitocannabinoides. Esta transformación está catalizada por la enzima CBCA sintasa, una oxidociclasa dependiente de flavina que dirige la ciclación oxidativa del CBGA hacia la formación de CBCA, en competencia directa con otras sintasas como la THCA sintasa y la CBDA sintasa. Este punto de ramificación metabólica es clave para entender la variabilidad en la composición cannabinoide entre distintas quimiovariedades de Cannabis sativa L. (Taura et al., 2007; Sirikantaramas et al., 2005).
La biosíntesis de CBCA tiene lugar principalmente en los tricomas glandulares capitados, estructuras epidérmicas especializadas que actúan como centros de producción y almacenamiento de metabolitos secundarios. En estas estructuras, el CBGA se sintetiza a partir de la condensación de olivetolato y geranil pirofosfato (GPP), catalizada por la preniltransferasa correspondiente, para posteriormente ser canalizado hacia diferentes rutas enzimáticas que dan lugar a los ácidos cannabinoides específicos (Gagne et al., 2012).
Tras su formación, el CBCA puede acumularse en la matriz resinosa de los tricomas y, bajo condiciones de calor, luz o envejecimiento, sufre un proceso de descarboxilación no enzimática que da lugar al cannabicromeno (CBC) en su forma neutra. Este proceso es análogo al observado en otros cannabinoides, aunque la eficiencia y cinética de descarboxilación pueden variar en función de factores ambientales y del estado fisiológico del tejido vegetal (Citti et al., 2018).
Desde un punto de vista cuantitativo, la concentración de CBC en la planta es altamente variable. En muchas variedades modernas seleccionadas por su contenido en THC o CBD, el CBC suele encontrarse en niveles relativamente bajos. Sin embargo, en quimiotipos menos manipulados o en líneas específicas, puede alcanzar concentraciones significativamente más elevadas, lo que sugiere que su papel biosintético y ecológico podría haber sido infraestimado en programas de selección centrados en cannabinoides mayoritarios (ElSohly et al., 2005).
Además, estudios metabolómicos han mostrado que el CBC puede estar presente en proporciones más altas en fases tempranas del desarrollo floral, lo que sugiere que su producción podría estar asociada a funciones fisiológicas específicas durante el crecimiento de la planta, como la defensa frente a estrés ambiental o la interacción con microorganismos (Happyana et al., 2013).
En conjunto, la distribución del CBC no debe interpretarse únicamente en términos de abundancia absoluta, sino como parte de una red biosintética dinámica en la que múltiples enzimas, factores genéticos y condiciones ambientales determinan el perfil final de fitocannabinoides. Este enfoque resulta esencial para comprender la complejidad química del cannabis y la variabilidad observada entre extractos vegetales aparentemente similares.
Interacción con el sistema endocannabinoide
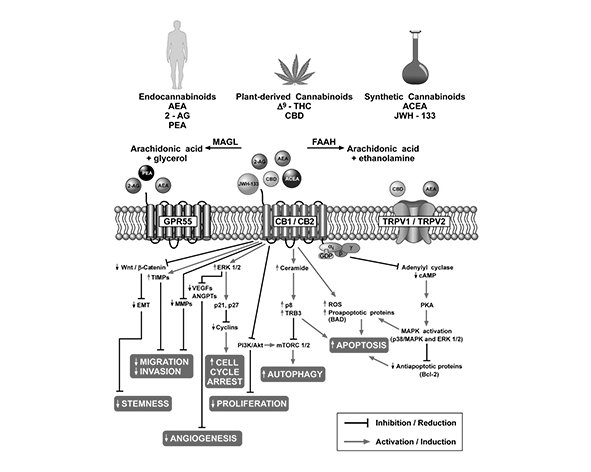
El cannabicromeno (CBC) presenta un perfil de interacción singular dentro del sistema endocannabinoide, caracterizado por una baja afinidad directa por los receptores cannabinoides clásicos CB1 y CB2, lo que lo diferencia de otros fitocannabinoides como el Δ9-tetrahidrocannabinol (THC). Esta limitada interacción con CB1 explica la ausencia de efectos psicotrópicos, mientras que su actividad sobre CB2 parece ser más relevante en determinados contextos celulares, aunque con una potencia moderada y dependiente del modelo experimental (DeLong et al., 2010).
A pesar de esta afinidad reducida por los receptores canónicos, el CBC ha demostrado interactuar de forma significativa con otros componentes del denominado endocannabinoidome, un sistema ampliado que incluye múltiples dianas moleculares más allá de CB1 y CB2. Entre estas, destacan los canales iónicos de la familia de potencial receptor transitorio (TRP), particularmente TRPV1 y TRPA1, que participan en la transducción de señales químicas y térmicas a nivel celular (Ligresti et al., 2006).
La activación de TRPV1 por CBC resulta especialmente relevante desde un punto de vista fisiológico, ya que este canal está implicado en procesos de señalización nociceptiva y regulación del calcio intracelular. La interacción con TRPA1, por su parte, sugiere una posible implicación en la detección de estímulos químicos y en la modulación de respuestas celulares frente a estrés ambiental. Estas interacciones sitúan al CBC dentro de un grupo de fitocannabinoides capaces de modular sistemas sensoriales a través de mecanismos no mediados por receptores cannabinoides clásicos (Cascio & Pertwee, 2014).
Adicionalmente, se ha propuesto que el CBC puede influir de manera indirecta en el tono endocannabinoide mediante la modulación de los niveles de endocannabinoides endógenos, como la anandamida (AEA). Este efecto podría estar relacionado con la inhibición de su recaptación o degradación, aunque los mecanismos específicos aún no están completamente definidos y continúan siendo objeto de investigación (Rock et al., 2012).
Otro aspecto relevante es la posible interacción del CBC con receptores acoplados a proteínas G no clásicos, como GPR55, así como con otras dianas moleculares implicadas en la señalización intracelular. Estas interacciones reflejan la naturaleza pleiotrópica del CBC, cuya actividad biológica no se limita a un único receptor, sino que emerge de la integración de múltiples vías de señalización distribuidas en diferentes tipos celulares.
En conjunto, el perfil de interacción del CBC pone de manifiesto la complejidad funcional del sistema endocannabinoide ampliado, donde compuestos con baja afinidad por los receptores clásicos pueden desempeñar un papel relevante a través de mecanismos alternativos. Este enfoque resulta clave para comprender la diversidad de efectos observados en extractos de cannabis y la contribución específica de cannabinoides menos estudiados dentro de estos sistemas biológicos complejos.
Farmacología
El perfil farmacológico del cannabicromeno (CBC) se caracteriza por una actividad multifactorial y no canónica, en la que predominan las interacciones con dianas moleculares distintas a los receptores cannabinoides clásicos. Esta característica lo sitúa dentro de un grupo de fitocannabinoides cuya acción no puede explicarse mediante modelos farmacológicos tradicionales basados en afinidad y eficacia sobre CB1 o CB2, sino que requiere un enfoque más amplio que integre múltiples sistemas de señalización (Cascio & Pertwee, 2014).
A nivel experimental, el CBC ha mostrado actividad en diversos modelos preclínicos, particularmente en estudios in vitroy en animales, donde se ha observado su capacidad para modular procesos celulares relacionados con la señalización neuronal, la regulación del calcio intracelular y la expresión de mediadores inflamatorios. Sin embargo, estos efectos deben interpretarse dentro de las limitaciones inherentes a estos modelos, ya que la evidencia en humanos sigue siendo limitada y no permite establecer conclusiones clínicas definitivas (Izzo et al., 2009).
Uno de los aspectos más relevantes del CBC es su capacidad para actuar sobre canales iónicos de la familia TRP, especialmente TRPV1 y TRPA1, lo que lo vincula con procesos de señalización sensorial y respuesta celular a estímulos físicos y químicos. La activación de estos canales puede desencadenar cambios en la concentración intracelular de calcio, afectando a múltiples rutas de señalización downstream, incluyendo vías dependientes de proteínas quinasas como MAPK (Ligresti et al., 2006).
Además, el CBC ha demostrado actuar como agonista selectivo de CB2 en determinados contextos experimentales, lo que sugiere una posible implicación en sistemas periféricos e inmunológicos. Esta actividad, aunque menos potente que la de otros cannabinoides, refuerza la idea de que el CBC puede contribuir a la modulación de procesos biológicos complejos a través de mecanismos indirectos o complementarios (DeLong et al., 2010).
Otro aspecto farmacológico relevante es su posible influencia sobre el sistema endocannabinoide endógeno, particularmente en la modulación de niveles de anandamida (AEA). Se ha propuesto que el CBC podría alterar la disponibilidad de este endocannabinoide mediante mecanismos relacionados con su transporte o degradación, aunque estos procesos aún no están completamente caracterizados (Rock et al., 2012).
Desde una perspectiva más amplia, el CBC debe considerarse dentro del contexto de formulaciones multicomponente, donde su contribución farmacológica no depende únicamente de su actividad individual, sino de su interacción con otros fitocannabinoides, terpenos y compuestos presentes en el extracto vegetal. Este enfoque es especialmente relevante en el estudio de extractos complejos, donde la actividad global no puede atribuirse a un único compuesto aislado, sino a la interacción entre múltiples moléculas con diferentes dianas y mecanismos de acción (Pollastro et al., 2018).
En conjunto, el perfil farmacológico del CBC refleja la transición de un modelo centrado en receptores específicos hacia una visión más integradora de la señalización biológica, donde los fitocannabinoides actúan como moduladores de redes moleculares complejas. Este paradigma resulta fundamental para comprender la diversidad funcional del cannabis y la relevancia de compuestos menos estudiados dentro de este sistema.
Mecanismos moleculares
El cannabicromeno (CBC) actúa a través de una red de mecanismos moleculares complejos que reflejan su naturaleza pleiotrópica y su capacidad para interactuar con múltiples dianas celulares. A diferencia de los cannabinoides con afinidad marcada por receptores específicos, el CBC ejerce su actividad mediante la modulación integrada de canales iónicos, receptores acoplados a proteínas G y rutas de señalización intracelular, lo que dificulta su encaje en modelos farmacológicos clásicos (Cascio & Pertwee, 2014).
Uno de los mecanismos mejor caracterizados es su interacción con canales de la familia TRP, especialmente TRPV1 y TRPA1. La activación de estos canales conduce a un aumento en la concentración de calcio intracelular (Ca²⁺), lo que actúa como señal secundaria clave en múltiples procesos celulares. Este incremento de Ca²⁺ puede desencadenar cascadas de señalización que incluyen la activación de quinasas dependientes de calcio y la modulación de factores de transcripción (Ligresti et al., 2006).
En paralelo, el CBC ha mostrado capacidad para modular indirectamente la señalización mediada por receptores cannabinoides, particularmente CB2, donde puede comportarse como agonista débil o modulador funcional dependiendo del contexto celular. Esta interacción contribuye a la regulación de vías intracelulares asociadas a proteínas G, incluyendo la inhibición de la adenilato ciclasa y la modulación de niveles de AMPc (DeLong et al., 2010).
Otro mecanismo relevante es la influencia del CBC sobre el tono endocannabinoide, especialmente en relación con la anandamida (AEA). Se ha propuesto que el CBC podría interferir en los procesos de recaptación o degradación de este endocannabinoide, lo que resultaría en un aumento de su disponibilidad local y, por tanto, en una amplificación indirecta de la señalización endocannabinoide. Aunque este mecanismo no está completamente dilucidado, representa una vía potencial de regulación moduladora más que de activación directa (Rock et al., 2012).
A nivel intracelular, el CBC puede influir en rutas de señalización como:
- MAPK/ERK, implicadas en proliferación y supervivencia celular
- PI3K/Akt, relacionadas con procesos de crecimiento y regulación metabólica
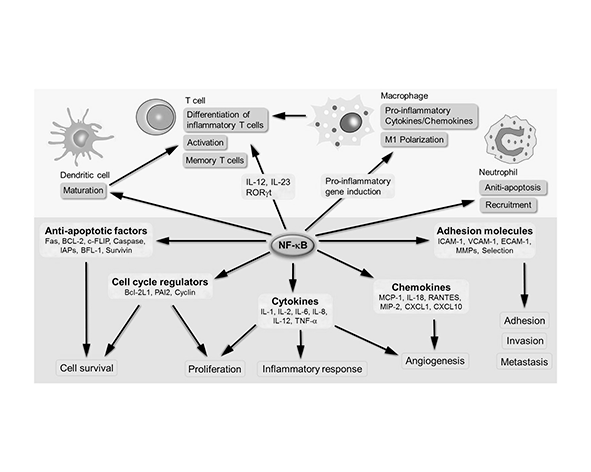
- NF-κB, asociadas a la regulación de la expresión génica en respuesta a estímulos celulares
Estas vías no actúan de forma aislada, sino que están interconectadas en redes dinámicas donde señales provenientes de distintos receptores y canales convergen y se integran. En este contexto, el CBC actúa como un modulador de estas redes más que como un activador lineal de una única vía (Cascio & Pertwee, 2014).
Además, se ha sugerido la posible implicación de receptores no clásicos como GPR55, así como la interacción con componentes lipídicos de la membrana celular, lo que podría influir en la organización de microdominios lipídicos (lipid rafts) y, en consecuencia, en la señalización celular global.
En conjunto, los mecanismos moleculares del CBC ponen de manifiesto un patrón de acción distribuido y dependiente del contexto, donde la actividad biológica emerge de la integración de múltiples interacciones a nivel celular. Este comportamiento refuerza la necesidad de abordar el estudio de los fitocannabinoides desde una perspectiva sistémica, alejada de modelos simplificados basados en un único receptor o mecanismo dominante.
Importancia en investigación científica
El cannabicromeno (CBC) ha emergido en los últimos años como un fitocannabinoide de interés estratégico dentro de la investigación en cannabis, no tanto por su abundancia o potencia individual, sino por su valor como modelo para estudiar la diversidad funcional del endocannabinoidome. Su perfil farmacológico atípico, caracterizado por una baja afinidad por los receptores CB1 y CB2 y una mayor interacción con dianas no canónicas, lo convierte en una herramienta relevante para explorar mecanismos de señalización alternativos (Cascio & Pertwee, 2014).
En este contexto, el CBC permite ampliar la comprensión del sistema endocannabinoide más allá del paradigma clásico centrado en CB1/CB2, facilitando el estudio de redes moleculares complejas donde intervienen canales iónicos, receptores huérfanos y vías intracelulares interconectadas. Este enfoque resulta especialmente útil en un momento en el que la investigación biomédica tiende a integrar modelos de señalización sistémicos en lugar de aproximaciones reduccionistas (Ligresti et al., 2006).
Además, el CBC ha sido incorporado en estudios que analizan formulaciones multicomponente, donde se evalúa la interacción entre distintos fitocannabinoides y otros metabolitos secundarios del cannabis. En estos sistemas, su contribución no debe interpretarse de forma aislada, sino como parte de una matriz química compleja en la que múltiples compuestos pueden influir de manera conjunta sobre diferentes dianas biológicas. Este tipo de aproximación es clave para entender la variabilidad observada entre extractos vegetales y la dificultad de atribuir efectos a un único componente (Pollastro et al., 2018).
Desde un punto de vista metodológico, el CBC también ha sido utilizado como referencia en estudios comparativos entre cannabinoides, permitiendo identificar similitudes y diferencias en afinidad, eficacia y mecanismos de acción. Estos trabajos han contribuido a redefinir la clasificación funcional de los fitocannabinoides, alejándola de criterios basados exclusivamente en la psicoactividad o en la interacción con CB1 (Izzo et al., 2009).
Por otra parte, el creciente interés por cannabinoides menos abundantes ha impulsado el desarrollo de técnicas analíticas más precisas, incluyendo métodos cromatográficos y espectrométricos capaces de detectar y cuantificar compuestos minoritarios como el CBC con mayor fiabilidad. Este avance ha permitido integrar de forma más rigurosa estos cannabinoides en estudios metabolómicos y farmacológicos (ElSohly et al., 2005).
En conjunto, la relevancia del CBC en investigación no radica únicamente en sus efectos específicos, sino en su capacidad para expandir el marco conceptual del estudio del cannabis, contribuyendo a una visión más completa, compleja y realista de los sistemas biológicos en los que intervienen los fitocannabinoides. Su estudio refleja, en última instancia, la transición hacia una ciencia del cannabis basada en la integración de múltiples niveles de análisis, desde la química estructural hasta la señalización celular y la fisiología sistémica.
Referencias
- Gaoni, Y., & Mechoulam, R. (1966). Isolation, structure, and partial synthesis of an active constituent of hashish. Journal of the American Chemical Society, 88(8), 1646–1647. - DeLong, G. T., Wolf, C. E., Poklis, A., & Lichtman, A. H. (2010). Pharmacological evaluation of the natural constituent of Cannabis sativa, cannabichromene and its modulation by Δ9-tetrahydrocannabinol. Drug and Alcohol Dependence, 112(1–2), 126–133. - Izzo, A. A., Borrelli, F., Capasso, R., Di Marzo, V., & Mechoulam, R. (2009). Non-psychotropic plant cannabinoids: new therapeutic opportunities from an ancient herb. Trends in Pharmacological Sciences, 30(10), 515–527. - Ligresti, A., Moriello, A. S., Starowicz, K., Matias, I., Pisanti, S., De Petrocellis, L., & Di Marzo, V. (2006). Antitumor activity of plant cannabinoids with emphasis on the effect of cannabidiol on human breast carcinoma. Journal of Pharmacology and Experimental Therapeutics, 318(3), 1375–1387. - Cascio, M. G., & Pertwee, R. G. (2014). Known pharmacological actions of cannabinoids in the central nervous system. Handbook of Experimental Pharmacology, 231, 1–36. - Pollastro, F., Taglialatela-Scafati, O., Allarà, M., Muñoz, E., Di Marzo, V., & De Petrocellis, L. (2018). Bioactive prenylogous cannabinoids from fiber hemp (Cannabis sativa). Journal of Natural Products, 81(12), 2647–2656. - Rock, E. M., Limebeer, C. L., Parker, L. A. (2012). Effect of cannabinoids on neurogenesis and neuroinflammation. British Journal of Pharmacology, 167(8), 1599–1610. - Taura, F., Sirikantaramas, S., Shoyama, Y., Yoshikai, K., Shoyama, Y., & Morimoto, S. (2007). Cannabidiolic-acid synthase, the chemotype-determining enzyme in the fiber-type Cannabis sativa. FEBS Letters, 581(16), 2929–2934. - ElSohly, M. A., Mehmedic, Z., Foster, S., Gon, C., Chandra, S., & Church, J. C. (2005). Changes in cannabis potency over the last two decades. Journal of Forensic Sciences, 50(4), 1–5. - Gagne, S. J., Stout, J. M., Liu, E., Boubakir, Z., Clark, S. M., & Page, J. E. (2012). Identification of olivetolic acid cyclase from Cannabis sativa reveals a unique catalytic route to plant polyketides. Proceedings of the National Academy of Sciences, 109(31), 12811–12816. - Happyana, N., Agnolet, S., Muntendam, R., van Dam, A., Schneider, B., & Kayser, O. (2013). Analysis of cannabinoids in laser-microdissected trichomes of medicinal Cannabis sativa using LC-MS and NMR. Analytical and Bioanalytical Chemistry, 405(15), 4969–4976. - Sirikantaramas, S., Taura, F., Morimoto, S., & Shoyama, Y. (2005). Recent advances in Cannabis sativa research: biosynthetic studies of cannabinoids. Current Pharmaceutical Biotechnology, 6(3), 201–210.