Introducción
El Δ9-tetrahidrocannabinol (THC) es el principal fitocannabinoide psicoactivo presente en la planta Cannabis sativa L. y uno de los compuestos más estudiados dentro del sistema endocannabinoide. Desde el punto de vista químico, pertenece a la familia de los cannabinoides terpenofenólicos derivados del ácido cannabigerólico (CBGA), y su naturaleza altamente lipofílica le permite atravesar con facilidad las membranas biológicas, incluida la barrera hematoencefálica, lo que condiciona su actividad en el sistema nervioso central. (Pertwee, 2008; ElSohly et al., 2017)
A nivel farmacológico, el THC actúa como agonista parcial de los receptores cannabinoides CB1 y CB2, con una afinidad especialmente relevante por CB1, que se expresa de forma abundante en regiones cerebrales implicadas en funciones como la memoria, la percepción, la coordinación motora y la regulación emocional. La activación de estos receptores modula la liberación de neurotransmisores mediante mecanismos de señalización retrógrada, alterando la actividad sináptica en múltiples circuitos neuronales. (Howlett et al., 2002; Castillo et al., 2012)
A diferencia de los endocannabinoides, que se sintetizan de forma local y transitoria en respuesta a estímulos fisiológicos, el THC actúa como un ligando exógeno que puede desajustar temporalmente la señalización endocannabinoide. Sus efectos dependen de factores como la dosis, la vía de administración, la tolerancia individual y el contexto fisiológico, lo que refleja la complejidad de su interacción con los sistemas biológicos. (Lu & Mackie, 2016; Zou & Kumar, 2018)
Desde una perspectiva histórica, el aislamiento y la caracterización estructural del THC marcaron un punto de inflexión en la investigación sobre cannabinoides, sentando las bases para el descubrimiento posterior de los receptores CB1 y CB2, así como de los endocannabinoides. Este avance permitió definir el sistema endocannabinoide como un sistema de señalización biológica fundamental en la regulación de la homeostasis. (Mechoulam & Gaoni, 1964; Devane et al., 1992)
Historia del descubrimiento
El Δ9-tetrahidrocannabinol (THC) fue aislado e identificado por primera vez en 1964 por el químico Raphael Mechoulamy su colega Yehiel Gaoni en el Instituto Weizmann de Israel, a partir de extractos de resina de Cannabis sativa. Este trabajo representó el primer aislamiento exitoso del principal componente psicoactivo del cannabis y permitió, por primera vez, asociar de forma directa una molécula concreta con los efectos farmacológicos observados en humanos. (Mechoulam & Gaoni, 1964)
Antes de este descubrimiento, la investigación sobre cannabis estaba limitada por la falta de compuestos puros y por una comprensión incompleta de su composición química. Aunque el uso medicinal y recreativo del cannabis se remonta a miles de años en distintas culturas, no fue hasta mediados del siglo XX cuando las técnicas de química orgánica permitieron aislar y caracterizar sus principios activos con precisión estructural. (Russo, 2007)
La elucidación de la estructura química del THC marcó un punto de inflexión en la farmacología moderna, ya que abrió la puerta al estudio sistemático de los cannabinoides y sus efectos biológicos. Durante las décadas siguientes, este avance permitió el desarrollo de análogos sintéticos, estudios de relación estructura-actividad y, de forma crucial, la identificación de dianas moleculares específicas en el organismo. (Pertwee, 2006)
Uno de los hitos más relevantes derivados de este descubrimiento fue la identificación del receptor cannabinoide CB1 en 1990, seguido del CB2 en 1993, lo que llevó a la formulación del concepto de sistema endocannabinoide. Posteriormente, el hallazgo de ligandos endógenos como la anandamida y el 2-araquidonoilglicerol consolidó la idea de que el organismo dispone de un sistema de señalización propio que puede ser modulado por compuestos como el THC. (Matsuda et al., 1990; Munro et al., 1993; Devane et al., 1992)
En conjunto, el aislamiento del THC no solo permitió comprender los efectos del cannabis a nivel molecular, sino que también actuó como catalizador para el descubrimiento de uno de los sistemas de regulación fisiológica más relevantes en biología moderna: el sistema endocannabinoide. (Lu & Mackie, 2016)
Estructura química y propiedades fisicoquímicas
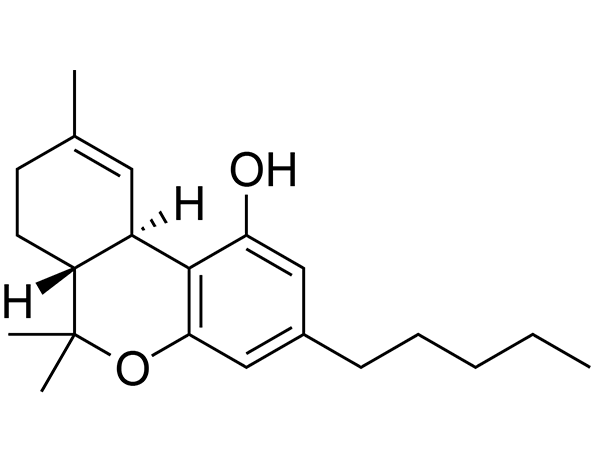
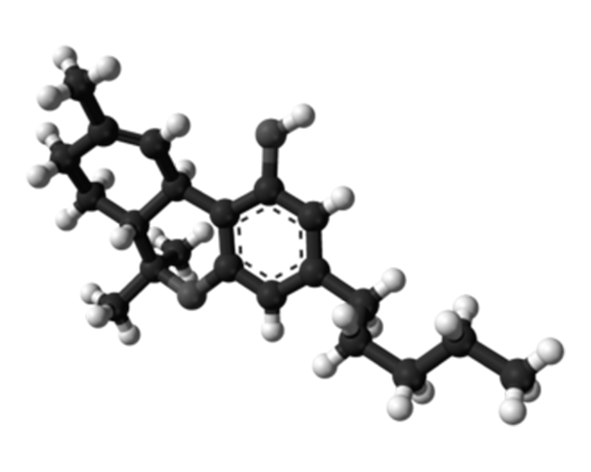
El Δ9-tetrahidrocannabinol (THC) es un compuesto de naturaleza terpenofenólica derivado biosintéticamente del ácido cannabigerólico (CBGA), precursor común de los principales fitocannabinoides. Su estructura química está compuesta por un sistema tricíclico que integra un anillo aromático fenólico, un anillo ciclohexénico y una cadena lateral pentílica, elementos clave que determinan su afinidad por los receptores cannabinoides y su comportamiento lipofílico. (ElSohly et al., 2017; Pertwee, 2008)
La configuración espacial del THC es un factor determinante en su actividad biológica. El isómero natural Δ9-THC presenta una orientación estereoquímica específica que permite su interacción con los receptores CB1 y CB2, mientras que otros isómeros, como el Δ8-THC, muestran diferencias en potencia y afinidad debido a variaciones en la posición del doble enlace dentro de la molécula. Esta relación entre estructura y actividad ha sido fundamental para comprender la farmacología de los cannabinoides. (Mechoulam et al., 1970; Razdan, 1986)
Desde el punto de vista fisicoquímico, el THC es altamente lipofílico y presenta una baja solubilidad en agua, lo que condiciona su absorción, distribución y almacenamiento en tejidos ricos en lípidos como el tejido adiposo y el sistema nervioso central. Esta propiedad contribuye a su biodisponibilidad variable y a su persistencia en el organismo, especialmente en exposiciones repetidas. (Huestis, 2007; Grotenhermen, 2003)
Además, el THC es una molécula relativamente inestable frente a factores ambientales como la luz, el oxígeno y la temperatura, pudiendo degradarse progresivamente a otros compuestos como el cannabinol (CBN). Esta degradación tiene implicaciones tanto en la conservación de productos derivados del cannabis como en la interpretación de perfiles químicos en estudios analíticos. (Ross & ElSohly, 1999)
En conjunto, las propiedades estructurales y fisicoquímicas del THC no solo determinan su interacción con el sistema endocannabinoide, sino que también condicionan su comportamiento farmacocinético y su estabilidad en distintos contextos biológicos y ambientales. (Pertwee, 2008)
Mecanismo de acción y señalización
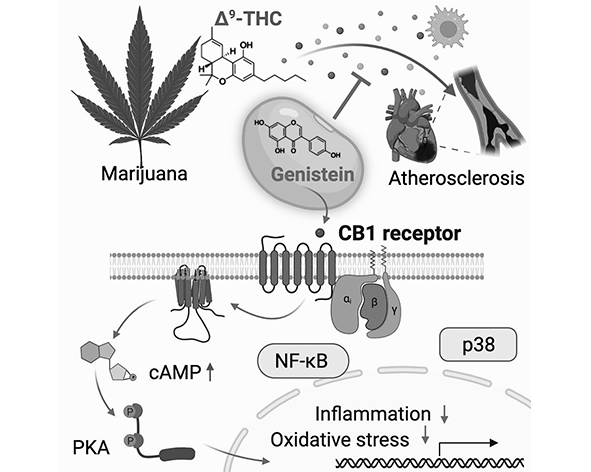
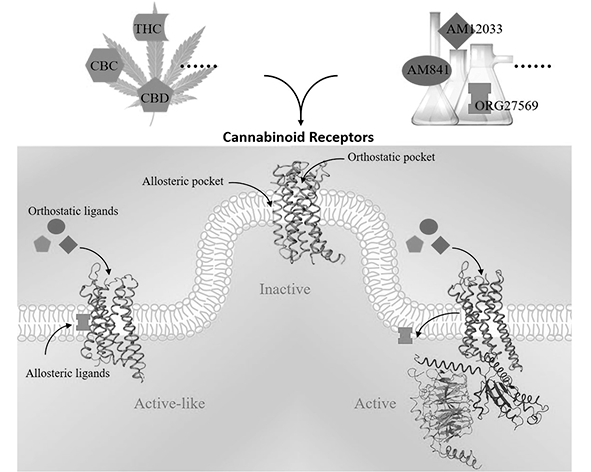
El Δ9-tetrahidrocannabinol (THC) ejerce sus efectos biológicos principalmente a través de la activación de los receptores cannabinoides CB1 y CB2, ambos pertenecientes a la familia de receptores acoplados a proteínas G (GPCR). El THC actúa como agonista parcial, lo que implica que su capacidad de activación depende del contexto celular y de la densidad de receptores, generando respuestas variables en función del tejido y las condiciones fisiológicas. (Howlett et al., 2002; Pertwee, 2008)
En el sistema nervioso central, la interacción del THC con el receptor CB1 conduce a la inhibición de la adenilato ciclasa mediante proteínas Gᵢ/ₒ, reduciendo los niveles intracelulares de AMPc y modulando múltiples cascadas de señalización intracelular. Este proceso se traduce en la regulación de canales iónicos, incluyendo la inhibición de canales de calcio dependientes de voltaje y la activación de canales de potasio, lo que disminuye la excitabilidad neuronal y la liberación de neurotransmisores. (Mackie, 2005; Castillo et al., 2012)
Uno de los mecanismos más relevantes asociados a la señalización cannabinoide es la modulación retrógrada de la sinapsis. En condiciones fisiológicas, los endocannabinoides son liberados desde la neurona postsináptica y actúan sobre receptores CB1 en la terminal presináptica para regular la liberación de neurotransmisores. El THC, al imitar esta señalización de forma exógena, puede alterar este equilibrio, modulando la liberación de glutamato, GABA y otros neurotransmisores clave en la función neuronal. (Kano et al., 2009; Lu & Mackie, 2016)
Además de la vía clásica mediada por proteínas G, el THC puede activar rutas adicionales de señalización intracelular, incluyendo la fosforilación de quinasas como MAPK/ERK, lo que sugiere efectos más amplios sobre procesos como la plasticidad neuronal, la expresión génica y la adaptación celular a largo plazo. Estos mecanismos contribuyen a la complejidad de sus efectos, tanto agudos como crónicos. (Bouaboula et al., 1995; Turu & Hunyady, 2010)
Aunque el THC presenta afinidad predominante por CB1, también puede interactuar con CB2, especialmente en células del sistema inmunológico, donde modula procesos relacionados con la respuesta inflamatoria y la señalización celular periférica. Sin embargo, su papel en estos contextos es más variable y dependiente de las condiciones fisiopatológicas. (Atwood & Mackie, 2010)
En conjunto, el THC actúa como un modulador exógeno del sistema endocannabinoide, interfiriendo en mecanismos de señalización diseñados para ser transitorios y localizados, lo que explica tanto su potencial como herramienta experimental como la complejidad de sus efectos en el organismo. (Zou & Kumar, 2018)
Distribución y farmacocinética
El Δ9-tetrahidrocannabinol (THC) presenta una farmacocinética compleja determinada en gran medida por su elevada lipofilia, lo que condiciona su absorción, distribución, metabolismo y eliminación en el organismo. La vía de administración es un factor crítico: la inhalación permite una absorción rápida a través del epitelio pulmonar, alcanzando concentraciones plasmáticas máximas en pocos minutos, mientras que la administración oral produce una absorción más lenta, irregular y sujeta a un intenso metabolismo de primer paso hepático. (Huestis, 2007; Grotenhermen, 2003)
Tras su entrada en el torrente sanguíneo, el THC se distribuye rápidamente hacia tejidos altamente perfundidos como el cerebro, el corazón, el hígado y los pulmones. Debido a su afinidad por los lípidos, también se acumula en tejido adiposo, desde donde puede liberarse de forma gradual, contribuyendo a su persistencia en el organismo incluso después de haber cesado la exposición. Esta redistribución explica en parte la duración variable de sus efectos y su detección prolongada en fluidos biológicos. (Huestis, 2007; Pertwee, 2008)
El metabolismo del THC ocurre principalmente en el hígado, mediado por enzimas del citocromo P450, especialmente CYP2C9 y CYP3A4. El principal metabolito activo es el 11-hidroxi-THC (11-OH-THC), que posee capacidad para atravesar la barrera hematoencefálica y contribuir a los efectos psicoactivos. Posteriormente, este metabolito se oxida a 11-nor-9-carboxi-THC (THC-COOH), una forma inactiva que constituye el principal producto de excreción. (Watanabe et al., 2007; Huestis, 2007)
La eliminación del THC y sus metabolitos se produce principalmente a través de las heces y, en menor medida, por vía urinaria. Sin embargo, debido a su almacenamiento en tejidos grasos, la liberación sostenida puede prolongar su presencia en el organismo durante días o incluso semanas en consumidores habituales, lo que tiene implicaciones tanto en estudios farmacocinéticos como en la interpretación de pruebas toxicológicas. (Grotenhermen, 2003; Huestis, 2007)
En conjunto, el comportamiento farmacocinético del THC refleja la interacción entre sus propiedades fisicoquímicas y los sistemas metabólicos del organismo, dando lugar a perfiles de exposición altamente variables que dependen de factores como la dosis, la frecuencia de uso, la vía de administración y las características individuales del sujeto. (Pertwee, 2008)
Efectos fisiológicos y cognitivos
Los efectos del Δ9-tetrahidrocannabinol (THC) derivan principalmente de su interacción con receptores CB1 en el sistema nervioso central, lo que modula múltiples funciones neurobiológicas. Entre los efectos más característicos se encuentran alteraciones en la percepción sensorial, cambios en el estado de ánimo, modificaciones en la memoria a corto plazo y variaciones en la coordinación motora. Estos efectos reflejan la distribución de los receptores CB1 en regiones cerebrales como el hipocampo, el cerebelo, los ganglios basales y la corteza prefrontal. (Iversen, 2003; Pertwee, 2008)
A nivel cognitivo, el THC puede interferir en procesos relacionados con la memoria de trabajo, la atención y la función ejecutiva, especialmente en exposiciones agudas o a dosis elevadas. Estos efectos están asociados a la modulación de la neurotransmisión glutamatérgica y GABAérgica en circuitos neuronales implicados en el procesamiento de la información. La magnitud de estas alteraciones depende de factores como la experiencia previa, la tolerancia y el contexto de consumo. (Ranganathan & D’Souza, 2006; Bossong & Niesink, 2010)
En el plano emocional, el THC puede inducir respuestas variables que van desde estados de relajación o euforia hasta sensaciones de inquietud o disforia, dependiendo de la dosis y de la susceptibilidad individual. Estas respuestas están relacionadas con la modulación de circuitos límbicos y con la liberación de neurotransmisores como la dopamina, que participan en la regulación del estado de ánimo y la motivación. (Volkow et al., 2014; Bloomfield et al., 2016)
Desde una perspectiva fisiológica, el THC también produce efectos periféricos, como cambios en la frecuencia cardíaca, la presión arterial y la percepción del tiempo, además de influir en la regulación del apetito y la respuesta al estrés. Estos efectos reflejan la presencia de receptores cannabinoides tanto en el sistema nervioso como en tejidos periféricos, integrando respuestas a nivel sistémico. (Benowitz & Jones, 1975; Pacher et al., 2006)
Es importante señalar que los efectos del THC no son uniformes ni universales, sino que dependen de una interacción compleja entre variables farmacológicas, biológicas y contextuales. Esta variabilidad subraya la necesidad de interpretar sus efectos dentro de un marco fisiológico amplio, evitando simplificaciones que no reflejan la complejidad de la señalización endocannabinoide. (Zou & Kumar, 2018)
Interacción con el sistema endocannabinoide
El Δ9-tetrahidrocannabinol (THC) interactúa directamente con el sistema endocannabinoide al actuar como un ligando exógeno capaz de unirse a los receptores cannabinoides CB1 y CB2, imitando en parte la acción de los endocannabinoides endógenos como la anandamida y el 2-araquidonoilglicerol (2-AG). Sin embargo, a diferencia de estos últimos, cuya síntesis y liberación están finamente reguladas en el espacio y el tiempo, el THC introduce una señal más prolongada y difusa que puede alterar el equilibrio fisiológico del sistema. (Lu & Mackie, 2016; Zou & Kumar, 2018)
En condiciones fisiológicas, los endocannabinoides se sintetizan “on demand” en la neurona postsináptica y actúan de forma retrógrada sobre receptores CB1 en la terminal presináptica para modular la liberación de neurotransmisores. El THC, al activar estos mismos receptores de manera sostenida, puede amplificar o distorsionar esta señalización, interfiriendo en procesos de regulación sináptica que normalmente son transitorios y altamente localizados. (Kano et al., 2009; Castillo et al., 2012)
Además, el THC no está sujeto a los mecanismos enzimáticos de degradación rápida que regulan a los endocannabinoides, como la FAAH en el caso de la anandamida o la MAGL para el 2-AG. Esta ausencia de control metabólico inmediato contribuye a una activación prolongada de los receptores cannabinoides, lo que puede modificar la dinámica de la señalización endocannabinoide y sus efectos fisiológicos. (Cravatt et al., 2001; Dinh et al., 2002)
La interacción del THC con el sistema endocannabinoide también puede inducir procesos de adaptación celular, como la desensibilización y la internalización de receptores CB1 tras exposiciones repetidas. Estos mecanismos reflejan la capacidad del organismo para ajustarse a la estimulación continua y están relacionados con fenómenos como la tolerancia farmacológica. (Breivogel et al., 1999; Hirvonen et al., 2012)
En conjunto, el THC actúa como un modulador exógeno que interfiere en un sistema diseñado para operar mediante señales precisas y temporales, lo que explica tanto su utilidad como herramienta de investigación como la complejidad de sus efectos a nivel fisiológico y neuronal. (Pertwee, 2008)
Relación estructura-actividad (SAR)
La actividad biológica del Δ9-tetrahidrocannabinol (THC) está estrechamente ligada a su estructura molecular, en particular a la longitud de su cadena lateral alquílica y a la conformación tridimensional de su sistema tricíclico. Estudios de relación estructura-actividad han demostrado que pequeñas modificaciones en la cadena lateral pueden alterar significativamente la afinidad por los receptores CB1 y CB2, siendo la cadena pentílica del THC especialmente relevante para su actividad psicoactiva. (Razdan, 1986; Pertwee, 2008)
La estereoquímica del THC también juega un papel fundamental en su interacción con los receptores cannabinoides. El isómero natural (−)-trans-Δ9-THC es el responsable de la mayor parte de la actividad farmacológica observada, mientras que otros isómeros presentan una afinidad reducida o perfiles funcionales distintos. Este fenómeno refleja la especificidad de la interacción ligando-receptor en el sistema endocannabinoide. (Mechoulam et al., 1970; Reggio, 2010)
Además, modificaciones estructurales en el núcleo fenólico o en la región terpénica han permitido desarrollar análogos sintéticos con perfiles farmacológicos diversos, lo que ha contribuido a entender mejor los determinantes moleculares de la actividad cannabinoide y a explorar nuevas dianas dentro del sistema endocannabinoide. (Pertwee, 2006)
Tolerancia y adaptación del sistema endocannabinoide
La exposición repetida al THC induce procesos de adaptación en el sistema endocannabinoide, particularmente a nivel de los receptores CB1. Entre estos mecanismos se incluyen la desensibilización funcional del receptor, su internalización y la reducción de su expresión en la membrana celular, lo que se traduce en una disminución progresiva de la respuesta biológica ante una misma dosis. (Breivogel et al., 1999; Hirvonen et al., 2012)
Estos procesos adaptativos reflejan la capacidad del sistema endocannabinoide para mantener la homeostasis frente a estímulos externos persistentes. La regulación a la baja de CB1 es especialmente relevante en regiones cerebrales implicadas en la cognición y la motivación, lo que puede modificar la respuesta del organismo a lo largo del tiempo. (Sim-Selley, 2003; Lu & Mackie, 2016)
Además, la tolerancia al THC no depende exclusivamente de cambios a nivel receptor, sino que también puede implicar adaptaciones en las vías de señalización intracelular y en la liberación de neurotransmisores, lo que contribuye a la complejidad de su perfil farmacológico en exposiciones prolongadas. (Turu & Hunyady, 2010)
Interacción con otros fitocannabinoides y el entorno químico
El THC no actúa de forma aislada en el contexto de la planta de Cannabis sativa, sino que coexiste con otros fitocannabinoides, terpenos y compuestos fenólicos que pueden modular su actividad. Este fenómeno, a menudo descrito como interacción entre compuestos, refleja la complejidad del fitocomplejo y su influencia en la señalización biológica. (Russo, 2011)
Por ejemplo, la presencia de cannabidiol (CBD) puede modificar algunos efectos del THC mediante mecanismos que incluyen la modulación alostérica de CB1, la interferencia en su metabolismo o la interacción con otras dianas moleculares. Estas interacciones no son lineales ni universales, sino dependientes de la proporción entre compuestos, la dosis y el contexto fisiológico. (Laprairie et al., 2015; Pertwee, 2008)
Asimismo, los terpenos presentes en la planta pueden influir en la farmacocinética y en la percepción subjetiva de los efectos, aunque los mecanismos específicos de estas interacciones siguen siendo objeto de investigación. Este conjunto de interacciones subraya la importancia de considerar el THC dentro de un sistema químico más amplio. (Russo, 2011)
Variabilidad individual y factores moduladores
La respuesta al THC presenta una alta variabilidad interindividual, influida por factores genéticos, fisiológicos y ambientales. Polimorfismos en genes relacionados con el sistema endocannabinoide, como los que codifican para el receptor CB1 o enzimas metabólicas, pueden modificar la sensibilidad al THC y su perfil de efectos. (Huestis, 2007; Zou & Kumar, 2018)
Factores como la edad, el sexo, la composición corporal y la experiencia previa también influyen en la respuesta al THC. Por ejemplo, la acumulación en tejido adiposo puede variar entre individuos, afectando su distribución y eliminación, mientras que la tolerancia adquirida modula la intensidad de los efectos observados. (Grotenhermen, 2003)
El contexto en el que se produce la exposición —incluyendo el entorno, el estado emocional y las expectativas del individuo— también desempeña un papel relevante en la experiencia subjetiva asociada al THC, reflejando la interacción entre factores biológicos y psicológicos. (Volkow et al., 2014)
Importancia en investigación y contexto científico
El Δ9-tetrahidrocannabinol (THC) ha desempeñado un papel fundamental como herramienta experimental en la investigación del sistema endocannabinoide y en la comprensión de los mecanismos de señalización neuronal. Su capacidad para activar de forma directa los receptores CB1 y CB2 permitió, en su momento, identificar estas dianas moleculares y caracterizar sus funciones en distintos tejidos, estableciendo las bases de la farmacología cannabinoide moderna. (Howlett et al., 2002; Pertwee, 2008)
El estudio del THC ha contribuido de manera decisiva al descubrimiento de los endocannabinoides, como la anandamida y el 2-araquidonoilglicerol (2-AG), al evidenciar la existencia de un sistema endógeno capaz de interactuar con este tipo de compuestos. Este avance no solo permitió definir el sistema endocannabinoide como un sistema fisiológico propio, sino que también abrió nuevas líneas de investigación en neurobiología, fisiología y regulación homeostática. (Devane et al., 1992; Mechoulam et al., 1995)
Además, el THC ha sido utilizado como modelo para el desarrollo de agonistas y antagonistas selectivos, facilitando el estudio de la relación entre estructura y actividad en los receptores cannabinoides. Estos trabajos han permitido diferenciar los efectos mediados por CB1 y CB2, así como explorar vías de señalización alternativas y posibles aplicaciones farmacológicas en distintos contextos experimentales. (Pertwee, 2006; Atwood & Mackie, 2010)
En el ámbito de la investigación traslacional, el THC ha servido como referencia para estudiar la interacción entre compuestos exógenos y sistemas de señalización endógenos, aportando información relevante sobre procesos como la plasticidad sináptica, la modulación del estrés, la regulación del apetito y la respuesta al entorno. No obstante, estos estudios se interpretan dentro de marcos experimentales controlados y no implican necesariamente efectos directos extrapolables a contextos clínicos. (Lu & Mackie, 2016; Zou & Kumar, 2018)
En conjunto, el THC no solo representa un compuesto de interés por sus efectos biológicos, sino también una herramienta clave que ha permitido desentrañar uno de los sistemas de regulación más complejos del organismo, consolidando su relevancia en el estudio de la biología integrativa y la señalización celular. (Pertwee, 2008)
Referencias
- Atwood, B. K., & Mackie, K. (2010). CB2: a cannabinoid receptor with an identity crisis. British Journal of Pharmacology, 160(3), 467–479. - Benowitz, N. L., & Jones, R. T. (1975). Cardiovascular effects of prolonged delta-9-tetrahydrocannabinol ingestion. Clinical Pharmacology & Therapeutics, 18(3), 287–297. - Bloomfield, M. A. P., Ashok, A. H., Volkow, N. D., & Howes, O. D. (2016). The effects of Δ9-tetrahydrocannabinol on the dopamine system. Nature Reviews Neuroscience, 17(6), 346–358. - Bouaboula, M., Perrachon, S., Milligan, L., et al. (1995). A selective inverse agonist for central cannabinoid receptor inhibits mitogen-activated protein kinase activation stimulated by insulin or insulin-like growth factor 1. Journal of Biological Chemistry, 270(23), 13973–13980. - Breivogel, C. S., Childers, S. R., Deadwyler, S. A., et al. (1999). Chronic delta9-tetrahydrocannabinol treatment produces a time-dependent loss of cannabinoid receptors and cannabinoid receptor-activated G proteins in rat brain. Journal of Neurochemistry, 73(6), 2447–2459. - Castillo, P. E., Younts, T. J., Chávez, A. E., & Hashimotodani, Y. (2012). Endocannabinoid signaling and synaptic function. Neuron, 76(1), 70–81. - Cravatt, B. F., Demarest, K., Patricelli, M. P., et al. (2001). Supersensitivity to anandamide and enhanced endogenous cannabinoid signaling in mice lacking fatty acid amide hydrolase. Proceedings of the National Academy of Sciences, 98(16), 9371–9376. - Devane, W. A., Hanus, L., Breuer, A., et al. (1992). Isolation and structure of a brain constituent that binds to the cannabinoid receptor. Science, 258(5090), 1946–1949. - Dinh, T. P., Freund, T. F., & Piomelli, D. (2002). A role for monoglyceride lipase in 2-arachidonoylglycerol inactivation. Chemical Physics of Lipids, 121(1–2), 149–158. - ElSohly, M. A., Gul, W., Wanas, A. S., et al. (2017). Cannabinoids in Cannabis: Chemistry and pharmacology. Progress in the Chemistry of Organic Natural Products, 103, 1–36. - Grotenhermen, F. (2003). Pharmacokinetics and pharmacodynamics of cannabinoids. Clinical Pharmacokinetics, 42(4), 327–360. - Hirvonen, J., Goodwin, R. S., Li, C. T., et al. (2012). Reversible and regionally selective downregulation of brain cannabinoid CB1 receptors in chronic cannabis smokers. Molecular Psychiatry, 17(6), 642–649. - Howlett, A. C., Barth, F., Bonner, T. I., et al. (2002). International Union of Pharmacology. XXVII. Classification of cannabinoid receptors. Pharmacological Reviews, 54(2), 161–202. - Huestis, M. A. (2007). Human cannabinoid pharmacokinetics. Chemical Biodiversity, 4(8), 1770–1804. - Iversen, L. (2003). Cannabis and the brain. Brain, 126(6), 1252–1270. - Kano, M., Ohno-Shosaku, T., Hashimotodani, Y., et al. (2009). Endocannabinoid-mediated control of synaptic transmission. Physiological Reviews, 89(1), 309–380. - Laprairie, R. B., Bagher, A. M., Kelly, M. E. M., & Denovan-Wright, E. M. (2015). Cannabidiol is a negative allosteric modulator of the cannabinoid CB1 receptor. British Journal of Pharmacology, 172(20), 4790–4805. - Lu, H. C., & Mackie, K. (2016). An introduction to the endogenous cannabinoid system. Biological Psychiatry, 79(7), 516–525. - Mackie, K. (2005). Cannabinoid receptors as therapeutic targets. Annual Review of Pharmacology and Toxicology, 45, 101–122. - Matsuda, L. A., Lolait, S. J., Brownstein, M. J., et al. (1990). Structure of a cannabinoid receptor and functional expression of the cloned cDNA. Nature, 346(6284), 561–564. - Mechoulam, R., & Gaoni, Y. (1964). A total synthesis of dl-Δ1-tetrahydrocannabinol. Journal of the American Chemical Society, 86(8), 1646–1647. - Mechoulam, R., Ben-Shabat, S., Hanus, L., et al. (1995). Identification of an endogenous 2-monoglyceride, present in canine gut, that binds to cannabinoid receptors. Biochemical Pharmacology, 50(1), 83–90. - Munro, S., Thomas, K. L., & Abu-Shaar, M. (1993). Molecular characterization of a peripheral receptor for cannabinoids. Nature, 365(6441), 61–65. - Pacher, P., Bátkai, S., & Kunos, G. (2006). The endocannabinoid system as an emerging target of pharmacotherapy. Pharmacological Reviews, 58(3), 389–462. - Pertwee, R. G. (2006). Cannabinoid pharmacology: the first 66 years. British Journal of Pharmacology, 147(S1), S163–S171. - Pertwee, R. G. (2008). The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids. British Journal of Pharmacology, 153(2), 199–215. - Razdan, R. K. (1986). Structure-activity relationships in cannabinoids. Pharmacological Reviews, 38(2), 75–149. - Reggio, P. H. (2010). Endocannabinoid binding to the cannabinoid receptors: what is known and what remains unknown. Current Medicinal Chemistry, 17(14), 1468–1486. - Ross, S. A., & ElSohly, M. A. (1999). CBN and Δ9-THC concentration ratio as an indicator of the age of stored marijuana samples. Journal of Forensic Sciences, 44(4), 731–734. - Russo, E. B. (2007). History of cannabis and its preparations in saga, science, and sobriquet. Chemistry & Biodiversity, 4(8), 1614–1648. - Russo, E. B. (2011). Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. British Journal of Pharmacology, 163(7), 1344–1364. - Sim-Selley, L. J. (2003). Regulation of cannabinoid CB1 receptors in the central nervous system. Progress in Neurobiology, 70(4), 303–329. - Turu, G., & Hunyady, L. (2010). Signal transduction of the CB1 cannabinoid receptor. Journal of Molecular Endocrinology, 44(2), 75–85. - Volkow, N. D., Baler, R. D., Compton, W. M., & Weiss, S. R. B. (2014). Adverse health effects of marijuana use. New England Journal of Medicine, 370(23), 2219–2227. - Watanabe, K., Yamaori, S., Funahashi, T., et al. (2007). Cytochrome P450 enzymes involved in the metabolism of tetrahydrocannabinols. Life Sciences, 80(15), 1415–1419. - Zou, S., & Kumar, U. (2018). Cannabinoid receptors and the endocannabinoid system: signaling and function in the central nervous system. International Journal of Molecular Sciences, 19(3), 833.