Introducción
La monoacilglicerol lipasa (MAGL) es una enzima central del sistema endocannabinoide encargada de la degradación del endocannabinoide 2-araquidonoilglicerol (2-AG), un lípido señalizador que actúa como agonista completo de los receptores cannabinoides CB1 y CB2. A través de su actividad hidrolítica, la MAGL convierte el 2-AG en ácido araquidónico y glicerol, regulando de forma directa la duración, intensidad y localización espacial de la señal endocannabinoide en el organismo (Dinh et al., 2002; Blankman et al., 2007).
A nivel funcional, el 2-AG es el endocannabinoide predominante en el sistema nervioso central, con concentraciones significativamente superiores a las de anandamida. Esta abundancia convierte a la MAGL en el principal mecanismo de terminación de la señalización cannabinoide mediada por 2-AG, siendo responsable de aproximadamente el 80–85% de su degradación en el cerebro, mientras que otras enzimas como ABHD6 y ABHD12 desempeñan funciones complementarias en compartimentos celulares específicos (Sugiura et al., 2002; Blankman et al., 2007).
Más allá de su papel en la señalización cannabinoide, la actividad de la MAGL conecta directamente con el metabolismo lipídico y las rutas inflamatorias. El ácido araquidónico liberado tras la hidrólisis del 2-AG actúa como precursor de eicosanoides, incluyendo prostaglandinas y leucotrienos, lo que sitúa a la MAGL en un punto de convergencia entre el sistema endocannabinoide y los sistemas clásicos de señalización inflamatoria (Nomura et al., 2011).
En conjunto, la MAGL no solo regula la señalización endocannabinoide retrógrada, especialmente en el contexto sináptico, sino que también modula procesos fisiológicos amplios como la neurotransmisión, la respuesta inmune y el equilibrio lipídico, consolidándose como una de las enzimas más relevantes en la arquitectura funcional del sistema endocannabinoide.
Historia y descubrimiento
El estudio de la hidrólisis de monoacilglicéridos se remonta a investigaciones clásicas sobre metabolismo lipídico en la segunda mitad del siglo XX, donde ya se describía la existencia de actividades enzimáticas capaces de degradar lípidos simples derivados de glicerol. Sin embargo, durante décadas estas observaciones permanecieron desvinculadas de cualquier sistema de señalización específico, ya que el sistema endocannabinoide aún no había sido descrito (Karlsson et al., 1997).
El punto de inflexión llegó tras la identificación del 2-araquidonoilglicerol (2-AG) a finales de los años 90 como un endocannabinoide funcional. Este descubrimiento generó la necesidad de identificar las enzimas responsables de su síntesis y degradación. En este contexto, a principios de los años 2000, se logró aislar y caracterizar la monoacilglicerol lipasa (MAGL) como la principal enzima responsable de la hidrólisis del 2-AG, estableciendo su papel dentro del sistema endocannabinoide (Dinh et al., 2002).
El desarrollo de herramientas de proteómica basada en actividad (activity-based protein profiling, ABPP) permitió avanzar significativamente en la caracterización funcional de la MAGL. En particular, el trabajo de Blankman et al. (2007) fue clave para cuantificar su contribución, demostrando que la MAGL es responsable de aproximadamente el 85% de la degradación de 2-AG en el cerebro, mientras que enzimas como ABHD6 y ABHD12 participan en menor medida y en compartimentos celulares más específicos.
A partir de estos hallazgos, la investigación comenzó a explorar implicaciones más amplias de la MAGL más allá de la señalización cannabinoide. Estudios posteriores revelaron que su actividad influye directamente en los niveles de ácido araquidónico, integrando la señalización endocannabinoide con la biosíntesis de eicosanoides y, por tanto, con procesos inflamatorios y metabólicos complejos (Nomura et al., 2011).
En conjunto, la identificación de la MAGL no solo completó el esquema básico del metabolismo del 2-AG dentro del sistema endocannabinoide, sino que también abrió nuevas líneas de investigación centradas en su papel como nodo regulador entre señalización lipídica, inflamación y función neuronal.
Estructura y características bioquímicas
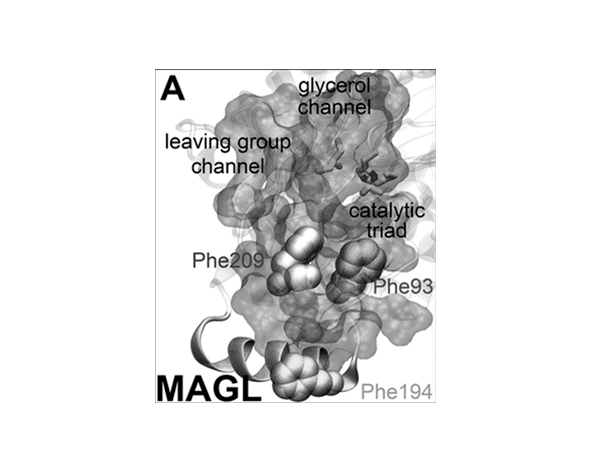
La monoacilglicerol lipasa (MAGL) es una enzima citosólica asociada a membranas que pertenece a la superfamilia de las α/β-hidrolasas, un grupo ampliamente distribuido de enzimas caracterizadas por un plegamiento estructural conservado y un mecanismo catalítico basado en una tríada catalítica clásica formada por serina, histidina y ácido aspártico. Este tipo de arquitectura es típico de enzimas lipolíticas implicadas en la hidrólisis de enlaces éster en lípidos bioactivos (Karlsson et al., 1997; Labar et al., 2010).
Desde el punto de vista estructural, la MAGL presenta un núcleo α/β plegado que alberga el sitio activo en una cavidad hidrofóbica adaptada para reconocer sustratos lipídicos como el 2-AG. La serina nucleofílica del sitio activo actúa como residuo catalítico central, iniciando el ataque sobre el enlace éster del monoacilglicérido, mientras que la histidina y el ácido aspártico estabilizan los estados de transición y facilitan la transferencia de protones durante la reacción (Labar et al., 2010).
Una característica clave de la MAGL es su afinidad por sustratos lipofílicos de cadena larga, especialmente aquellos derivados del ácido araquidónico. Esta especificidad explica su papel predominante en la degradación del 2-AG frente a otros monoacilglicéridos, aunque también puede actuar sobre diferentes sustratos en contextos metabólicos más amplios (Dinh et al., 2002).
A nivel subcelular, la MAGL se localiza principalmente en el citosol y en la cara citosólica de membranas intracelulares, lo que le permite acceder a sustratos generados “on demand” a partir de fosfolípidos de membrana. Esta localización es coherente con la naturaleza del sistema endocannabinoide, donde los ligandos no se almacenan en vesículas, sino que se sintetizan y degradan de forma rápida en respuesta a estímulos celulares (Blankman et al., 2007).
Además, la actividad de la MAGL está finamente regulada tanto por la disponibilidad de sustrato como por mecanismos farmacológicos. Diversos inhibidores selectivos han permitido estudiar su función con gran precisión, revelando que su bloqueo produce un aumento significativo de los niveles de 2-AG y una disminución concomitante del ácido araquidónico libre, lo que refuerza su papel como punto de control entre señalización endocannabinoide y metabolismo lipídico (Nomura et al., 2011).
En conjunto, la estructura de la MAGL no solo define su capacidad catalítica, sino que también determina su posición estratégica dentro del sistema endocannabinoide, actuando como una enzima clave en la regulación dinámica de lípidos bioactivos en múltiples contextos fisiológicos.
Mecanismo de acción
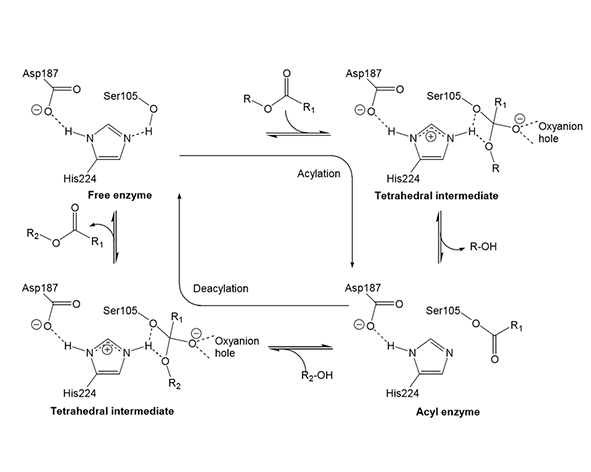
La monoacilglicerol lipasa (MAGL) cataliza la hidrólisis del 2-araquidonoilglicerol (2-AG) mediante un mecanismo clásico de serina hidrolasa, en el que se rompe el enlace éster del sustrato para generar ácido araquidónico y glicerol. Este proceso constituye el principal mecanismo de terminación de la señalización endocannabinoide mediada por 2-AG (Dinh et al., 2002; Labar et al., 2010).
El mecanismo catalítico comienza con la entrada del 2-AG en el sitio activo de la enzima, una cavidad hidrofóbica que orienta el sustrato de manera precisa. La serina nucleofílica de la tríada catalítica ataca el carbono carbonílico del enlace éster del 2-AG, formando un intermediario tetraédrico inestable. Este estado de transición es estabilizado por la estructura del sitio activo, permitiendo la progresión de la reacción (Labar et al., 2010).
Tras esta primera etapa, se libera la fracción de glicerol, mientras que el grupo acilo (derivado del ácido araquidónico) queda temporalmente unido a la enzima formando un intermediario acil-enzima. Este paso es característico de las hidrolasas de serina y representa un punto clave en la catálisis (Karlsson et al., 1997).
En una segunda fase, una molécula de agua activada por la histidina del sitio activo ataca el intermediario acil-enzima, provocando la liberación del ácido araquidónico y regenerando la enzima en su estado basal. Este ciclo catalítico permite a la MAGL procesar múltiples moléculas de sustrato de forma eficiente (Labar et al., 2010).
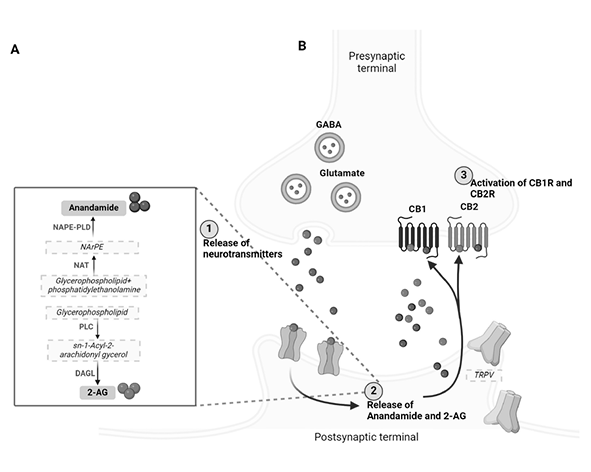
Desde un punto de vista funcional, este mecanismo tiene implicaciones directas en la señalización neuronal. El 2-AG se produce “on demand” en la neurona postsináptica y actúa de forma retrógrada sobre receptores CB1 presinápticos. La acción de la MAGL, localizada en gran medida en terminales presinápticas, limita la duración de esta señal, modulando la liberación de neurotransmisores y manteniendo el equilibrio sináptico (Stella et al., 1997; Blankman et al., 2007).
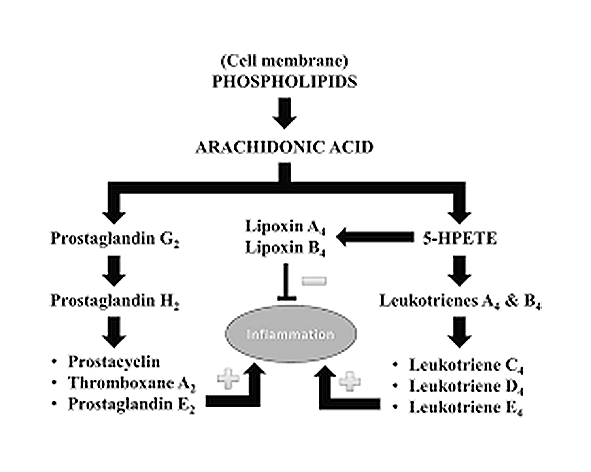
Además, la hidrólisis del 2-AG no solo termina la señal endocannabinoide, sino que también alimenta rutas metabólicas paralelas. El ácido araquidónico liberado puede ser convertido en eicosanoides bioactivos, lo que sitúa a la MAGL como un punto de conexión entre la señalización cannabinoide y los sistemas inflamatorios clásicos (Nomura et al., 2011).
En conjunto, el mecanismo de acción de la MAGL no es simplemente degradativo, sino que constituye un proceso dinámico que integra señalización lipídica, neurotransmisión y metabolismo inflamatorio en un mismo eje funcional.
Distribución y localización
La monoacilglicerol lipasa (MAGL) presenta una distribución amplia en el organismo, aunque su expresión y función adquieren especial relevancia en el sistema nervioso central, donde desempeña un papel clave en la regulación de la señalización endocannabinoide mediada por 2-AG. En el cerebro, la MAGL se localiza predominantemente en terminales presinápticas, lo que la posiciona estratégicamente para modular la señalización retrógrada inducida por endocannabinoides (Blankman et al., 2007; Stella et al., 1997).
A nivel neuronal, el 2-AG se sintetiza principalmente en la neurona postsináptica y difunde hacia la terminal presináptica, donde activa receptores CB1. La presencia de MAGL en este compartimento permite una terminación rápida y localizada de la señal, limitando la activación prolongada de estos receptores y regulando la liberación de neurotransmisores como glutamato y GABA. Esta organización espacial es fundamental para el control fino de la plasticidad sináptica y el equilibrio excitatorio-inhibitorio (Kano et al., 2009).
Además del sistema nervioso central, la MAGL también se expresa en diversos tejidos periféricos, incluyendo hígado, tejido adiposo, músculo esquelético y células del sistema inmunitario. En estos contextos, su función no se limita a la señalización endocannabinoide, sino que se integra en el metabolismo general de lípidos, contribuyendo a la regulación de monoacilglicéridos y a la disponibilidad de ácido araquidónico (Nomura et al., 2011).
A nivel subcelular, la MAGL se encuentra asociada principalmente al citosol y a la cara citosólica de membranas intracelulares, lo que le permite acceder de forma eficiente a sustratos generados a partir de fosfolípidos de membrana. Esta localización es coherente con la naturaleza “on demand” de los endocannabinoides, que no se almacenan en vesículas, sino que se sintetizan y degradan localmente en respuesta a señales fisiológicas (Dinh et al., 2002).
Cabe destacar que otras enzimas como ABHD6 y ABHD12 también participan en la degradación del 2-AG, pero presentan distribuciones diferentes. ABHD6 se localiza principalmente en compartimentos postsinápticos, mientras que ABHD12 tiene una distribución más amplia, incluyendo células microgliales. Esta compartimentalización sugiere que la degradación del 2-AG está finamente regulada en distintos microentornos celulares, siendo la MAGL el componente dominante en términos cuantitativos (Blankman et al., 2007).
En conjunto, la distribución de la MAGL refleja su papel como regulador central de la señalización endocannabinoide y del metabolismo lipídico, actuando en múltiples niveles —sináptico, celular y sistémico— para mantener el equilibrio funcional del organismo.
Relación con el sistema endocannabinoide
La monoacilglicerol lipasa (MAGL) ocupa una posición central dentro del sistema endocannabinoide al actuar como el principal mecanismo de terminación de la señalización mediada por 2-araquidonoilglicerol (2-AG), uno de los dos endocannabinoides más relevantes junto con la anandamida. Mientras que la síntesis de 2-AG ocurre de forma localizada y “on demand” en respuesta a estímulos celulares, su degradación por parte de la MAGL determina la duración y el alcance de su acción sobre los receptores cannabinoides (Sugiura et al., 2002; Blankman et al., 2007).
El 2-AG actúa como un agonista completo de los receptores CB1 y CB2, con una especial relevancia en el sistema nervioso central, donde modula la liberación de neurotransmisores a través de mecanismos de señalización retrógrada. En este contexto, la MAGL regula directamente la intensidad de esta señal al hidrolizar el 2-AG en terminales presinápticas, limitando la activación de los receptores CB1 y evitando una estimulación prolongada (Kano et al., 2009).
Esta función convierte a la MAGL en un regulador negativo clave del tono endocannabinoide, entendido como el nivel basal de activación del sistema. Cuando la actividad de la MAGL aumenta, los niveles de 2-AG disminuyen, reduciendo la señalización cannabinoide. Por el contrario, la inhibición de la MAGL provoca una acumulación de 2-AG y un incremento de la activación de CB1 y CB2, lo que ha sido ampliamente utilizado en investigación para estudiar las funciones del sistema endocannabinoide (Nomura et al., 2011).
A diferencia de la anandamida —cuya degradación está mediada principalmente por la FAAH—, el 2-AG representa la mayor fracción del pool endocannabinoide, lo que implica que la MAGL ejerce un control dominante sobre la señalización global del sistema. Esta diferencia funcional establece una dualidad en la regulación enzimática del sistema endocannabinoide, donde MAGL y FAAH actúan sobre ligandos distintos pero complementarios (Di Marzo et al., 1998).
Además, la acción de la MAGL tiene implicaciones que trascienden la señalización cannabinoide. El ácido araquidónico liberado tras la hidrólisis del 2-AG alimenta la síntesis de eicosanoides, integrando el sistema endocannabinoide con rutas inflamatorias clásicas. De este modo, la MAGL actúa como un nodo de conexión entre señalización lipídica y procesos inflamatorios, ampliando su relevancia más allá del sistema cannabinoide en sentido estricto (Nomura et al., 2011).
En conjunto, la MAGL no solo regula la terminación de la señal endocannabinoide, sino que modula el equilibrio dinámico del sistema en su totalidad, influyendo en procesos como la neurotransmisión, la respuesta inmune y la homeostasis lipídica.
Importancia en investigación
La monoacilglicerol lipasa (MAGL) se ha consolidado como una de las principales dianas en la investigación del sistema endocannabinoide debido a su papel dominante en la regulación de los niveles de 2-araquidonoilglicerol (2-AG). El desarrollo de inhibidores selectivos de MAGL ha permitido estudiar de forma precisa cómo la modulación de este endocannabinoide influye en distintos procesos fisiológicos, especialmente en el sistema nervioso central (Blankman et al., 2007).
Uno de los hallazgos más relevantes en este campo es que la inhibición de la MAGL produce un aumento significativo de los niveles de 2-AG, lo que conlleva una mayor activación de los receptores CB1 y CB2. Este enfoque ha sido ampliamente utilizado en modelos experimentales para analizar el papel del sistema endocannabinoide en la modulación de la neurotransmisión, la plasticidad sináptica y la respuesta al estrés (Nomura et al., 2011).
A diferencia de otros enfoques que actúan directamente sobre los receptores cannabinoides, la modulación de MAGL permite aumentar el tono endocannabinoide de forma indirecta, respetando en mayor medida los mecanismos fisiológicos de señalización “on demand”. Este aspecto ha generado interés en el estudio de estrategias que actúan sobre enzimas del sistema en lugar de sobre los receptores, aunque estas aproximaciones se mantienen dentro del ámbito experimental (Labar et al., 2010).
Además, la MAGL ha sido objeto de investigación por su papel en la regulación del ácido araquidónico y, por extensión, en la síntesis de eicosanoides. La inhibición de la MAGL no solo eleva los niveles de 2-AG, sino que también reduce la disponibilidad de ácido araquidónico libre, lo que puede alterar la producción de mediadores lipídicos implicados en procesos inflamatorios. Esta doble acción ha reforzado la idea de que la MAGL actúa como un punto de intersección entre señalización endocannabinoide y metabolismo lipídico (Nomura et al., 2011).
Por otro lado, estudios en modelos animales han explorado las consecuencias de la inhibición prolongada de la MAGL, observando fenómenos de adaptación del sistema endocannabinoide, como la desensibilización de receptores CB1 tras exposiciones sostenidas a niveles elevados de 2-AG. Estos resultados han puesto de manifiesto la importancia de la regulación temporal en la modulación de este sistema (Schlosburg et al., 2010).
En conjunto, la investigación sobre la MAGL ha permitido comprender mejor cómo el equilibrio entre síntesis y degradación de endocannabinoides influye en la fisiología del organismo. Aunque muchas de estas aproximaciones se encuentran en fases preclínicas, el estudio de esta enzima sigue siendo clave para desentrañar los mecanismos fundamentales del sistema endocannabinoide y su interacción con otros sistemas de señalización lipídica.
Referencias
- Blankman, J. L., Simon, G. M., & Cravatt, B. F. (2007). A comprehensive profile of brain enzymes that hydrolyze the endocannabinoid 2-arachidonoylglycerol. Chemistry & Biology, 14(12), 1347–1356. - Dinh, T. P., Carpenter, D., Leslie, F. M., Freund, T. F., Katona, I., Sensi, S. L., Kathuria, S., & Piomelli, D. (2002). Brain monoglyceride lipase participating in endocannabinoid inactivation. Proceedings of the National Academy of Sciences, 99(16), 10819–10824. - Di Marzo, V., Melck, D., Bisogno, T., & De Petrocellis, L. (1998). Endocannabinoids: endogenous cannabinoid receptor ligands with neuromodulatory action. Trends in Neurosciences, 21(12), 521–528. - Kano, M., Ohno-Shosaku, T., Hashimotodani, Y., Uchigashima, M., & Watanabe, M. (2009). Endocannabinoid-mediated control of synaptic transmission. Physiological Reviews, 89(1), 309–380. - Karlsson, M., Contreras, J. A., Hellman, U., Tornqvist, H., & Holm, C. (1997). cDNA cloning, tissue distribution, and identification of the catalytic triad of monoglyceride lipase. Journal of Biological Chemistry, 272(43), 27218–27223. - Labar, G., Bauvois, C., Borel, F., Ferrer, J. L., Wouters, J., & Lambert, D. M. (2010). Crystal structure of the human monoacylglycerol lipase, a key actor in endocannabinoid signaling. ChemBioChem, 11(15), 218–227. - Nomura, D. K., Morrison, B. E., Blankman, J. L., Long, J. Z., Kinsey, S. G., Marcondes, M. C. G., Ward, A. M., Hahn, Y. K., Lichtman, A. H., Conti, B., & Cravatt, B. F. (2011). Endocannabinoid hydrolysis generates brain prostaglandins that promote neuroinflammation. Science, 334(6057), 809–813. - Schlosburg, J. E., Blankman, J. L., Long, J. Z., Nomura, D. K., Pan, B., Kinsey, S. G., Nguyen, P. T., Ramesh, D., Booker, L., Burston, J. J., Thomas, E. A., Selley, D. E., Sim-Selley, L. J., Liu, Q. S., Lichtman, A. H., & Cravatt, B. F. (2010). Chronic monoacylglycerol lipase blockade causes functional antagonism of the endocannabinoid system. Nature Neuroscience, 13(9), 1113–1119. - Stella, N., Schweitzer, P., & Piomelli, D. (1997). A second endogenous cannabinoid that modulates long-term potentiation. Nature, 388(6644), 773–778. - Sugiura, T., Kondo, S., Sukagawa, A., Nakane, S., Shinoda, A., Itoh, K., Yamashita, A., & Waku, K. (2002). 2-Arachidonoylglycerol: a possible endogenous cannabinoid receptor ligand in brain. Biochemical and Biophysical Research Communications, 215(1), 89–97.