Introducción
La anandamida, conocida científicamente como N-araquidonoiletanolamida (AEA), es uno de los principales endocannabinoides del sistema endocannabinoide. Se trata de un mediador lipídico derivado del ácido araquidónico que actúa como ligando endógeno de los receptores cannabinoides, particularmente del receptor CB1 y, en menor medida, del receptor CB2. Desde su descubrimiento en 1992, la anandamida ha sido reconocida como un componente central en la señalización endocannabinoide, participando en la regulación de procesos fisiológicos relacionados con la homeostasis neuronal, inmunológica y metabólica (Devane et al., 1992; Di Marzo et al., 1998).
El término anandamida deriva del sánscrito ananda, que significa “felicidad” o “bienaventuranza”, en referencia a los efectos moduladores que este compuesto puede ejercer sobre estados emocionales y funciones neurológicas. A diferencia de neurotransmisores clásicos almacenados en vesículas sinápticas, la anandamida se sintetiza de novo en las membranas celulares a partir de fosfolípidos de membrana, lo que refleja su naturaleza como mediador lipídico de señalización rápida (Piomelli, 2003; Di Marzo & De Petrocellis, 2012).
La señalización mediada por anandamida forma parte de un sistema regulador distribuido ampliamente en el organismo, que incluye receptores cannabinoides, enzimas biosintéticas y enzimas degradativas. Este sistema actúa como un mecanismo de retroalimentación que modula la liberación de neurotransmisores y otros mediadores celulares, contribuyendo al mantenimiento del equilibrio fisiológico frente a cambios ambientales o fisiológicos (Lu & Mackie, 2016).
Historia del descubrimiento
La anandamida fue identificada por primera vez en 1992 por William Devane, Lumír Hanuš y Raphael Mechoulam, quienes aislaron este compuesto a partir de tejido cerebral de cerdo mientras investigaban ligandos endógenos capaces de activar los receptores cannabinoides recientemente descubiertos. El hallazgo representó un avance fundamental en la comprensión del sistema endocannabinoide, ya que proporcionó la primera evidencia de que el organismo produce moléculas endógenas capaces de interactuar con los mismos receptores activados por los fitocannabinoides de la planta Cannabis sativa (Devane et al., 1992).
El descubrimiento de la anandamida marcó el inicio de una nueva área de investigación en neurobiología y farmacología, centrada en la identificación de endocannabinoides adicionales, las enzimas responsables de su metabolismo y los mecanismos fisiológicos asociados a su señalización. En los años posteriores se identificaron otros ligandos endógenos, entre ellos el 2-araquidonoilglicerol (2-AG), que junto con la anandamida constituye uno de los principales mediadores del sistema endocannabinoide (Mechoulam & Parker, 2013).
La identificación de la anandamida también permitió comprender que el sistema cannabinoide no es un mecanismo exclusivo de interacción con compuestos exógenos, sino un sistema de señalización fisiológica intrínseco al organismo. Este hallazgo cambió profundamente la percepción científica del cannabis y de los cannabinoides, orientando la investigación hacia la fisiología de los lípidos señalizadores derivados de ácidos grasos poliinsaturados (Pertwee, 2008).
Estructura química y características moleculares
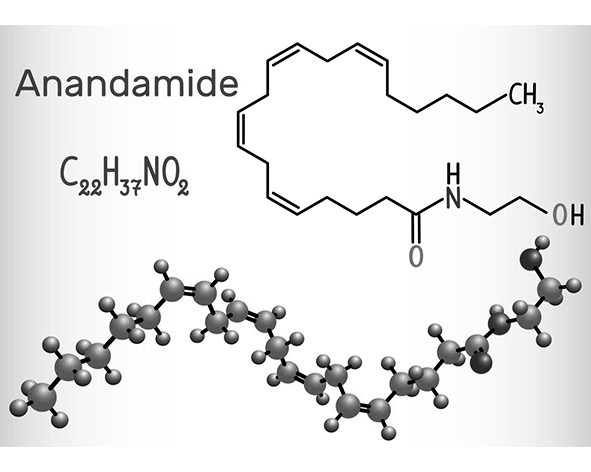
La anandamida pertenece a la familia de las N-aciletanolaminas (NAE), un grupo de lípidos bioactivos derivados de ácidos grasos de cadena larga unidos a etanolamina. En el caso específico de la anandamida, el ácido graso implicado es el ácido araquidónico, un ácido graso poliinsaturado de 20 carbonos que forma parte de los fosfolípidos de las membranas celulares (Di Marzo et al., 1998).
Desde el punto de vista estructural, la anandamida presenta una cadena hidrocarbonada altamente insaturada que le confiere una naturaleza lipofílica y flexible, facilitando su interacción con dominios hidrofóbicos de receptores de membrana como CB1. Esta característica estructural permite que la molécula adopte diferentes conformaciones espaciales al interactuar con su sitio de unión en los receptores cannabinoides (Makriyannis, 2014).
La naturaleza lipídica de la anandamida también condiciona su comportamiento farmacocinético a nivel celular. A diferencia de neurotransmisores hidrosolubles, la anandamida difunde a través de membranas celulares y puede ser rápidamente captada y degradada por enzimas intracelulares, lo que limita su duración de acción y contribuye a la regulación precisa de la señalización endocannabinoide (Piomelli, 2003).
Biosíntesis
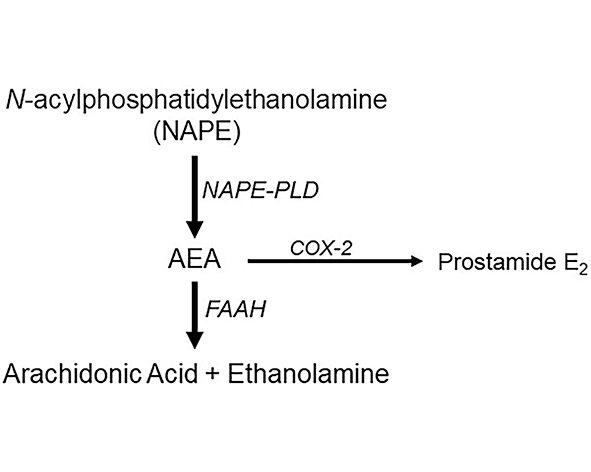
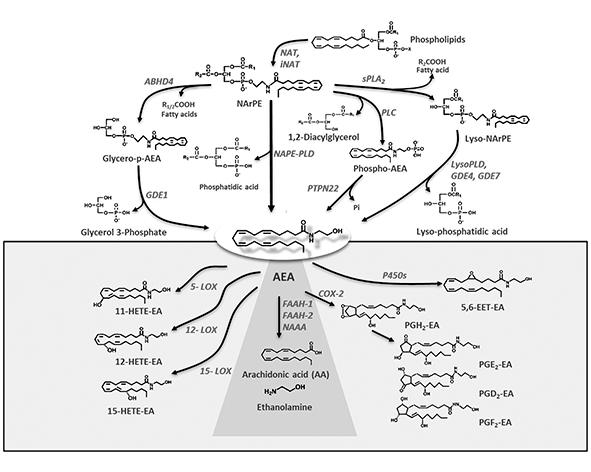
La anandamida se sintetiza a partir de fosfolípidos de membrana que contienen N-araquidonoil fosfatidiletanolamina (NAPE) como precursor inmediato. El proceso biosintético puede ocurrir mediante varias rutas enzimáticas, siendo la más estudiada la mediada por la enzima NAPE-fosfolipasa D (NAPE-PLD), que hidroliza NAPE para generar anandamida y fosfatidato (Okamoto et al., 2004).
Además de esta vía principal, se han descrito rutas alternativas de síntesis que implican enzimas como fosfolipasas C, fosfatasas y otras hidrolasas, lo que sugiere que la producción de anandamida puede adaptarse a diferentes contextos celulares y fisiológicos. Estas rutas alternativas reflejan la complejidad del metabolismo de los endocannabinoides y su integración en redes metabólicas más amplias relacionadas con el metabolismo de lípidos (Di Marzo & De Petrocellis, 2012).
A diferencia de neurotransmisores clásicos que se almacenan en vesículas sinápticas, la anandamida se produce bajo demanda, es decir, en respuesta a estímulos celulares específicos como aumentos en la concentración intracelular de calcio o la activación de ciertos receptores acoplados a proteína G. Este mecanismo permite una regulación dinámica de la señalización endocannabinoide en función de las necesidades fisiológicas del tejido (Lu & Mackie, 2016).
Mecanismos de señalización
La anandamida actúa principalmente como ligando endógeno de los receptores cannabinoides, especialmente del receptor CB1, al que se une con afinidad moderada. Al activarse este receptor, que pertenece a la familia de los receptores acoplados a proteína G (GPCR), se desencadena una cascada de señalización intracelular que conduce a la inhibición de la adenilato ciclasa, la disminución de los niveles intracelulares de AMPc y la modulación de múltiples rutas de señalización celular implicadas en la regulación neuronal y metabólica (Howlett et al., 2002; Pertwee, 2008).
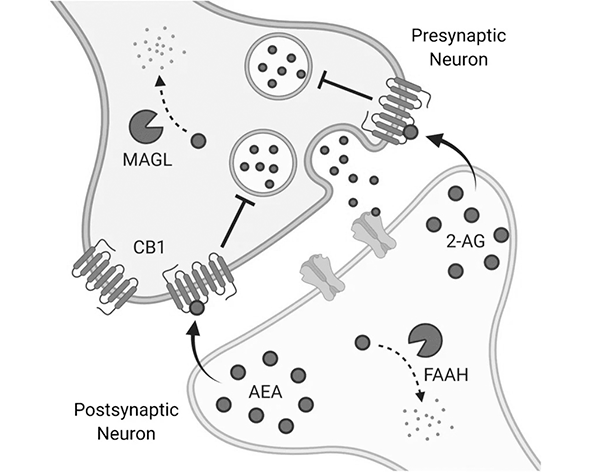
En el sistema nervioso central, la anandamida participa en mecanismos de señalización retrógrada sináptica. En este proceso, la molécula es sintetizada en la neurona postsináptica y difunde hacia la terminal presináptica, donde activa receptores CB1 localizados en la membrana presináptica. Esta activación reduce la liberación de neurotransmisores excitatorios o inhibitorios, contribuyendo a la regulación de la transmisión sináptica y al equilibrio entre señales excitatorias e inhibitorias en circuitos neuronales (Castillo et al., 2012; Lu & Mackie, 2016).
Además de su interacción con los receptores cannabinoides clásicos, la anandamida también puede modular otras dianas moleculares. Entre ellas se encuentra el canal iónico TRPV1 (Transient Receptor Potential Vanilloid 1), implicado en la percepción del dolor y la regulación de procesos inflamatorios. La activación de TRPV1 por anandamida sugiere que los endocannabinoides pueden participar en redes de señalización más amplias que van más allá de los receptores cannabinoides tradicionales (Ross, 2003; Di Marzo & De Petrocellis, 2012).
La señalización mediada por anandamida está estrechamente controlada por mecanismos de síntesis y degradación rápida. Este carácter transitorio permite que los endocannabinoides actúen como moduladores locales de corta duración, ajustando la actividad de circuitos celulares sin producir activaciones prolongadas que podrían alterar el equilibrio fisiológico del sistema (Piomelli, 2003).
Distribución en el organismo
La anandamida se encuentra distribuida en numerosos tejidos del organismo, aunque sus concentraciones varían dependiendo del tipo celular y del estado fisiológico. En el sistema nervioso central, se ha detectado en regiones cerebrales implicadas en la regulación de la memoria, el control motor, la percepción del dolor y la modulación emocional, incluyendo el hipocampo, la corteza cerebral, el cerebelo y los ganglios basales (Herkenham et al., 1991; Pertwee, 2008).
Fuera del sistema nervioso central, la anandamida también se encuentra en tejidos periféricos como el sistema inmunitario, el tracto gastrointestinal, el tejido adiposo y el sistema cardiovascular. En estos contextos, la señalización endocannabinoide participa en procesos relacionados con la respuesta inmunitaria, el metabolismo energético y la regulación de funciones fisiológicas locales (Di Marzo et al., 1998; Lu & Mackie, 2016).
La presencia de anandamida en diferentes sistemas fisiológicos refleja la naturaleza multifuncional del sistema endocannabinoide, que actúa como una red reguladora distribuida en el organismo. Esta distribución amplia permite que los endocannabinoides participen en la modulación de múltiples procesos celulares y fisiológicos, contribuyendo al mantenimiento de la homeostasis biológica (Di Marzo & De Petrocellis, 2012).
Transporte celular de anandamida
Tras su liberación desde la membrana postsináptica, la anandamida puede difundirse a través del espacio extracelular para interactuar con receptores cannabinoides localizados en células vecinas o en terminales presinápticas. Debido a su naturaleza lipofílica, durante muchos años se asumió que su movimiento a través de las membranas celulares ocurría principalmente mediante difusión pasiva a través de la bicapa lipídica (Piomelli, 2003).
Sin embargo, diversos estudios han sugerido la existencia de mecanismos más complejos de captación intracelular que podrían facilitar el transporte de endocannabinoides desde el medio extracelular hacia el interior de la célula. Este proceso ha sido denominado transporte de endocannabinoides o “endocannabinoid membrane transport”, aunque la identidad molecular exacta de un transportador específico sigue siendo objeto de debate en la literatura científica (Fowler, 2013).
Una vez dentro de la célula, la anandamida es rápidamente dirigida hacia compartimentos intracelulares donde puede ser degradada por enzimas como FAAH. Este proceso de captación y degradación contribuye a mantener niveles bajos de anandamida en el espacio extracelular y limita la duración de su señalización. De este modo, la captación celular actúa como un mecanismo funcionalmente equivalente a la recaptación de neurotransmisores, aunque basado en principios bioquímicos distintos (Piomelli, 2003; Fowler, 2013).
La naturaleza exacta de los mecanismos de transporte de endocannabinoides continúa siendo investigada, y se ha propuesto que proteínas de unión intracelulares y transportadores lipídicos podrían desempeñar un papel relevante en la regulación de la disponibilidad de anandamida dentro de las células (Kaczocha et al., 2009).
Interacción con receptores cannabinoides
La anandamida actúa como ligando endógeno parcial de los receptores cannabinoides, mostrando afinidad principalmente por el receptor CB1 y, en menor medida, por el receptor CB2. El receptor CB1 se expresa abundantemente en el sistema nervioso central y es responsable de gran parte de los efectos fisiológicos asociados a la señalización endocannabinoide mediada por anandamida (Pertwee, 2008).
La activación de CB1 por anandamida desencadena una señalización intracelular mediada por proteínas G del tipo Gi/o, lo que conduce a la inhibición de la adenilato ciclasa, la reducción de los niveles de AMPc y la modulación de múltiples rutas de señalización intracelular. Entre los efectos celulares asociados se incluyen la regulación de canales de calcio dependientes de voltaje, la activación de canales de potasio y la modulación de cascadas de señalización como MAPK (Howlett et al., 2002).
En el contexto neuronal, la activación de CB1 por anandamida contribuye a la regulación de la liberación de neurotransmisores en las terminales presinápticas. Este mecanismo se basa en la señalización retrógrada característica del sistema endocannabinoide, mediante la cual los endocannabinoides producidos en la neurona postsináptica modulan la actividad de la neurona presináptica, ajustando la intensidad de la transmisión sináptica (Castillo et al., 2012).
Aunque la anandamida puede interactuar con el receptor CB2, su afinidad por este receptor es menor en comparación con CB1. CB2 se expresa predominantemente en células del sistema inmunitario y en tejidos periféricos, lo que sugiere que la señalización mediada por anandamida puede extenderse también a contextos fisiológicos relacionados con la regulación inmunitaria y la respuesta inflamatoria (Pertwee, 2008).
Anandamida y otros endocannabinoides
Aunque la anandamida fue el primer endocannabinoide identificado, no es el único mediador lipídico que participa en la señalización del sistema endocannabinoide. Otro endocannabinoide fundamental es el 2-araquidonoilglicerol (2-AG), descubierto pocos años después y que comparte con la anandamida la capacidad de activar los receptores cannabinoides. Ambos compuestos constituyen los principales ligandos endógenos del sistema endocannabinoide, aunque presentan diferencias importantes en su abundancia, metabolismo y funciones fisiológicas (Mechoulam & Parker, 2013).
Una de las diferencias más destacadas entre anandamida y 2-AG es su concentración relativa en los tejidos. En el sistema nervioso central, el 2-AG suele encontrarse en concentraciones significativamente más altas que la anandamida, lo que sugiere que ambos endocannabinoides pueden desempeñar roles complementarios en la regulación de la señalización sináptica. Mientras que el 2-AG parece actuar como un mediador predominante en ciertos procesos de señalización neuronal, la anandamida podría participar en funciones moduladoras más específicas dentro del sistema endocannabinoide (Sugiura et al., 2002; Di Marzo & De Petrocellis, 2012).
Otra diferencia importante radica en los mecanismos de degradación enzimática. La anandamida es degradada principalmente por la enzima FAAH (Fatty Acid Amide Hydrolase), mientras que el 2-AG es metabolizado principalmente por monoacilglicerol lipasa (MAGL). Estas diferencias en las rutas metabólicas permiten que ambos endocannabinoides se regulen de manera independiente, lo que añade un nivel adicional de complejidad a la regulación del sistema endocannabinoide (Blankman et al., 2007).
Desde el punto de vista funcional, la coexistencia de múltiples endocannabinoides permite que el sistema endocannabinoide actúe como una red de señalización lipídica dinámica, capaz de responder a distintos estímulos fisiológicos mediante la producción diferencial de mediadores bioactivos. Esta diversidad molecular contribuye a la flexibilidad del sistema en la regulación de procesos fisiológicos complejos (Lu & Mackie, 2016).
Regulación fisiológica de los niveles de anandamida
Las concentraciones de anandamida en los tejidos no son estáticas, sino que pueden variar en respuesta a múltiples factores fisiológicos. Diversos estudios han demostrado que la producción y liberación de anandamida puede aumentar en determinadas condiciones celulares, como cambios en la actividad neuronal, variaciones en la concentración intracelular de calcio o activación de determinados receptores acoplados a proteína G (Piomelli, 2003).
En el sistema nervioso, la síntesis de anandamida puede activarse en respuesta a la actividad sináptica, actuando como un modulador de la transmisión neuronal. Este mecanismo permite que los endocannabinoides participen en procesos de plasticidad sináptica, ajustando dinámicamente la intensidad de la señalización neuronal en función de las necesidades fisiológicas del circuito neuronal (Castillo et al., 2012).
Factores sistémicos como el estrés fisiológico, la actividad física o cambios metabólicos también pueden influir en los niveles de anandamida. Se ha observado que determinadas condiciones fisiológicas pueden alterar la producción o degradación de endocannabinoides, lo que sugiere que el sistema endocannabinoide actúa como un mecanismo de regulación adaptativa frente a cambios en el entorno interno o externo del organismo (Di Marzo & De Petrocellis, 2012).
La regulación de los niveles de anandamida depende de un equilibrio entre su síntesis, transporte y degradación enzimática. Este control dinámico permite que la señalización endocannabinoide sea rápida, localizada y transitoria, características esenciales para su función como sistema modulador de múltiples procesos fisiológicos (Lu & Mackie, 2016).
Interacción con otras dianas moleculares
Además de los receptores cannabinoides clásicos, la anandamida puede interactuar con varias dianas moleculares no cannabinoides, lo que amplía el espectro funcional del sistema endocannabinoide. Una de las interacciones más estudiadas es la activación del canal iónico TRPV1 (Transient Receptor Potential Vanilloid 1), conocido por su papel en la detección de estímulos térmicos y en la percepción del dolor (Ross, 2003).
La activación de TRPV1 por anandamida sugiere que los endocannabinoides pueden participar en redes de señalización que integran múltiples sistemas fisiológicos. Este tipo de interacción representa un ejemplo de señalización lipídica convergente, en la que una misma molécula puede modular diferentes receptores y canales iónicos dependiendo del contexto celular (Di Marzo & De Petrocellis, 2012).
Además de TRPV1, se ha observado que la anandamida puede interactuar con receptores nucleares como PPAR-α (Peroxisome Proliferator-Activated Receptor alpha), implicados en la regulación del metabolismo lipídico y en la modulación de respuestas celulares relacionadas con el metabolismo energético. Estas interacciones reflejan la complejidad de las redes de señalización en las que participan los endocannabinoides (O’Sullivan, 2007).
También se han descrito posibles interacciones con otros receptores acoplados a proteína G considerados receptores cannabinoides no clásicos, como GPR55, aunque la naturaleza exacta de estas interacciones y su relevancia fisiológica continúan siendo objeto de investigación (Pertwee et al., 2010).
Degradación y metabolismo
La actividad de la anandamida está regulada principalmente por su rápida degradación enzimática. La enzima más importante en este proceso es la hidrolasa de amidas de ácidos grasos (FAAH, Fatty Acid Amide Hydrolase), localizada en el interior de las células. Esta enzima hidroliza la anandamida en ácido araquidónico y etanolamina, terminando así su acción señalizadora (Cravatt et al., 1996).
La degradación mediada por FAAH constituye uno de los mecanismos clave que controlan la duración de la señalización endocannabinoide. Dado que la anandamida no se almacena en vesículas y se produce bajo demanda, su eliminación rápida tras ejercer su función es esencial para evitar una activación prolongada de los receptores cannabinoides (Piomelli, 2003).
Además de la hidrólisis mediada por FAAH, se han descrito rutas metabólicas adicionales en las que la anandamida puede ser oxidada por enzimas como ciclooxigenasas, lipoxigenasas y citocromos P450, generando metabolitos bioactivos que pueden participar en otras vías de señalización celular relacionadas con el metabolismo de eicosanoides (Di Marzo & De Petrocellis, 2012).
Importancia en la investigación científica
La anandamida ha sido objeto de un intenso interés científico desde su descubrimiento, debido a su papel central en la señalización del sistema endocannabinoide. La investigación en este campo ha contribuido a ampliar la comprensión de los mecanismos de regulación fisiológica mediados por lípidos señalizadores y ha revelado nuevas interacciones entre el sistema endocannabinoide y otras redes de señalización celular (Mechoulam & Parker, 2013).
Los estudios sobre anandamida también han permitido explorar la relevancia del sistema endocannabinoide en múltiples contextos fisiológicos y experimentales, incluyendo la regulación de la transmisión sináptica, la respuesta al estrés, el metabolismo energético y la interacción entre sistemas neurológicos e inmunológicos. Estas investigaciones han situado a los endocannabinoides como un área relevante dentro de la neurobiología y la farmacología contemporánea (Lu & Mackie, 2016).
El análisis de las enzimas responsables de la síntesis y degradación de anandamida, así como de los receptores implicados en su señalización, continúa siendo un campo activo de investigación. Estos estudios contribuyen a mejorar la comprensión del papel del sistema endocannabinoide en la fisiología humana y en los mecanismos moleculares que regulan la homeostasis biológica (Di Marzo & De Petrocellis, 2012).
Referencias
- Devane WA, Hanuš L, Breuer A, et al. (1992). Isolation and structure of a brain constituent that binds to the cannabinoid receptor. Science. 258(5090):1946–1949. - Di Marzo V, Melck D, Bisogno T, De Petrocellis L. (1998). Endocannabinoids: endogenous cannabinoid receptor ligands with neuromodulatory action. Trends in Neurosciences. 21(12):521–528. - Howlett AC, Barth F, Bonner TI, et al. (2002). International Union of Pharmacology. XXVII. Classification of cannabinoid receptors. Pharmacological Reviews. 54(2):161–202. - Cravatt BF, Giang DK, Mayfield SP, et al. (1996). Molecular characterization of an enzyme that degrades neuromodulatory fatty-acid amides. Nature. 384(6604):83–87. - Sugiura T, Kishimoto S, Oka S, Gokoh M. (2002). Biochemistry, pharmacology and physiology of 2-arachidonoylglycerol, an endogenous cannabinoid receptor ligand. Progress in Lipid Research. 41(6):473–505. - Blankman JL, Simon GM, Cravatt BF. (2007). A comprehensive profile of brain enzymes that hydrolyze the endocannabinoid 2-arachidonoylglycerol. Chemistry & Biology. 14(12):1347–1356. - Castillo PE, Younts TJ, Chávez AE, Hashimotodani Y. (2012). Endocannabinoid signaling and synaptic function. Neuron. 76(1):70–81. - Lu HC, Mackie K. (2016). An introduction to the endogenous cannabinoid system. Biological Psychiatry. 79(7):516–525. - Piomelli D. (2003). The molecular logic of endocannabinoid signalling. Nature Reviews Neuroscience. 4(11):873–884. - Di Marzo V, De Petrocellis L. (2012). Why do cannabinoid receptors have more than one endogenous ligand? Philosophical Transactions of the Royal Society B. 367:3216–3228. - Fowler CJ. (2013). Transport of endocannabinoids across the plasma membrane and within the cell. FEBS Journal. 280(9):1895–1904. - Kaczocha M, Glaser ST, Deutsch DG. (2009). Identification of intracellular carriers for the endocannabinoid anandamide. Proceedings of the National Academy of Sciences. 106(15):6375–6380. - Ross RA. (2003). Anandamide and vanilloid TRPV1 receptors. British Journal of Pharmacology. 140(5):790–801. - O’Sullivan SE. (2007). Cannabinoids go nuclear: evidence for activation of peroxisome proliferator-activated receptors. British Journal of Pharmacology. 152(5):576–582. - Pertwee RG. (2008). The diverse CB1 and CB2 receptor pharmacology of cannabinoids. British Journal of Pharmacology. 153(2):199–215. - Mechoulam R, Parker LA. (2013). The endocannabinoid system and the brain. Annual Review of Psychology. 64:21–47.