Introducción
El sistema endocannabinoide (SEC) constituye una red de señalización lipídica ampliamente distribuida en organismos vertebrados que participa en la regulación de múltiples procesos fisiológicos y en el mantenimiento de la homeostasis sistémica. Este sistema está compuesto por receptores cannabinoides acoplados a proteínas G, ligandos endógenos derivados de ácidos grasos poliinsaturados —denominados endocannabinoides— y un conjunto de enzimas responsables de su síntesis y degradación (Di Marzo et al., 1998; Pertwee, 2008).
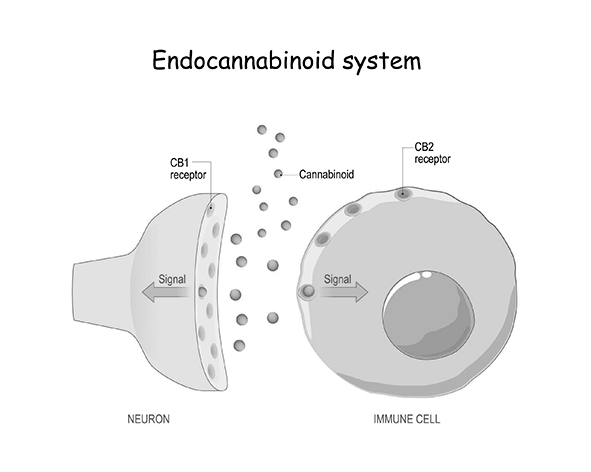
El reconocimiento del sistema endocannabinoide como sistema fisiológico independiente surgió a partir de investigaciones farmacológicas destinadas a comprender los mecanismos de acción del Δ9-tetrahidrocannabinol (THC), el principal cannabinoide psicoactivo presente en Cannabis sativa. Durante la década de 1980 se demostró que los cannabinoides ejercían sus efectos mediante receptores específicos presentes en el sistema nervioso central, lo que condujo a la identificación del receptor cannabinoide tipo 1 (CB1) mediante estudios de unión radioligante en tejido cerebral (Devane et al., 1988).
La posterior identificación de un segundo receptor cannabinoide, CB2, predominantemente expresado en células del sistema inmunitario y tejidos periféricos, amplió la comprensión de la señalización cannabinoide más allá del sistema nervioso central (Munro et al., 1993). Estos descubrimientos condujeron a la hipótesis de que el organismo debía producir ligandos endógenos capaces de activar dichos receptores, lo que culminó con el aislamiento del primer endocannabinoide, N-araquidonoiletanolamina, posteriormente denominado anandamida, a partir de tejido cerebral de mamíferos (Devane et al., 1992).
Pocos años después se identificó un segundo ligando endógeno principal, 2-araquidonoilglicerol (2-AG), presente en concentraciones significativamente superiores a las de anandamida en diversos tejidos del organismo (Mechoulam et al., 1995; Sugiura et al., 1995). El descubrimiento de estos ligandos estableció definitivamente la existencia de un sistema de señalización endógeno basado en lípidos bioactivos, actualmente conocido como sistema endocannabinoide.
A nivel molecular, la señalización endocannabinoide presenta varias características distintivas respecto a otros sistemas de neurotransmisión. A diferencia de muchos neurotransmisores clásicos, los endocannabinoides no se almacenan en vesículas presinápticas, sino que se sintetizan de novo a partir de precursores lipídicos de membrana en respuesta a estímulos celulares específicos (Di Marzo, 2008). Tras su liberación, estos lípidos difunden localmente y actúan principalmente mediante mecanismos de señalización retrógrada, modulando la liberación de neurotransmisores en terminales presinápticas mediante la activación de receptores CB1 (Kano et al., 2009).
Desde su caracterización inicial, el sistema endocannabinoide ha sido identificado como un modulador fisiológico clave implicado en la regulación de procesos tan diversos como la neurotransmisión sináptica, la respuesta inmunitaria, el metabolismo energético, la plasticidad neuronal y la respuesta al estrés (Lu & Mackie, 2016). Debido a esta función integradora, el SEC se considera actualmente un sistema regulador central en el mantenimiento de la estabilidad fisiológica en organismos complejos.
Historia del descubrimiento
El desarrollo del concepto moderno de sistema endocannabinoide fue el resultado de varias décadas de investigación en farmacología, neurobiología y bioquímica de lípidos. La comprensión de este sistema surgió inicialmente a partir de estudios destinados a caracterizar los mecanismos moleculares responsables de los efectos farmacológicos de los cannabinoides derivados de Cannabis sativa.
Identificación de los receptores cannabinoides
Durante gran parte del siglo XX se asumía que los cannabinoides ejercían sus efectos mediante interacciones inespecíficas con las membranas celulares debido a su elevada lipofilia. Sin embargo, esta hipótesis comenzó a cuestionarse cuando diversos estudios farmacológicos demostraron que los efectos del Δ9-tetrahidrocannabinol (THC) presentaban características propias de interacciones receptor-ligando altamente específicas, incluyendo afinidad saturable y estereoselectividad (Howlett et al., 1988).
La evidencia definitiva de la existencia de un receptor específico para cannabinoides se obtuvo mediante experimentos de unión radioligante, en los que se identificó un sitio de unión de alta afinidad en membranas neuronales de cerebro de rata. Este receptor fue posteriormente denominado receptor cannabinoide tipo 1 (CB1) y se caracterizó como un receptor acoplado a proteína G perteneciente a la familia de los receptores acoplados a proteína G de siete dominios transmembrana (GPCR) (Devane et al., 1988; Matsuda et al., 1990).
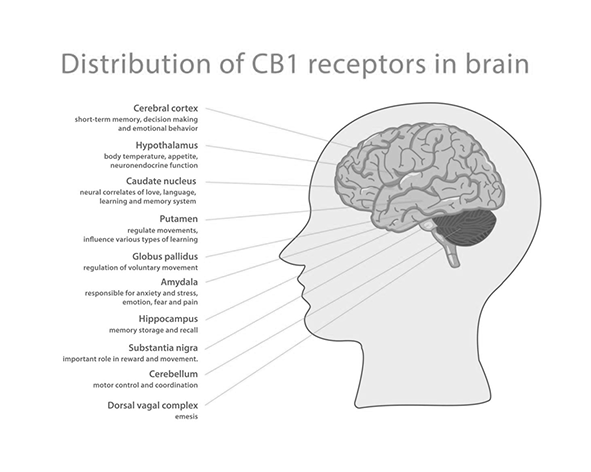
El receptor CB1 se reveló como uno de los GPCR más abundantes del sistema nervioso central, con elevada densidad en regiones cerebrales implicadas en funciones como memoria, control motor, procesamiento emocional y modulación sensorial, incluyendo el hipocampo, ganglios basales, cerebelo y corteza cerebral (Herkenham et al., 1990).
Pocos años después se identificó un segundo receptor cannabinoide, denominado CB2, inicialmente descrito en células del sistema inmunitario y tejidos periféricos (Munro et al., 1993). A diferencia del receptor CB1, cuya expresión se concentra principalmente en el sistema nervioso central, el receptor CB2 se asocia predominantemente con células hematopoyéticas, macrófagos y otras poblaciones celulares implicadas en procesos inmunológicos.
La identificación de estos dos receptores estableció las bases moleculares para comprender la señalización cannabinoide y planteó una cuestión fundamental: si existían receptores específicos para cannabinoides en el organismo, era probable que existieran ligandos endógenos capaces de activarlos.
Descubrimiento de los endocannabinoides
La búsqueda de ligandos endógenos para los receptores cannabinoides condujo al descubrimiento de los endocannabinoides, un grupo de lípidos bioactivos derivados de ácidos grasos poliinsaturados capaces de activar los receptores CB1 y CB2.
En 1992, Devane y colaboradores aislaron el primer ligando endógeno para el receptor CB1 a partir de extractos de cerebro de cerdo. Este compuesto fue identificado como N-araquidonoiletanolamina, posteriormente denominado anandamida (AEA), un término derivado de la palabra sánscrita ānanda, que significa “felicidad” o “bienestar” (Devane et al., 1992).
La anandamida mostró afinidad moderada por el receptor CB1 y fue capaz de reproducir varios de los efectos farmacológicos observados con cannabinoides derivados del cannabis, lo que confirmó la existencia de un sistema de señalización endógeno funcional.
Posteriormente, en 1995, se identificó un segundo ligando endógeno de gran relevancia fisiológica: 2-araquidonoilglicerol (2-AG). Este compuesto fue descubierto de forma independiente por dos grupos de investigación y se encontró presente en concentraciones significativamente mayores que la anandamida en diversos tejidos del organismo (Mechoulam et al., 1995; Sugiura et al., 1995).
A diferencia de la anandamida, el 2-AG actúa como agonista completo tanto de CB1 como de CB2, y se considera actualmente uno de los principales mediadores de la señalización endocannabinoide en el sistema nervioso central.
Consolidación del concepto de sistema endocannabinoide
El descubrimiento de los receptores cannabinoides y de sus ligandos endógenos llevó a la formulación del concepto de sistema endocannabinoide como una red de señalización fisiológica compuesta por receptores, ligandos y enzimas metabólicas encargadas de regular su síntesis y degradación (Di Marzo et al., 1998).
A finales de la década de 1990 y principios de los años 2000, diversos estudios identificaron las principales enzimas responsables del metabolismo de los endocannabinoides, incluyendo la fatty acid amide hydrolase (FAAH), implicada en la degradación de la anandamida, y la monoacylglycerol lipase (MAGL), responsable de la hidrólisis del 2-AG (Cravatt et al., 1996; Dinh et al., 2002).
La identificación de estos componentes permitió establecer el marco conceptual actual del sistema endocannabinoide como un sistema de señalización lipídica dinámico, implicado en la regulación de múltiples procesos fisiológicos mediante mecanismos de comunicación celular altamente especializados.
Componentes del sistema endocannabinoide
El sistema endocannabinoide está constituido por tres grupos principales de elementos moleculares:
-
Receptores cannabinoides
-
Endocannabinoides
-
Enzimas responsables de su biosíntesis y degradación
Estos componentes forman una red de señalización lipídica altamente regulada que permite la modulación de procesos fisiológicos mediante mecanismos de comunicación celular dependientes de lípidos bioactivos (Di Marzo, 2008; Lu & Mackie, 2016).
A diferencia de muchos sistemas clásicos de neurotransmisión basados en moléculas hidrosolubles almacenadas en vesículas sinápticas, la señalización endocannabinoide se caracteriza por la producción transitoria de mediadores lipídicos a partir de fosfolípidos de membrana, seguida de su rápida degradación enzimática.
Receptores cannabinoides
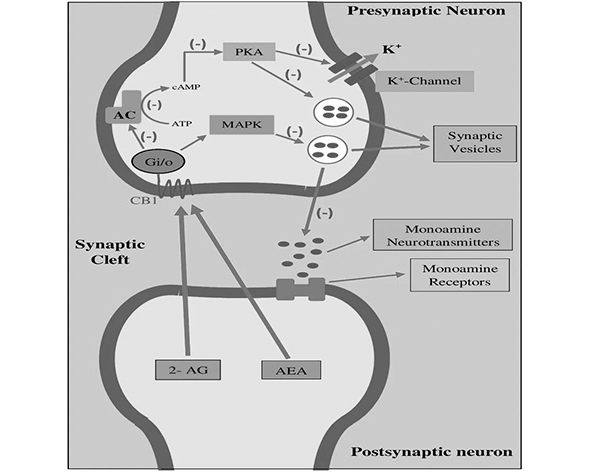
Los receptores cannabinoides pertenecen a la familia de los receptores acoplados a proteínas G (GPCR), una de las familias de receptores más extensas en organismos vertebrados. Estos receptores se caracterizan por presentar siete dominios transmembrana y por acoplarse principalmente a proteínas Gi/o, lo que conduce a la inhibición de la adenilato ciclasa y a la modulación de diversas rutas de señalización intracelular (Howlett et al., 2002).
Los dos receptores cannabinoides mejor caracterizados son CB1 y CB2, aunque investigaciones recientes han identificado otras posibles dianas moleculares capaces de responder a cannabinoides o compuestos relacionados.
Receptor CB1
El receptor cannabinoide tipo 1 (CB1) es uno de los receptores GPCR más abundantes en el sistema nervioso central. Su expresión se ha detectado en múltiples regiones cerebrales, incluyendo el hipocampo, cerebelo, ganglios basales, corteza cerebral y amígdala, lo que refleja su papel en la modulación de procesos neuronales complejos (Herkenham et al., 1990; Mackie, 2008).
A nivel celular, la activación de CB1 produce diversos efectos intracelulares, entre ellos:
-
inhibición de la adenilato ciclasa
-
reducción de los niveles intracelulares de AMP cíclico (cAMP)
-
modulación de canales iónicos dependientes de voltaje
-
activación de rutas de señalización como MAPK/ERK
En terminales presinápticas, la activación de CB1 suele conducir a una disminución de la liberación de neurotransmisores, incluyendo glutamato, GABA, dopamina y acetilcolina, lo que explica su papel modulador en la transmisión sináptica.
Receptor CB2
El receptor cannabinoide tipo 2 (CB2) fue identificado inicialmente en células del sistema inmunitario y tejidos periféricos (Munro et al., 1993). A diferencia de CB1, cuya expresión es predominante en el sistema nervioso central, CB2 se encuentra principalmente en:
-
células inmunitarias
-
macrófagos
-
células B y T
-
tejidos hematopoyéticos
Posteriormente se ha observado que CB2 también puede expresarse en determinadas poblaciones celulares del sistema nervioso, especialmente en células gliales y microglía, lo que sugiere un posible papel en la regulación de procesos neuroinmunológicos.
Endocannabinoides
Los endocannabinoides son mediadores lipídicos derivados de ácidos grasos poliinsaturados que actúan como ligandos endógenos de los receptores cannabinoides. Estos compuestos se sintetizan a partir de fosfolípidos de membrana y se liberan en respuesta a estímulos celulares específicos.
Entre los endocannabinoides identificados hasta la fecha, los dos mejor caracterizados son anandamida (AEA) y 2-araquidonoilglicerol (2-AG).
Anandamida (AEA)
La anandamida, también conocida como N-araquidonoiletanolamina, fue el primer endocannabinoide identificado (Devane et al., 1992). Este compuesto presenta afinidad moderada por el receptor CB1 y actúa como agonista parcial en este receptor.
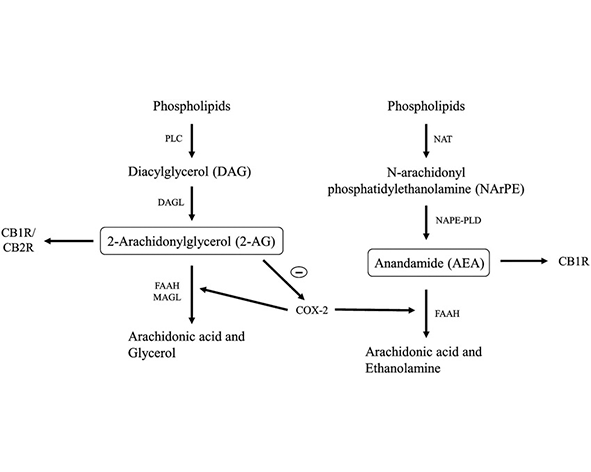
La anandamida se sintetiza principalmente a partir de N-acilfosfatidiletanolaminas (NAPE) mediante una serie de reacciones enzimáticas que implican la actividad de la enzima NAPE-fosfolipasa D (NAPE-PLD).
En comparación con el 2-AG, la anandamida suele encontrarse en concentraciones tisulares relativamente bajas, aunque su actividad biológica puede ser significativa debido a su capacidad para interactuar con múltiples dianas moleculares, incluyendo receptores cannabinoides y canales iónicos como TRPV1.
2-araquidonoilglicerol (2-AG)
El 2-araquidonoilglicerol (2-AG) es el endocannabinoide más abundante en el cerebro y en numerosos tejidos periféricos (Sugiura et al., 1995).
Este compuesto actúa como agonista completo de los receptores CB1 y CB2 y desempeña un papel central en la señalización endocannabinoide a nivel sináptico.
El 2-AG se sintetiza principalmente a partir de diacilgliceroles (DAG) mediante la acción de las enzimas diacilglicerol lipasas (DAGLα y DAGLβ). Tras su liberación, el 2-AG puede difundir a través de la membrana celular y activar receptores cannabinoides en células vecinas o en terminales presinápticas.
Enzimas del sistema endocannabinoide
La señalización endocannabinoide está estrechamente regulada por enzimas que controlan tanto la biosíntesis como la degradación de los endocannabinoides.
Entre las enzimas degradativas más relevantes se encuentran:
FAAH
La fatty acid amide hydrolase (FAAH) es una enzima responsable de la hidrólisis de la anandamida, produciendo ácido araquidónico y etanolamina (Cravatt et al., 1996).
Esta enzima se localiza principalmente en el retículo endoplasmático y desempeña un papel fundamental en la terminación de la señalización mediada por anandamida.
MAGL
La monoacylglycerol lipase (MAGL) es la principal enzima responsable de la degradación del 2-AG, catalizando su hidrólisis para generar ácido araquidónico y glicerol (Dinh et al., 2002).
Se estima que aproximadamente el 80-85 % de la degradación del 2-AG en el cerebro depende de la actividad de MAGL, lo que la convierte en un regulador clave de la señalización endocannabinoide.
Otras enzimas implicadas
Además de FAAH y MAGL, se han identificado otras enzimas que pueden participar en el metabolismo de los endocannabinoides, incluyendo:
-
ABHD6
-
ABHD12
-
COX-2
Estas enzimas pueden contribuir a la regulación fina de los niveles de endocannabinoides en distintos contextos fisiológicos.
Mecanismos de señalización endocannabinoide
La señalización endocannabinoide representa un mecanismo de comunicación intercelular basado en mediadores lipídicos sintetizados bajo demanda, que actúan principalmente mediante señalización retrógrada en sinapsis neuronales. Este sistema permite que neuronas postsinápticas modulen la actividad de terminales presinápticas mediante la liberación transitoria de endocannabinoides que difunden a través de la membrana celular y activan receptores cannabinoides (Kano et al., 2009; Castillo et al., 2012).
A diferencia de neurotransmisores clásicos como glutamato o GABA, que se liberan desde terminales presinápticas hacia neuronas postsinápticas, los endocannabinoides suelen actuar en dirección inversa, constituyendo uno de los ejemplos más estudiados de señalización retrógrada en el sistema nervioso central.
Señalización retrógrada sináptica
El mecanismo fundamental de señalización endocannabinoide en sinapsis neuronales puede describirse en varias etapas:
-
Activación postsináptica
Un incremento en la actividad neuronal postsináptica, frecuentemente asociado a aumentos en la concentración intracelular de Ca²⁺ o a la activación de receptores acoplados a proteínas G, desencadena la síntesis de endocannabinoides a partir de fosfolípidos de membrana.
-
Síntesis y liberación de endocannabinoides
Los endocannabinoides, principalmente 2-AG y en menor medida anandamida, se sintetizan de novo mediante enzimas específicas como DAGLα o NAPE-PLD. Una vez generados, estos lípidos difunden localmente a través de la membrana plasmática.
-
Activación presináptica de CB1
Tras su difusión, los endocannabinoides se unen a receptores CB1 localizados en terminales presinápticas, donde desencadenan la activación de proteínas Gi/o.
-
Modulación de la liberación de neurotransmisores
La activación presináptica de CB1 produce varios efectos intracelulares que culminan en una disminución de la liberación de neurotransmisores, incluyendo:
-
inhibición de canales de calcio dependientes de voltaje
-
activación de canales de potasio
-
reducción de la actividad de la adenilato ciclasa
-
El resultado final es una modulación temporal de la transmisión sináptica, permitiendo a la neurona postsináptica ajustar la intensidad de la señal que recibe.
Supresión inducida por despolarización
Uno de los fenómenos mejor caracterizados de señalización endocannabinoide es la supresión inducida por despolarización de la inhibición (DSI) y la supresión inducida por despolarización de la excitación (DSE).
Estos procesos reflejan la capacidad de los endocannabinoides para modular diferentes tipos de sinapsis.
DSI — Depolarization-induced suppression of inhibition
La DSI consiste en una disminución transitoria de la liberación de neurotransmisores inhibitorios, principalmente GABA, tras la despolarización de una neurona postsináptica.
Este fenómeno se produce cuando el aumento de Ca²⁺ intracelular induce la síntesis de endocannabinoides que activan receptores CB1 en terminales presinápticas de interneuronas GABAérgicas (Wilson & Nicoll, 2001).
DSE — Depolarization-induced suppression of excitation
De forma análoga, la DSE implica una reducción transitoria de la liberación de neurotransmisores excitatorios, particularmente glutamato, mediante un mecanismo similar dependiente de la activación de receptores CB1 en terminales presinápticas glutamatérgicas.
Este mecanismo permite una regulación dinámica del equilibrio entre excitación e inhibición dentro de circuitos neuronales (Kreitzer & Regehr, 2001).
Regulación de la plasticidad sináptica
Además de sus efectos transitorios sobre la transmisión sináptica, la señalización endocannabinoide también participa en procesos de plasticidad sináptica a largo plazo.
Entre los fenómenos más estudiados se encuentra la depresión a largo plazo mediada por endocannabinoides (eCB-LTD), un proceso mediante el cual la activación prolongada de receptores CB1 conduce a una disminución sostenida de la eficacia sináptica.
Este tipo de plasticidad se ha observado en diversas regiones cerebrales, incluyendo:
-
hipocampo
-
corteza prefrontal
-
estriado
-
cerebelo
y se considera relevante para procesos como aprendizaje, memoria y adaptación neuronal (Heifets & Castillo, 2009).
Regulación espacial y temporal de la señalización
Una característica fundamental del sistema endocannabinoide es la limitada duración temporal de la señalización, que se debe a la rápida degradación de los endocannabinoides por enzimas metabólicas.
La anandamida es degradada principalmente por FAAH, mientras que el 2-AG es hidrolizado mayoritariamente por MAGL, aunque otras enzimas como ABHD6 y ABHD12 también contribuyen a su metabolismo (Blankman et al., 2007).
Este control enzimático asegura que la señalización endocannabinoide sea localizada y transitoria, evitando efectos prolongados sobre la actividad neuronal.
Importancia funcional
La capacidad del sistema endocannabinoide para modular la liberación de neurotransmisores en sinapsis excitatorias e inhibitorias lo convierte en un regulador clave de la actividad neuronal.
Diversos estudios han demostrado que este sistema participa en la regulación de:
-
excitabilidad neuronal
-
circuitos de recompensa
-
procesamiento emocional
-
aprendizaje y memoria
-
regulación del dolor
Debido a esta función moduladora, el sistema endocannabinoide se considera uno de los principales mecanismos homeostáticos del sistema nervioso central.
Distribución del sistema endocannabinoide en el organismo
El sistema endocannabinoide presenta una amplia distribución en el organismo, lo que refleja su papel como modulador fisiológico global. La expresión de receptores cannabinoides, así como la presencia de enzimas implicadas en la síntesis y degradación de endocannabinoides, se ha documentado en múltiples tejidos y sistemas orgánicos (Lu & Mackie, 2016; Di Marzo, 2008).
Aunque inicialmente se consideró un sistema predominantemente neuronal debido a la elevada densidad del receptor CB1en el cerebro, investigaciones posteriores han demostrado que los componentes del SEC se encuentran distribuidos en una gran variedad de tejidos periféricos, incluyendo órganos metabólicos, tejidos inmunitarios y sistemas endocrinos.
Sistema nervioso central
El sistema nervioso central (SNC) constituye una de las regiones con mayor densidad de receptores cannabinoides, especialmente del receptor CB1. Estudios de autoradiografía y técnicas de inmunohistoquímica han demostrado una distribución heterogénea de estos receptores en distintas regiones cerebrales (Herkenham et al., 1990).
Entre las regiones con mayor expresión de CB1 se encuentran:
-
hipocampo, asociado a procesos de memoria y aprendizaje
-
cerebelo, implicado en coordinación motora
-
ganglios basales, relacionados con el control del movimiento
-
corteza cerebral, involucrada en funciones cognitivas superiores
-
amígdala, relacionada con procesamiento emocional
Esta distribución explica la capacidad del sistema endocannabinoide para modular diversas funciones neuronales, incluyendo la plasticidad sináptica, la regulación del tono emocional y la modulación del dolor.
Además del receptor CB1, el receptor CB2 también puede encontrarse en el sistema nervioso central, particularmente en células gliales y microglía, donde se ha asociado con procesos neuroinmunológicos y respuestas inflamatorias en el tejido nervioso.
Sistema nervioso periférico
Los componentes del sistema endocannabinoide también se encuentran presentes en el sistema nervioso periférico, incluyendo neuronas sensoriales y fibras nerviosas autónomas.
En estas regiones, la señalización endocannabinoide puede influir en procesos como:
-
transmisión nociceptiva
-
regulación de reflejos autonómicos
-
modulación de señales sensoriales periféricas
La presencia de receptores cannabinoides en neuronas periféricas contribuye a la modulación de la transmisión del dolor y de otras señales sensoriales procedentes de tejidos periféricos.
Sistema inmunitario
El sistema endocannabinoide desempeña un papel importante en la regulación de funciones inmunológicas. El receptor CB2 se expresa ampliamente en diversas células del sistema inmunitario, incluyendo:
-
linfocitos B
-
linfocitos T
-
macrófagos
-
células dendríticas
-
células NK
La activación de CB2 puede influir en procesos como la migración celular, la liberación de citocinas y la regulación de respuestas inflamatorias, lo que sugiere una función moduladora del sistema endocannabinoide en la actividad inmunitaria (Klein, 2005).
Tejidos metabólicos
Los componentes del sistema endocannabinoide también se han identificado en tejidos implicados en la regulación del metabolismo energético, como:
-
hígado
-
tejido adiposo
-
músculo esquelético
-
páncreas
En estos tejidos, la señalización endocannabinoide puede participar en la regulación de procesos metabólicos relacionados con el equilibrio energético, la homeostasis lipídica y la sensibilidad a la insulina (Cota et al., 2003).
La presencia de receptores CB1 en tejidos metabólicos ha sido objeto de numerosas investigaciones debido a su posible papel en la regulación del apetito y del metabolismo energético.
Sistema digestivo
El sistema endocannabinoide también se encuentra ampliamente distribuido en el tracto gastrointestinal, donde sus componentes se localizan en:
-
neuronas entéricas
-
células epiteliales intestinales
-
terminaciones nerviosas sensoriales
En este contexto, la señalización endocannabinoide puede participar en la regulación de diversas funciones digestivas, incluyendo:
-
motilidad intestinal
-
secreción gastrointestinal
-
percepción visceral
Estos mecanismos sugieren que el sistema endocannabinoide desempeña un papel modulador en la fisiología gastrointestinal.
Sistema endocrino y reproductivo
Diversos estudios han identificado la presencia de componentes del sistema endocannabinoide en órganos endocrinos y tejidos reproductivos.
Entre los tejidos en los que se ha descrito actividad endocannabinoide se incluyen:
-
hipotálamo
-
hipófisis
-
gónadas
En estos contextos, el sistema endocannabinoide puede interactuar con mecanismos hormonales que regulan procesos como la secreción endocrina, la reproducción y el desarrollo embrionario.
Significado fisiológico de su distribución
La amplia distribución del sistema endocannabinoide sugiere que este sistema actúa como un modulador fisiológico de amplio alcance, capaz de influir en la actividad de múltiples sistemas orgánicos.
Esta presencia en diferentes tejidos permite que los endocannabinoides funcionen como mediadores que integran señales neuronales, inmunológicas y metabólicas, contribuyendo al mantenimiento de la homeostasis en condiciones fisiológicas y frente a cambios ambientales.
Función fisiológica y homeostasis
El sistema endocannabinoide desempeña un papel central en la regulación homeostática del organismo, actuando como un modulador fisiológico capaz de integrar señales neuronales, inmunológicas y metabólicas. A través de la activación de receptores cannabinoides por ligandos endógenos, este sistema permite ajustar la actividad celular y tisular en respuesta a cambios en el entorno interno y externo (Di Marzo, 2008; Lu & Mackie, 2016).
La homeostasis biológica implica la capacidad de los organismos para mantener condiciones internas relativamente estables frente a fluctuaciones ambientales. En este contexto, el sistema endocannabinoide actúa como un sistema modulador retroalimentado, capaz de regular múltiples procesos fisiológicos mediante la modulación de vías de señalización intracelular.
Diversos estudios han demostrado que los endocannabinoides participan en la regulación de funciones tan diversas como la neurotransmisión, la respuesta inmunitaria, el metabolismo energético y la adaptación al estrés fisiológico.
Regulación de la neurotransmisión
En el sistema nervioso central, el sistema endocannabinoide actúa principalmente como un modulador de la transmisión sináptica. Mediante mecanismos de señalización retrógrada, los endocannabinoides liberados por neuronas postsinápticas pueden reducir la liberación de neurotransmisores en terminales presinápticas que expresan receptores CB1 (Kano et al., 2009).
Este mecanismo permite ajustar la intensidad de la señal neuronal en circuitos excitatorios e inhibitorios, contribuyendo a mantener el equilibrio entre diferentes sistemas de neurotransmisión.
En particular, la señalización endocannabinoide puede modular la liberación de neurotransmisores como:
-
glutamato, principal neurotransmisor excitatorio del sistema nervioso central
-
GABA, principal neurotransmisor inhibitorio
-
dopamina, implicada en circuitos de recompensa y motivación
-
acetilcolina, relacionada con procesos cognitivos y neuromusculares
La modulación de estos sistemas de neurotransmisión sitúa al SEC como un regulador clave de la excitabilidad neuronal y la plasticidad sináptica.
Regulación del metabolismo energético
El sistema endocannabinoide también desempeña un papel relevante en la regulación del equilibrio energético y del metabolismo.
Diversas investigaciones han demostrado que los receptores CB1 se expresan en regiones del cerebro implicadas en el control del apetito, particularmente en el hipotálamo, donde pueden influir en la regulación de la ingesta alimentaria (Cota et al., 2003).
Además de sus efectos centrales, los componentes del SEC se encuentran presentes en tejidos metabólicos periféricos, incluyendo:
-
hígado
-
tejido adiposo
-
músculo esquelético
En estos tejidos, la señalización endocannabinoide puede participar en la regulación de procesos como:
-
metabolismo lipídico
-
almacenamiento de energía
-
utilización de glucosa
Estos hallazgos sugieren que el sistema endocannabinoide forma parte de una red fisiológica compleja que coordina la homeostasis energética a nivel sistémico.
Regulación de la respuesta inmunitaria
El receptor cannabinoide CB2, ampliamente expresado en células del sistema inmunitario, desempeña un papel importante en la regulación de procesos inmunológicos.
La activación de CB2 puede influir en la actividad de diversas células inmunitarias, incluyendo linfocitos, macrófagos y células dendríticas, modulando la liberación de citocinas y otros mediadores inflamatorios (Klein, 2005).
A través de estos mecanismos, el sistema endocannabinoide puede contribuir a la regulación de la respuesta inflamatoria, actuando como modulador de la actividad inmunitaria en distintos contextos fisiológicos.
Regulación del estrés y la adaptación fisiológica
El sistema endocannabinoide también participa en la regulación de la respuesta del organismo frente a situaciones de estrés fisiológico o psicológico.
Diversos estudios han demostrado que los endocannabinoides pueden modular la actividad de estructuras cerebrales implicadas en el procesamiento del estrés y las emociones, incluyendo:
-
amígdala
-
hipocampo
-
corteza prefrontal
La señalización endocannabinoide en estas regiones cerebrales puede contribuir a ajustar la actividad neuronal asociada con respuestas adaptativas frente a estímulos estresantes (Hill et al., 2010).
Papel integrador del sistema endocannabinoide
La participación del sistema endocannabinoide en múltiples procesos fisiológicos sugiere que este sistema actúa como un regulador integrador que coordina la actividad de distintos sistemas biológicos.
Debido a su capacidad para modular simultáneamente procesos neuronales, inmunológicos y metabólicos, el SEC se considera actualmente uno de los principales sistemas homeostáticos del organismo.
Esta función integradora ha llevado a considerar al sistema endocannabinoide como un componente clave en la regulación del equilibrio fisiológico y en la adaptación del organismo frente a cambios ambientales o metabólicos.
Importancia en investigación biomédica
Desde su identificación a finales del siglo XX, el sistema endocannabinoide ha atraído una atención considerable en el ámbito de la investigación biomédica debido a su participación en una amplia variedad de procesos fisiológicos. La capacidad de este sistema para modular la actividad neuronal, inmunológica y metabólica lo ha convertido en un área de estudio relevante en múltiples disciplinas, incluyendo neurociencia, farmacología, inmunología y fisiología integrativa(Lu & Mackie, 2016).
El interés científico por el sistema endocannabinoide se ha visto impulsado tanto por el descubrimiento de los ligandos endógenos que regulan este sistema como por la caracterización de los mecanismos moleculares mediante los cuales los cannabinoides exógenos pueden interactuar con estos receptores. Estos hallazgos han permitido comprender mejor cómo los lípidos bioactivos derivados de ácidos grasos poliinsaturados pueden participar en la regulación de procesos celulares complejos.
Investigación en neurociencia
Uno de los campos en los que el sistema endocannabinoide ha sido más estudiado es la neurociencia. La elevada densidad del receptor CB1 en el sistema nervioso central, junto con la participación de los endocannabinoides en mecanismos de señalización retrógrada, ha llevado a numerosos estudios destinados a comprender su papel en la modulación de circuitos neuronales.
Investigaciones experimentales han demostrado que la señalización endocannabinoide puede influir en fenómenos como:
-
plasticidad sináptica
-
aprendizaje y memoria
-
regulación del dolor
-
procesamiento emocional
Estos procesos están relacionados con regiones cerebrales donde la expresión de CB1 es particularmente elevada, incluyendo el hipocampo, la amígdala y la corteza cerebral (Kano et al., 2009; Castillo et al., 2012).
Investigación en inmunología
El receptor CB2, predominantemente expresado en células del sistema inmunitario, ha despertado un interés considerable en investigaciones relacionadas con la regulación de la respuesta inmunitaria.
Estudios experimentales han explorado cómo la activación de receptores cannabinoides puede influir en la actividad de células inmunitarias, incluyendo linfocitos, macrófagos y células dendríticas. Estos trabajos han contribuido a ampliar la comprensión de los mecanismos mediante los cuales los lípidos bioactivos pueden participar en la modulación de procesos inflamatorios (Klein, 2005).
Investigación en metabolismo y fisiología energética
Otra área de investigación relevante se centra en el papel del sistema endocannabinoide en la regulación del metabolismo energético.
La presencia de receptores cannabinoides en tejidos metabólicos, junto con su expresión en regiones cerebrales implicadas en la regulación del apetito, ha llevado a numerosos estudios destinados a comprender cómo la señalización endocannabinoide puede influir en el equilibrio energético del organismo (Cota et al., 2003).
Estas investigaciones han contribuido a identificar el sistema endocannabinoide como un componente potencialmente relevante en la regulación de procesos metabólicos complejos.
Complejidad molecular del sistema endocannabinoide
En las últimas décadas, la investigación científica ha revelado que el sistema endocannabinoide es considerablemente más complejo de lo que se pensaba inicialmente.
Además de los receptores CB1 y CB2, se han identificado múltiples dianas moleculares capaces de interactuar con cannabinoides o compuestos relacionados, incluyendo:
-
canales iónicos de la familia TRP
-
receptores nucleares como PPAR
-
receptores acoplados a proteína G adicionales
Asimismo, el metabolismo de los endocannabinoides implica la participación de diversas enzimas adicionales que contribuyen a regular sus niveles tisulares y su actividad biológica.
Estos hallazgos han llevado a algunos autores a proponer el concepto de “endocannabinoidome”, un término utilizado para describir la red ampliada de lípidos bioactivos, receptores y enzimas relacionados con la señalización endocannabinoide (Di Marzo & Piscitelli, 2015).
Perspectivas de investigación futura
A pesar de los avances realizados en las últimas décadas, el sistema endocannabinoide continúa siendo objeto de una intensa investigación científica.
Los estudios actuales se centran en comprender con mayor precisión:
-
la diversidad de mediadores lipídicos implicados en la señalización endocannabinoide
-
las interacciones entre el sistema endocannabinoide y otros sistemas de señalización celular
-
los mecanismos moleculares que regulan la síntesis y degradación de endocannabinoides
La creciente comprensión de estos procesos ha contribuido a consolidar el sistema endocannabinoide como un campo de estudio relevante dentro de la biología molecular y la fisiología moderna.
Referencias
- Blankman JL, Simon GM, Cravatt BF. (2007). A comprehensive profile of brain enzymes that hydrolyze the endocannabinoids 2-arachidonoylglycerol and anandamide. Chemistry & Biology. - Castillo PE, Younts TJ, Chávez AE, Hashimotodani Y. (2012). Endocannabinoid signaling and synaptic function. Neuron. - Cota D, Marsicano G, Tschöp M, et al. (2003). The endogenous cannabinoid system affects energy balance via central orexigenic drive and peripheral lipogenesis. Journal of Clinical Investigation. - Cravatt BF, Giang DK, Mayfield SP, et al. (1996). Molecular characterization of an enzyme that degrades neuromodulatory fatty-acid amides. Nature. - Devane WA, Dysarz FA, Johnson MR, Melvin LS, Howlett AC. (1988). Determination and characterization of a cannabinoid receptor in rat brain. Molecular Pharmacology. - Devane WA, Hanus L, Breuer A, et al. (1992). Isolation and structure of a brain constituent that binds to the cannabinoid receptor. Science. - Di Marzo V. (2008). Targeting the endocannabinoid system: to enhance or reduce? Nature Reviews Drug Discovery. - Di Marzo V, Piscitelli F. (2015). The endocannabinoid system and its modulation by phytocannabinoids. Neurotherapeutics. - Dinh TP, Carpenter D, Leslie FM, et al. (2002). Brain monoglyceride lipase participating in endocannabinoid inactivation. PNAS. - Herkenham M, Lynn AB, Johnson MR, et al. (1990). Characterization and localization of cannabinoid receptors in rat brain. Proceedings of the National Academy of Sciences. - Hill MN, Patel S, Carrier EJ, et al. (2010). The endocannabinoid system and stress: implications for anxiety and mood disorders. Nature Reviews Neuroscience. - Howlett AC, Barth F, Bonner TI, et al. (2002). International Union of Pharmacology. Classification of cannabinoid receptors. Pharmacological Reviews. - Kano M, Ohno-Shosaku T, Hashimotodani Y, Uchigashima M, Watanabe M. (2009). Endocannabinoid-mediated control of synaptic transmission. Physiological Reviews. - Klein TW. (2005). Cannabinoid-based drugs as anti-inflammatory therapeutics. Nature Reviews Immunology. - Lu HC, Mackie K. (2016). An introduction to the endogenous cannabinoid system. Biological Psychiatry. - Mackie K. (2008). Cannabinoid receptors: where they are and what they do. Handbook of Experimental Pharmacology. - Matsuda LA, Lolait SJ, Brownstein MJ, Young AC, Bonner TI. (1990). Structure of a cannabinoid receptor and functional expression of the cloned cDNA. Nature. - Mechoulam R, Ben-Shabat S, Hanus L, et al. (1995). Identification of an endogenous 2-monoglyceride cannabinoid receptor agonist. Biochemical Pharmacology. - Munro S, Thomas KL, Abu-Shaar M. (1993). Molecular characterization of a peripheral receptor for cannabinoids. Nature. - Sugiura T, Kondo S, Sukagawa A, et al. (1995). 2-Arachidonoylglycerol: a possible endogenous cannabinoid receptor ligand in brain. Biochemical and Biophysical Research Communications. - Wilson RI, Nicoll RA. (2001). Endogenous cannabinoids mediate retrograde signalling at hippocampal synapses. Nature.